自然杀伤(NK)细胞是先天淋巴细胞中最早被发现的成员,通过细胞毒性和细胞因子分泌参与肿瘤和病原体的防御。最初被称为“无效细胞”,因缺少其他淋巴细胞的标记物,技术进步揭示了NK细胞在宿主防御和免疫调节中的重要性。如今,单细胞RNA测序和多参数流式细胞术等技术可深入分析其多样性。
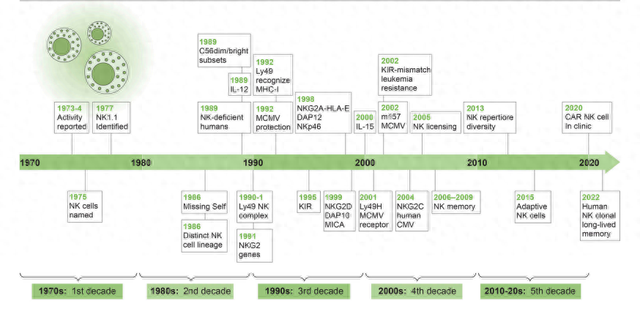
近期,《Journal of Experimental Medicine》刊登了加州大学Lewis L. Lanier博士的回顾性文章,基于他在2023年9月26日挪威第20次Nature Immunity学会会议上的主题演讲,回顾了过去50年NK细胞研究的重要进展。Lanier博士在过去40年中一直是NK细胞生物学研究的领军人物。
第一个十年:1973–1982;一种新的、非抗原特异性的细胞毒性淋巴细胞群体
在20世纪60年代末,开发了一种简单的体外51Cr释放测定法,用于定量测量细胞介导的细胞毒性。许多免疫学家利用此工具研究细胞毒性T淋巴细胞对同种异体和肿瘤细胞的杀伤能力。1974年,Herberman等人发现健康个体的外周血淋巴细胞能杀死多种人类淋巴母细胞,包括自体细胞系。1975年,Jondal和Pross报告,正常供体的非胸腺淋巴细胞对某些自体和异体淋巴细胞具有自发的细胞毒性,可能与携带补体受体的淋巴细胞有关。

同时,研究显示,年轻近交系小鼠的淋巴细胞也能在体外杀死敏感肿瘤细胞系。1973年,Herberman等人在研究MSV免疫小鼠时指出,正常淋巴细胞也有低水平的细胞毒性,不会被抗Thy1消除。Kiessling、Klein和Wigzell在一篇里程碑式论文中描述了非荷瘤近交系小鼠淋巴细胞对同基因和异基因莫罗尼白血病细胞的裂解活性,称之为“自然杀伤”,并认为这些效应细胞是一种新型淋巴细胞。
随后,Kiessling证实自然杀伤活性不仅存在于体外,还能通过幼稚小鼠体内对YAC-1白血病细胞的排斥反应和过继转移实验得到验证。1971年,Cudkowicz和Bennett报道F1受体小鼠对亲代骨髓移植物的排斥反应,称为“杂交抗性”,违背了当时的“移植定律”。1977年的研究揭示了这种现象与NK细胞的重要联系。
第二个十年:1983–1992;“自我缺失”假说与疱疹病毒防御中的NK细胞
在第二个十年,研究重点转向NK细胞的表型表征,以便更好地检测和定量。由于其较大的细胞体积和含有穿孔素与颗粒酶的细胞质颗粒,NK细胞被称为“大颗粒淋巴细胞”。1983年,通过CD16和CD57的表达,首次鉴定了人类NK细胞的功能亚群,其中CD57标记最成熟的NK细胞群。随后发现,未成熟和成熟的NK细胞表达CD56(NCAM1),且外周血中的NK细胞主要分为CD56brightCD16−和CD56dim、CD16+两个表型,分别在细胞溶解和细胞因子产生方面有所不同。

早期对人类和小鼠NK细胞的研究表明,NK细胞可以裂解同基因和异基因肿瘤,且不受“MHC限制”。Karre等人通过化学诱变C57BL/6淋巴瘤RMA,选出H-2阴性变体RMA-S,证明NK细胞优先杀死缺乏MHC I类的肿瘤细胞。这些研究揭示了NK细胞在对抗下调MHC I类以逃避T细胞检测的病毒和肿瘤中的重要作用,并预测了MHC I类抑制性受体的存在。
研究利用β2-微球蛋白(B2m)基因敲除小鼠,证明了NK细胞可杀伤正常健康细胞。野生型小鼠的NK细胞能体外杀死B2m缺陷小鼠的免疫细胞,并排斥其骨髓移植,首次提出“NK细胞耐受性”概念,因为B2m缺陷小鼠的NK细胞无法攻击I类阴性靶细胞。80年代,关于NK细胞是否属于非常规T细胞存在争议,随着T细胞受体基因的克隆,这一问题得以深入研究。
1989年前,人们对NK细胞在人体中的生理作用存在争论。Biron等人发现一个没有NK细胞但有B和T淋巴细胞的患者,该患者因GATA2基因突变导致严重疱疹病毒感染,显示NK细胞在识别疱疹病毒中的作用。随后,发现其他基因突变也可导致NK细胞缺陷。

在接下来的十年中,许多激活和抑制NK受体基因被鉴定和克隆,如小鼠的Ly49和NKR-P1基因统称为“NK细胞基因复合体”。Scalzo等人发现Ly49H基因保护小鼠免受巨细胞病毒感染。人类NK细胞表达CD3ζ,传最有效的NK受体CD16信号。1991年,Houchins等人鉴定了NKG2基因,包括抑制性CD94-NKG2A和活化CD94-NKG2C受体,识别HLA-E为配体。早期研究表明,NK细胞产生的IFN-γ在对抗细胞内病原体和肿瘤中起重要作用,直到Trinchieri等人发现“NK细胞刺激因子”IL-12,揭示其诱导机制。IL-12由骨髓细胞产生,促使NK细胞产生IFN-γ,引导幼稚T细胞分化为Th1细胞,并激活CD8+ T细胞的抗肿瘤活性。
第三个十年:1993-2002;抑制和激活NK受体及其配体的鉴定
缺失自我假说揭示了抑制性小鼠Ly49和人类KIR受体,它们识别MHC I类并调节肿瘤杀伤,成为免疫“检查点”受体。此外,假说暗示激活受体的存在,以平衡NK细胞的抑制和激活信号。
Moretta团队发现NKp30、NKp44和NKp46天然细胞毒性受体参与肿瘤识别。NKp44、CD94-NKG2C和激活的KIR、Ly49受体通过与DAP12适配器蛋白的非共价结合传递信号。抑制性Ly49、KIR和NKG2A受体通过其细胞质结构域中的免疫受体酪氨酸基抑制基序招募酪氨酸磷酸酶发挥功能。NKG2D是一种与DAP10结合的孤儿受体,其配体由细胞应激诱导,形成NK细胞识别“改变的自我”的基础。NKG2D广泛表达于NK和T细胞亚群,是癌症和自身免疫性疾病的治疗靶点。Velardi及其同事发现,供体和受体的MHC I类与KIR不匹配可降低造血干细胞移植后白血病复发率,可能由于供体NK细胞介导的缺失自我反应。

早期研究认为,先天免疫细胞通过模式识别受体识别病原体,而非抗原特异性识别。然而,2002年发现小鼠NK细胞具有特异性识别小鼠CMV(MCMV)抗原的受体,推翻了这一观点。MCMV编码的糖蛋白m157被Ly49H受体识别,尽管它最初可能通过与抑制性Ly49受体结合来抑制NK细胞反应,但Ly49H受体的进化抵消了这一机制。这一发现为其他激活和抑制受体的进化提供了基础,如识别人类CMV的抑制性CD94-NKG2A和激活性CD94-NKG2C受体,以及与小鼠CMV m12蛋白结合的激活性NKR-P1C和抑制性NKR-P1B受体。
第四个十年:2003-2012;NK细胞“记忆”与“许可”
经典免疫学教科书认为,先天免疫细胞对以前的感染或抗原没有记忆。但2006年,von Adrian及其同事发现小鼠NK细胞可介导半抗原特异性接触超敏反应。他们在Rag缺陷小鼠中排除了T和B细胞,通过半抗原引发的NK细胞过继转移证明了抗原特异性回忆反应,尽管尚未鉴定出特异性NK受体。MCMV引发的记忆性NK细胞过继转移到幼稚宿主后,Ly49H+ NK细胞进行克隆扩增并对MCMV感染产生保护。这表明NK细胞能产生精细抗原特异性反应,并揭示了这一过程的分子基础。条形码Ly49H+ NK细胞的研究显示,MCMV感染后单个NK细胞克隆可产生10000个后代。类似地,Lopez-Botet及其同事发现人类CMV感染优先扩增表达CD94-NKG2C受体的NK细胞,线粒体DNA测序证实了CMV感染后NK细胞的克隆扩增和长期持久性。

尽管抑制性受体被认为仅抑制NK细胞活化,但研究发现缺乏自身MHC I类同源配体的NK细胞反应较差。这被解释为缺乏抑制性受体的NK细胞的“解除武装”或携带自我抑制性受体NK细胞的“许可”。最近提出的机制是SHP-1磷酸酶在“未经许可”的NK细胞中更多表达和募集,激活免疫突触,从而解除其武装。
第五个十年:2013年至今;NK细胞多样性及走向临床
过去十年中,新技术推动了NK细胞生物学的进展。2013年,Horowitz等人通过质谱细胞仪研究了健康成人外周血中的NK细胞表型多样性,在12名健康个体中发现了6000–30000个表型亚群,总共超过100000个表型。这种多样性主要由于KIR基因的多样化表达,是仅次于MHC基因的最多态人类基因。单细胞转录分析进一步显示了NK细胞的多样性。
NK细胞表观遗传学研究揭示了小鼠和人类NK细胞在CMV感染下的变化。CMV感染使人类记忆或适应性NK细胞通过甲基化FCERIG和SYK基因沉默,并通过CD3ζ和ZAP70信号传导,增强抗体依赖性细胞毒性,而在小鼠Ly49H+记忆性NK细胞中,Syk和FcεR1γ的缺失则不会发生。
NK细胞的有效转导和CRISPR基因修饰技术的发展,为其在癌症患者中的细胞疗法设计提供了可能。2020年,CD19嵌合抗原受体NK细胞在淋巴肿瘤患者中的首次临床应用显示出令人鼓舞的结果,激发了进一步提高基于NK细胞治疗效果的兴趣。尽管面临短寿命和实体瘤中微环境灭活的挑战,临床使用NK细胞及其进化机制的经验为其临床潜力提供了希望。另一个令人期待的机会是NK细胞接合剂,如靶向活化NK受体和肿瘤相关抗原的多聚体抗体的临床进展。

小结:
NK细胞在宿主防御和免疫调节中发挥重要作用。它们自然杀死肿瘤和病毒感染细胞,并在I型干扰素作用下功能增强。NK细胞通过产生干扰素-γ激活巨噬细胞和其他免疫细胞,促进CD4+T细胞功能,并在初次接触微生物时成为干扰素-γ的主要来源。Trinchieri等人发现IL-12证实了NK细胞在先天免疫和适应性免疫中的桥梁作用。树突状细胞等先天免疫细胞通过IL-12、IL-15和IL-18激活NK细胞,而NK细胞则通过分泌趋化因子、FLT3配体和干扰素-γ促进树突状细胞成熟和激活。这些相互作用在抗微生物病原体和肿瘤的初始免疫反应中至关重要。
尽管NK细胞因直接细胞溶解和促炎因子分泌而著名,最新研究显示其在免疫反应中起关键调节作用,提供负反馈以防止病理。缺乏NK细胞时,T细胞反应可能过强,损害健康组织。NK细胞通过杀死过度活化的T细胞、消除树突状细胞或分泌抑制性因子来实现这一点。研究指出,IL-10缺陷小鼠患结肠炎,NK细胞耗竭会加重病情。NK细胞分泌的IL-10在小鼠CMV感染期间限制病理和CD8+ T细胞的扩增。NK细胞功能依赖环境,在自身免疫性疾病中可能有益或有害。

研究集中在外周血和次级淋巴组织中的NK细胞,蜕膜组织的研究首次发现了具有不同特性的组织驻留NK细胞。其他组织中的许多ILC表达NK标记,最初被认为是NK细胞亚群,但后续研究显示它们属于不同谱系,功能类似于Th亚群,NK细胞是CD8+T细胞的固有对应物。
未来研究问题包括:NK细胞如何获得抗原特异性记忆?其控制自身免疫性疾病T细胞的机制及治疗潜力?如何在肿瘤微环境中防止NK细胞功能障碍或重新激活?预计未来50年对NK细胞的研究将取得重大进展。
【参考文献】Lewis L. Lanier,Five decades of natural killer cell discovery. J Exp Med (2024) 221 (8): e20231222.
