9月5日,Medigene宣布美国食品药品监督管理局(FDA)已经批准T细胞受体工程T细胞(TCR-T)疗法MDG1015用于治疗晚期胃癌的研究性新药(IND)申请。

截图来源于参考资料1,侵权请联系删除
MDG1015是一款靶向 NY-ESO-1/LAGE-1a(纽约食管鳞状细胞癌 1/L 抗原家族成员-1a)的第三代 T细胞受体工程 T 细胞(TCR-T)疗法。T细胞受体工程化T细胞(TCR-T)疗法是指通过利用基因编辑技术改造患者外周血的T细胞,然后将改造后的T细胞回输至患者体内,回输患者体内后能够发挥特异性识别和杀伤肿瘤细胞作用。
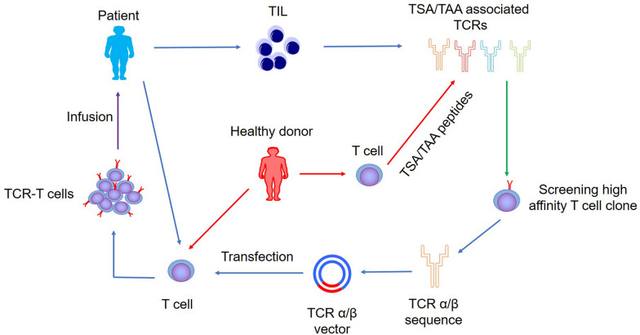
TCR-T细胞治疗转移性非小细胞肺癌
2018年,国际一流期刊《肿瘤学快报》(《Oncology Letters》)在线发表了TCR-T细胞治疗转移性非小细胞肺癌的病例报告。该患者是一名携带EGFR突变的HLA-A2阳性44岁女性肺腺癌(LADC)患者。在接受吉非替尼治疗后原发性肺肿瘤和肝转移灶稳定,但是在2.5年后病情复发,并出现新的胸膜和肝转移。随后改用厄洛替尼治疗,但是8个月后发现右侧肺门、纵隔、右侧胸膜、右侧肝叶和肝包膜疾病进展,于是患者接受TCR-T细胞治疗。
第一次输注后第43天,原发肺肿瘤消退,原发性肺病变大小从95×86×54 mm减小到64×44×54 mm。转移性肝病变也从19.8×19.6×20 mm减少到10×10×10 mm。一年后,患者病情依旧稳定。

截图来源于参考资料2,侵权请联系删除
该病例表明,TCR-T 细胞疗法可能对非小细胞肺癌患者有益。
TCR-T细胞疗法治疗肾癌
2024年美国临床肿瘤学会泌尿生殖系肿瘤分会(ASCO GU)公布了TCR-T细胞疗法治疗肾癌的临床(NCT03354390)数据,结果显示:7%的患者实现部分缓解(PR),29%的患者实现至少28周的病情稳定(SD)。
截图来源于参考资料3,侵权请联系删除
该数据表明TCR-T细胞疗法治疗肾癌有效。
TCR-T细胞疗法治疗转移性人瘤病毒相关上皮癌
2021年2月,国际顶级期刊《Nature》发表了靶向 HPV-16 E7 的TCR-T细胞疗法治疗转移性人瘤病毒相关上皮癌的临床试验(NCT02858310)数据。该试验12例患者中有一半的患者实现部分缓解(PR)。

截图来源于参考资料4,侵权请联系删除
该数据表明,靶向HPV-16 E7的TCR-T细胞疗法在转移性人瘤病毒相关上皮癌具有治疗潜力。
目前国内多家企业也在加速推进对TCR-T细胞疗法的研发。
来恩生物LioCyx-M004
LioCyx-M004是来恩生物研发一款针对乙肝病毒(HBV)的特异性T细胞受体(TCR)的自体T细胞产品。I期试验(NCT03899415)结果显示中位总生存期为33.57个月,将近3年!案例如下图:
截图来源于参考资料5,侵权请联系删除
星汉德生物SCG101
星汉德生物的SCG101是一种针对乙型肝炎表面抗原(HBsAg)特定表位的研究性细胞治疗产品。2024年欧洲肝脏研究协会年会(EASL Congress 2024)上报告了SCG101的突破性临床数据。
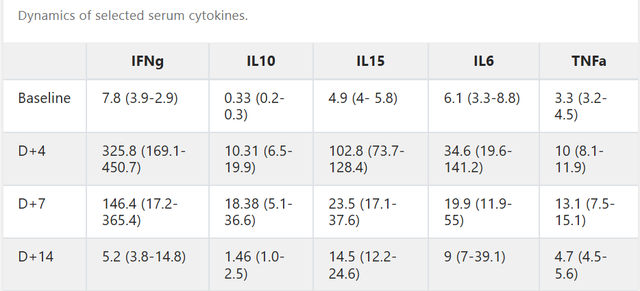
该研究中共有6例晚期乙型肝炎病毒(HBV)相关肝癌患者接受TCR-T细胞输注。结果显示:客观缓解率(ORR)达到33%,获得部分缓解(PR)的患者均维持缓解超过6个月,其中1例靶病灶完全缓解(pCR),且持续缓解超过27个月。4例患者血清HBsAg显著降低,均观察到肿瘤缩小,且无进展生存期(PFS)和生存期(OS)显著延长至5.9个月和19.0个月。
典型病例
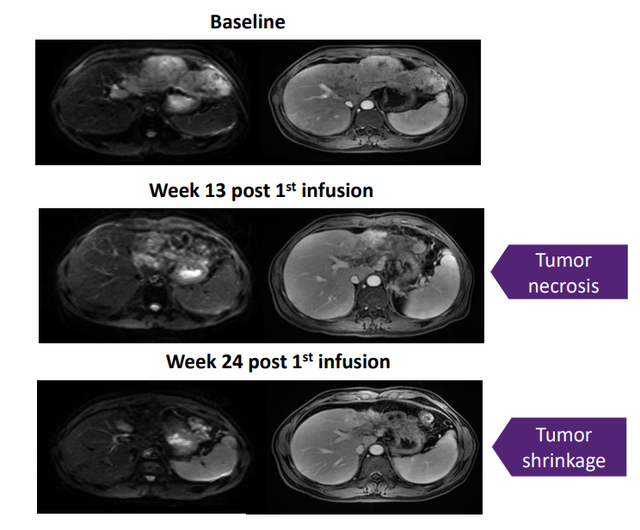
1例乙型肝炎病毒相关肝细胞癌患者,右叶有多个结节和两个目标病灶直径分别为38mm和21mm。

截图来源于参考资料6,侵权请联系删除
SCG101治疗28天后,大面积肿瘤坏死,肿瘤靶病灶分别缩小74.5%和47.5%。

截图来源于参考资料6,侵权请联系删除
该病例表明,SCG101治疗乙型肝炎病毒(HBV)相关肝细胞癌具有显著疗效。
结语
国内更多企业如:恒瑞源正的HRYZ-T101,天科雅的TC-N201、TC-E202,可瑞生物的CRTE7A2-01 TCR-T细胞注射液、科士华的KSH01等也在加速推进对TCR-T细胞疗法的研发。迄今为止,研究人员已经发表了多项TCR-T细胞疗法在实体癌中令人信服的临床数据,如滑膜肉瘤、黑色素瘤、尿路上皮癌、头颈癌、非小细胞肺癌、胃癌等,并显示出非常令人鼓舞的结果。随着科研的不断探索深入,会有更多如TCR-T、CAR-T的疗法获批上市,让患者有更加精准、多样的治疗选择!我们拭目以待!
参考资料
1.https://medigene.com/medigene-announces-u-s-fda-clearance-of-ind-application-for-mdg1015-for-multiple-solid-tumor-indications/
2.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6256329/
3.https://ascopubs.org/doi/10.1200/JCO.2024.42.4_suppl.435
4.https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9620481/
5.https://uploads-ssl.webflow.com/601374d8bb5a8e0e97896107/6020f331af6eba78c6c07f3e_2020%2C%20%5Bposter%5D%20Use%20of%20LioCyx-M.pdf
6.https://e-cmh.org/upload/pdf/cmh-2024-0058.pdf
免责声明:文本参考来源于网络,版权归原作者所有。
该文章仅供分享,如涉嫌侵犯您的著作权请联系我们删除,谢谢!