近日,一篇发表在JCR《Adipose-derived stem cell-based anti-inflammatory paracrine factor regulation for the treatment of inflammatory bowel disease》引起广泛专注,这或许给干细胞免疫调节能力提供了更明确的方向。

杂志简介:Journal of Controlled Release,简称J Control Release、JCR,创刊于1984年9月,是国际控释协会(Controlled Release Society, CRS)的官方期刊。该期刊为化学、 跨学科领域的科研人员提供了一个高影响力的论坛,使该领域的科研人员、从业人员和学生能够接触到尖端的经验性调查分析、学术对话以及行业科研成果的最新发展。该杂志通过收录高质量的原创论文和评论论文,促进该领域的应用与发展,以提高研究的质量和实用性。

1
摘要
干细胞疗法因其免疫调节特性而为治疗炎症性疾病提供了有前景的治疗手段。然而,它们在炎症组织中的生存和疗效仍然存在挑战。近日,韩国加图立大学(The Catholic University of Korea)生物技术系研究团队引入了一种新方法,通过工程化脂肪源性干细胞(ADSCs)提高其在炎症环境中的存活率,并促进旁分泌因子的分泌,以治疗炎症性肠病(IBD)。该方法的研究途径是将合成的精氨酸-甘氨酸-天冬氨酸肽-聚乙二醇-二氢卟吩e6偶联物(RPC)与ADSCs偶联,得到RPC标记的ADSCs(ARPC)。再利用RGD整合素相互作用来屏蔽干细胞,并使用二氢卟吩e6进行可视化和跟踪。ARPC在光照下表现出增强的存活率和旁分泌因子的分泌,调节炎症微环境。RNA测序分析揭示了有利于血管生成、DNA修复和外泌体分泌,同时下调炎症途径。在急性和慢性IBD的体内模型中,ARPC治疗导致炎症减少,结肠结构得以保留,调节性T细胞数量增加,突显了其治疗潜力。ARPC选择性地定位于炎症部位,证明了其靶向作用。总体而言,ARPC有望通过调节免疫反应和创造抗炎微环境,成为炎症性疾病(如IBD)的有效和安全的治疗策略。
2
研究背景
干细胞具有独特的属性,包括自我更新能力和多谱系分化潜力,使其成为组织再生和修复的宝贵工具。由于其治疗潜力,广泛的研究集中在来自骨髓和脂肪组织等各种来源的间充质干细胞(MSCs)上。据报道,干细胞具有抗炎和免疫调节活性,抑制T细胞增殖,削弱T细胞功能,并将M1巨噬细胞重新编程为M2表型。根据炎症信号的存在与否,干细胞对免疫细胞的反应不同。当面临炎症时,它们表现出抗炎行为,但当炎症不存在时,它们仍保持促炎特性。干细胞的这些治疗作用在很大程度上取决于它们的旁分泌作用,如释放细胞因子、生长因子、趋化因子或来源于其亲本细胞特性的外泌体。这些干细胞衍生物、条件培养基或细胞外囊泡迁移到炎症部位,并通过细胞内通讯改变靶细胞的活性和功能,在炎症中起着至关重要的。许多研究表明,这些衍生物对各种免疫细胞,包括树突状细胞、T细胞、B细胞和巨噬细胞具有免疫抑制作用,表明它们在炎症性疾病中起着广泛的作用。
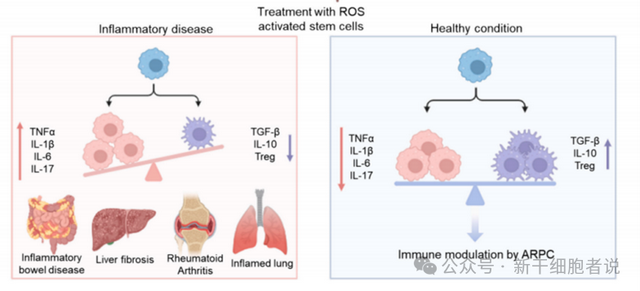
尽管干细胞疗法在治疗炎症性疾病方面具有巨大的潜力,但仍有一些挑战和局限性需要解决。临床应用的一个主要局限性是,在炎症组织中施用干细胞会抑制旁分泌因子的产生并促进细胞功能障碍。此外,炎症环境严重阻碍了移植干细胞的长期存活和有效性。通过单独施用干细胞来实现显著的治疗效果是具有挑战性的,需要改进细胞来源,规范细胞制备和递送方法,确定最佳给药方案,并解决长期安全问题。
化学偶联物RPC的制备与表征

3
研究目的
本研究旨在提高脂肪来源干细胞(ADSCs)在炎症微环境中分泌具有治疗炎症性疾病潜力的旁分泌因子。为了实现这一目标,研究者合成了一种缀合物,包含RGD肽和能够刺激干细胞的光敏剂(Chlorin e6,Ce6),RGD肽可改善炎症条件下的干细胞存活率。为了增强Ce6的亲水性,再将其与聚乙二醇(PEG)通过碳二亚胺偶联将马来酰亚胺(MAL)引入纯化的PEG-Ce6(PC)中,形成MAL-PEG-Ce6(MPC),将MPC与RGD的巯基结合合成共轭物RGD-Mal-PEG-Ce6(RPC)。RPC的紫外-可见吸收光谱在200 nm、400 nm和670 nm,显示出增强的光响应ROS生成能力,证实了RPC可作为ROS的潜力激光照射下的发生器。
探索外部介质(RGD肽和ROS)对ADSCs旁分泌因子的影响

为了评估外泌体的浓度,研究者使用BCA蛋白测定法,并在0.5 J/cm2激光照射的ARPC(ARPC(+))组中检测到外泌体蛋白的最高浓度。接下来,使用外泌体免疫染色方法,分析外泌体中特异性蛋白CD9和CD63等表面标志物的表达,确认外泌体的存在。此外,在ARPC(+)中检测到的大多数外泌体具有相同的趋势:使用ELISA对比单独用RGD处理的ADSCs、无激光照射的ARPC(ARPC(−))和有激光照射的ARPC(ARBC(+))中的细胞生长因子浓度。ARPC(+)显著增加了Ang-2、FGF、VEGF、HGF的水平,从而提高干细胞侵袭能力,刺激干细胞细胞生长或促进血管生成。
RNA测序分析

研究者使用基因本体将14523个基因分为8个簇(GO)分析:血管生成、炎症反应、细胞死亡、免疫反应、细胞周期、DNA修复、外泌体和旁分泌因子,值得注意的是,在ARPC(+)治疗组中,与血管生成、细胞周期、DNA相关的基因显著增加。

4
研究结果
结果显示,与未处理的ADSCs相比,ARPC(+)中与血管生成相关的生物途径上调。如JAK-STAT(抗凋亡作用)、NF-kB(免疫调节、凋亡、细胞生长作用)、PI3K-Akt(细胞周期调节)和VEGF(血管生成)信号通路增加。相反,与p53、Th17细胞分化和TNF信号传导等免疫激活因子分泌相关的途径似乎有所减少。
急性IBD模型中ARPC(+)的体内治疗作用

与所有动物相比,ARPC(+)治疗对DSS诱导的体重减轻具有保护作用。PBS组显示体重减轻2.1%。相比之下,ARPC(+)治疗使其体重增加19.5%。此外,ARPC(+)治疗有效地预防了DSS诱导的结肠缩短,结肠长度测量显示:与PBS处理组(5.65cm)相比,用ARPC(+)治疗的小鼠结肠长度更长(7.28cm)。脾脏重量也显示出类似的趋势。在ARPC(+)组中观察到有效缓解脾脏肿胀,可能与免疫相应有关。ARPC(+)治疗组检测到结肠组织中促炎细胞因子(IL-17、IL-1β、IL-6和TNF-α)显著降低。
3
研究结论

本研究介绍了一种开创性的分子修饰策略:结合脂肪干细胞(ADSCs)中的光响应激活机制,为未来提供了一条有前景的途径治疗性干预。精氨酸-甘氨酸-天冬氨酸的融合(RGD)肽与二氢卟吩e6(Ce6)形成RPC化合物,能够特异性结合ADSCs上的整合素受体,通过整合素介导的内吞作用促进光反应激活。这个激活机制增强ADSC行为和旁分泌活性,正如细胞因子分泌谱的改变和改善所证明的那样实验性炎症性肠病(IBD)模型中的细胞存活率。整合整合素靶向分子修饰和光响应激活标志着基于干细胞的治疗方法的重大飞跃,为各种炎症状况提供了定制治疗。然而,对长期安全性进行彻底评估,可扩展性和临床翻译势在必行,同时探索IBD之外的更广泛应用和各种药物的疗效验证临床前模型。这项研究代表了重塑基于干细胞的炎症治疗格局疾病,为精准驱动的治疗方式铺平道路正在进行的临床实施研究。

参考文献
[1] I. Ullah, R.B. Subbarao, G.J. Rho, Human mesenchymal stem cells-current trends and future prospective, Biosci. Rep. 35 (2015) e00191.[2] X.-L. Fan, Y. Zhang, X. Li, Q.-L. Fu, Mechanisms underlying the protective effects of mesenchymal stem cell-based therapy, Cell. Mol. Life Sci. 77 (2020) 2771–2794.[3] N. Song, M. Scholtemeijer, K. Shah, Mesenchymal stem cell immunomodulation: mechanisms and therapeutic potential, Trends Pharmacol. Sci. 41 (2020) 653–664.[4] H. Li, S. Shen, H. Fu, Z. Wang, X. Li, X. Sui, M. Yuan, S. Liu, G. Wang, Q. Guo, Immunomodulatory functions of mesenchymal stem cells in tissue engineering, Stem Cells Int. 2019 (2019).[5] S. Naik, S.B. Larsen, C.J. Cowley, E. Fuchs, Two to tango: dialog between immunity and stem cells in health and disease, Cell 175 (2018) 908–920.[6] J.M. Cicchese, S. Evans, C. Hult, L.R. Joslyn, T. Wessler, J.A. Millar, S. Marino, N. A. Cilfone, J.T. Mattila, J.J. Linderman, Dynamic balance of pro-and antiinflammatory signals controls disease and limits pathology, Immunol. Rev. 285 (2018) 147–167.[7] S. Dabrowska, A. Andrzejewska, M. Janowski, B. Lukomska, Immunomodulatoryand regenerative effects of mesenchymal stem cells and extracellular vesicles: therapeutic outlook for inflammatory and degenerative diseases, Front. Immunol. 11 (2021) 591065.[8] M. Kou, L. Huang, J. Yang, Z. Chiang, S. Chen, J. Liu, L. Guo, X. Zhang, X. Zhou,X. Xu, Mesenchymal stem cell-derived extracellular vesicles for immunomodulation and regeneration: a next generation therapeutic tool? Cell Death Dis. 13 (2022) 580.[9] G. Racchetti, J. Meldolesi, Extracellular vesicles of mesenchymal stem cells:therapeutic properties discovered with extraordinary success, Biomedicines 9 (2021) 667.[10] Y. Yang, Y. Peng, Y. Li, T. Shi, Y. Luan, C. Yin, Role of stem cell derivatives ininflammatory diseases, Front. Immunol. 14 (2023) 1153901.[11] M. Csobonyeiova, V. Smolinska, S. Harsanyi, M. Ivantysyn, M. Klein, The immunomodulatory role of cell-free approaches in SARS-CoV-2-induced cytokinestorm—a powerful therapeutic tool for COVID-19 patients, Biomedicines 11 (2023) 1736.[12] L. Müller, A. Tunger, M. Wobus, M. von Bonin, R. Towers, M. Bornhauser, F. Dazzi,R. Wehner, M. Schmitz, Immunomodulatory properties of mesenchymal stromal cells: an update, Front. Cell Development. Biol. 9 (2021) 637725.— END —

- 科普 情怀 责任 -
