活化能能垒。是反应速率的关键参数,通过和可量化;是反应的,影响和材料性能。二者在定义和理论本质上存在差异,活化能是宏观参数,能垒是微观势能面特征。
01、什么是活化能?
a,其标准单位为,定义为化学反应中,反应物分子转化为产物分子所必须克服的最低能量。它不是反应的总能量变化,而是反应过程中必须跨越的一个能量障碍,这个障碍通常被称为(Energy Barrier)。
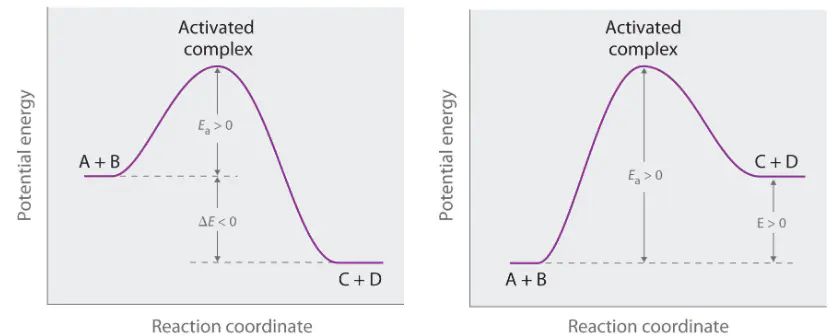
过渡态活化能,在物理图像上,就是反应物的平均能量与这个过渡态能量之间的差值DOI: 10.1002/wcms.1593
活化能有什么作用?
()反应速率的总开关高活化能意味着需要克服一个巨大的能垒低活化能意味着能垒较低温度对反应速率的巨大影响,正是通过活化能这一媒介实现的。,从而导致反应速率急剧加快。
2:催化剂之所以能够神奇地加速反应,其核心机理就是。
重要的是,,即不影响反应的整体热力学平衡。
()阿伦尼乌斯方程阿伦尼乌斯方程k其中,:速率常数,直接反映反应的快慢;A:指前因子或频率因子,代表在最佳方向上碰撞的总频率,与分子的碰撞频率和空间位阻有关。E:活化能(或kJ/mol)。R:理想气体常数(8.314J/(mol·K));K:绝对温度(K)。
速率常数与温度T呈指数关系。温度越高,指数项越大,反应速率越快。活化能E越高,指数项越小,反应速率越慢()艾林方程(Eyring Equation)过渡态理论为阿伦尼乌斯方程提供了坚实的理论基础,并推导出了更为精密的艾林方程。它将宏观的速率常数与微观的分子热力学参数直接关联起来:
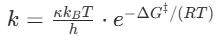
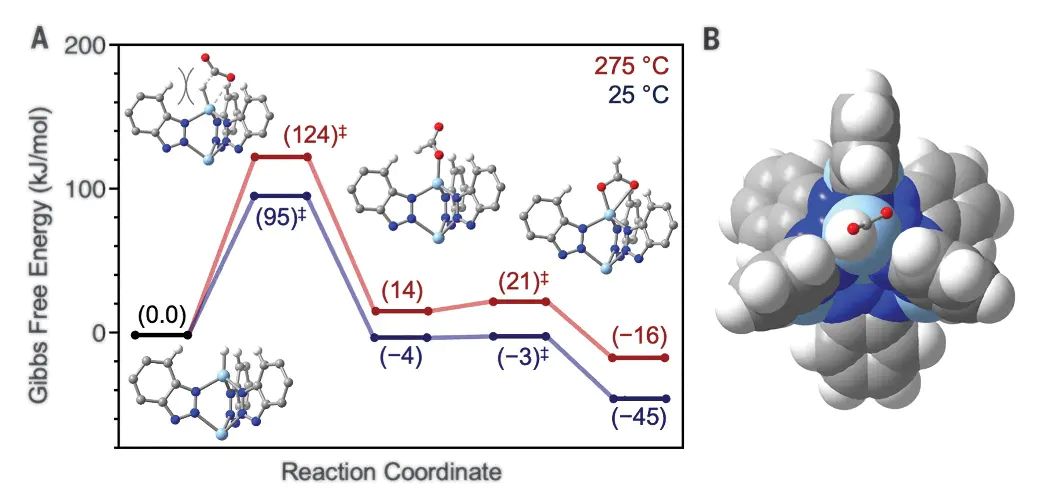
κ1k:玻尔兹曼常数;:普朗克常数;G:活化吉布斯自由能,即反应物到过渡态的吉布斯自由能变化。
艾林方程的深刻之处在于:
1不仅与温度有关,还与活化熵ΔS‡密切相关()它将能垒分解为H的贡献。H大致对应于阿伦尼乌斯活化能,反映了键的断裂和形成所需的能量变化。则反映了从反应物到过渡态时体系混乱度的变化,例如分子构象的束缚或自由度的改变。
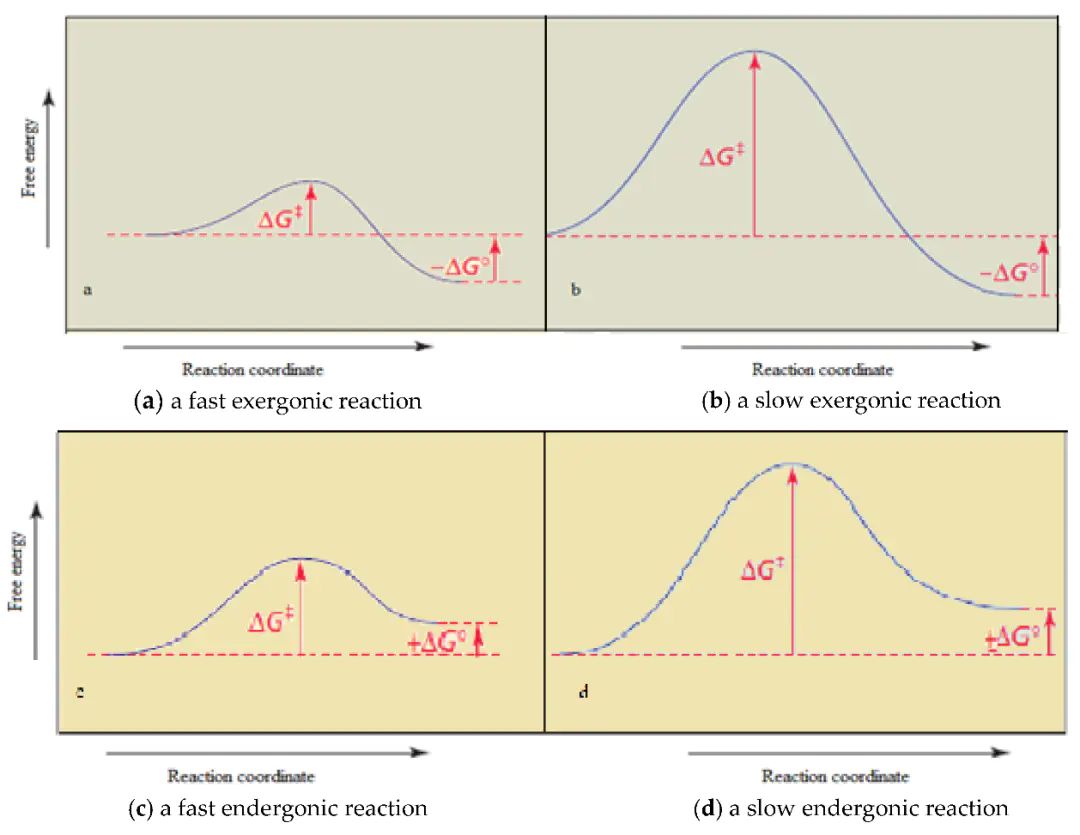
能垒是描述系统从一种稳定状态转变为另一种稳定状态所需克服的能量障碍的核心概念在物理学中,它表。
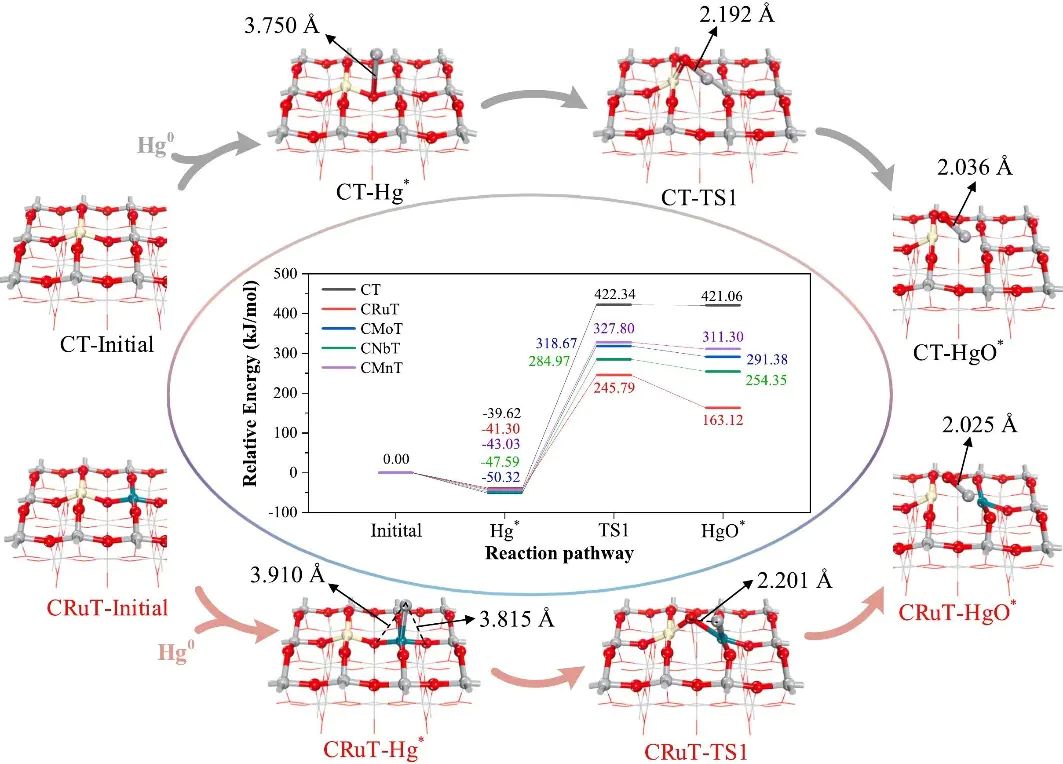
(1)热力学与动力学的桥梁作用
热力学仅决定反应的平衡位置,而动力学则通过能垒决定反应路径的可行性在复杂反应中,能垒的相对高度决定了反应路径的选择性。例如,在有机合成中,多种可能的产物往往对应不同的能垒路径,。这种能垒控制的选择性是理性设计催化剂和反应条件的理论基础。
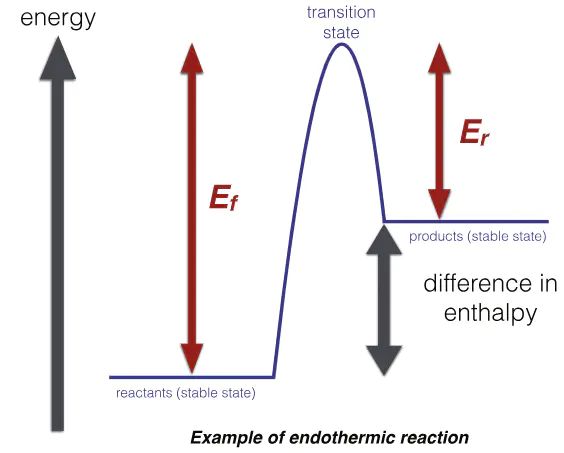
在材料科学中,能垒主导着多种关键物理过程:
散行原子或离子在晶格中的迁移需要克服迁移能垒,直接决定材料的离子导电性和自扩散系数。
马氏体相变、铁电相变等结构转变需克服相变能垒,影响相变温度和动力学路径。
电极反应的动力学由电化学能垒控制,该能垒与密切相关。
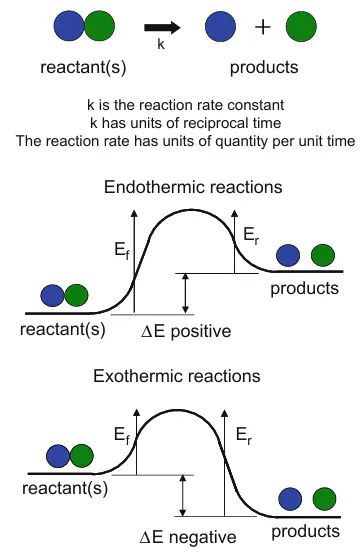
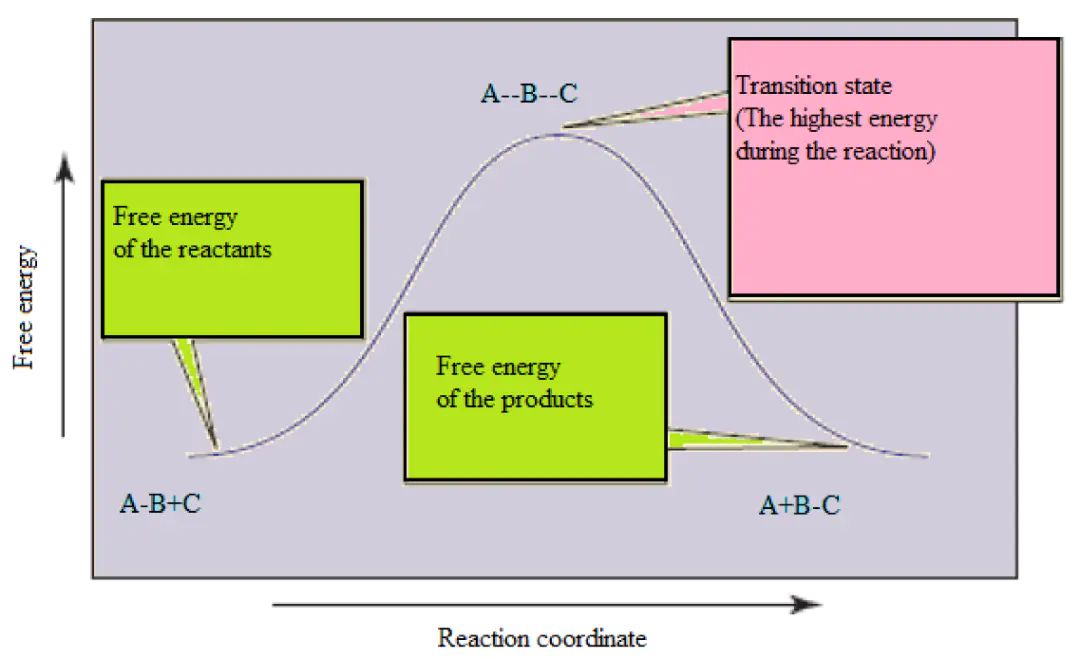
在化学动力学领域,活化能与能垒的术语混用现象极为普遍。被定义为反应物分子达到过渡态所需的最小能量,即;而则被直接描述为活化能的物理表现形式—势能面上的。
温度依赖性并非严格等价DOI: 10.1063/1.2839299
根本差异
活化能的本质是活化分子与一般分子的平均能量之差活化能能垒DOI: 10.1063/1.2839299