
2026年4月,《生物工程》期刊发表了一篇由多国研究团队完成的综述,全面阐述了胰腺类器官和诱导多能干细胞(iPSC)衍生β细胞在糖尿病治疗中的最新进展与挑战。

糖尿病仍然是全球最严重的健康挑战之一,影响着数亿患者的生活质量。目前治疗主要依赖外源性胰岛素注射,但这种方法无法模拟人体胰腺自然的胰岛素分泌模式,且无法阻止疾病进展。
01 现状传统治疗,胰岛素注射和尸体胰岛移植为糖尿病患者提供了生命支持,但这些方法存在明显局限。外源性胰岛素治疗无法完美模拟生理性胰岛素分泌,导致血糖控制不稳定。而尸体胰岛移植则面临供体短缺和慢性免疫抑制的副作用。
更根本的是,这些方法都未能解决糖尿病核心问题——胰腺β细胞的丧失或功能失调。人体胰腺中的β细胞负责感知血糖升高并分泌胰岛素,但在1型糖尿病中,自身免疫系统攻击并摧毁这些细胞;而在2型糖尿病后期,β细胞也会逐渐衰竭。
这种治疗现状凸显了对能够恢复生理性胰岛素分泌的新疗法的迫切需求。再生医学的快速发展为解决这一难题提供了全新思路。利用干细胞技术和生物工程手段,科学家们正试图“重建”或“修复”患者的胰岛素产生系统。
02 突破干细胞生物学和类器官工程的进步推动了胰腺类器官和诱导多能干细胞(iPSC)衍生β细胞的发展。胰腺类器官是从成人干细胞或多能干细胞培养的三维组织结构,能够高度模仿原生胰腺的关键特征,包括其复杂的细胞组成和空间排列。
这些微小的“迷你胰腺”可以在实验室中生长和研究,为糖尿病机制探索、药物测试提供了前所未有的平台。更令人振奋的是,它们具备成为移植材料的潜力,可能替代患者体内受损的胰岛组织。
与此同时,iPSC技术开辟了另一条道路。通过将普通细胞(如皮肤细胞)重新编程为类似胚胎干细胞的多能状态,再定向分化为胰岛素产生细胞。理论上,这项技术可以提供无限量的患者特异性β细胞,避免免疫排斥问题。
最新的进展显示,科学家已经能够制造出对葡萄糖刺激有反应的类β细胞,当血糖升高时,这些工程细胞能够分泌胰岛素。虽然实现与原生β细胞完全相同的功能成熟仍是一大挑战,但已经取得的进展足以让人看到希望。
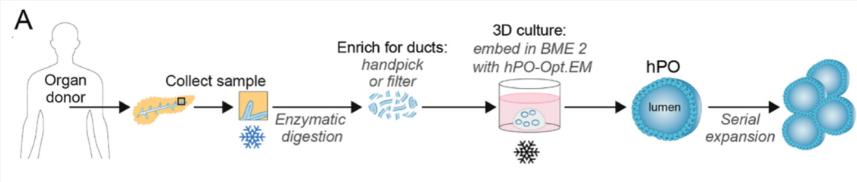 03 方法
03 方法研究人员通过多种生物工程策略提升了类器官和iPSC衍生系统的性能。生物材料支架模拟了胰腺的天然细胞外基质,为细胞生长提供物理支撑和生化信号。
微流控“器官芯片”平台创造了动态培养环境,精确控制营养输送和机械刺激,促进类器官的功能成熟。三维生物打印技术则允许在仿生支架内精确排列不同细胞类型,制造出具有特定结构的胰岛样组织。

微流控基于芯片的微生理系统设计与类器官培养及细胞配置概述
内皮共培养系统通过将β细胞与血管内皮细胞一起培养,促进了血管网络的形成,这对于移植后的存活至关重要。而基于CRISPR的基因组编辑技术则被用来优化细胞功能,甚至可能制造“隐形”细胞以避免免疫排斥。
令人印象深刻的是,光遗传学技术也被引入这一领域。科学家将对光敏感的离子通道插入人类干细胞来源的β细胞,使胰岛素分泌可以通过蓝光精确调控。在动物实验中,这些改造细胞移植后能够响应光刺激控制血糖,为无药物干预的血糖管理提供了全新思路。
04 挑战尽管前景广阔,但将这些实验室突破转化为临床疗法仍面临多重挑战。分化效率的波动使得难以大规模生产高质量的功能细胞。β细胞成熟度有限,工程细胞虽然能分泌胰岛素,但反应速度和分泌模式与天然β细胞仍有差距。
缺乏血管网络导致移植细胞难以获得足够营养和氧气,长期生存率低。免疫排斥问题在异体移植中尤为突出,即使是患者自身的iPSC衍生细胞,也可能在1型糖尿病患者中再次遭受自身免疫攻击。
可扩展制造也是一大障碍。从实验室规模扩大到临床治疗所需的数十亿细胞,需要自动化、标准化的生产流程,而当前多数方法仍依赖手工操作,批次间差异较大。
功能评估标准化的需求同样迫切。研究人员需要一致的方法来评估工程β细胞的质量和效能,包括葡萄糖刺激胰岛素分泌测试、电生理特性分析和长期稳定性评估。
05 临床近年来,胰腺类器官和干细胞衍生β细胞的临床试验已取得初步进展。
VX-880是一种由Vertex公司开发的干细胞衍生胰岛疗法,早期临床试验显示部分参与者实现了胰岛素独立性,前景看好。
Sernova公司的“细胞袋”装置试验表明,血管化的装置生态位可以支持移植胰岛的存活。
而Donislecel作为FDA批准的异体胰岛疗法,已证明在脆弱型1型糖尿病患者中细胞替代疗法的概念,尽管仍需要持续的免疫抑制。
这些早期试验面临的主要障碍包括成熟类器官的可靠生产、免疫排斥的有效管理以及可扩展的植入方法。未来的发展方向包括结合基因编辑技术创造免疫逃避型类器官、开发促进血管生成的生物材料,以及整合局部免疫调节策略。
值得注意的是,研究人员正在探索非侵入性组织获取方法,如从胰液中分离导管上皮细胞生成类器官,避免胰腺活检的风险。这为安全获取患者特异性细胞提供了新途径。
06 前景糖尿病治疗领域正处于革命性突破的前夜。生物工程、干细胞技术和基因编辑的融合正在创造出前所未有的治疗工具。胰腺类器官和iPSC衍生β细胞代表了两种互补的策略,各自具有独特优势。
成人组织来源的类器官在结构模仿方面表现优异,能够保留胰腺的微环境特征,且肿瘤发生风险较低。而iPSC衍生平台则提供了无与伦比的可扩展性,能够从少量起始细胞生产大量功能细胞。
未来成功的关键在于解决血管形成、免疫保护、功能成熟和可扩展制造这四大挑战。
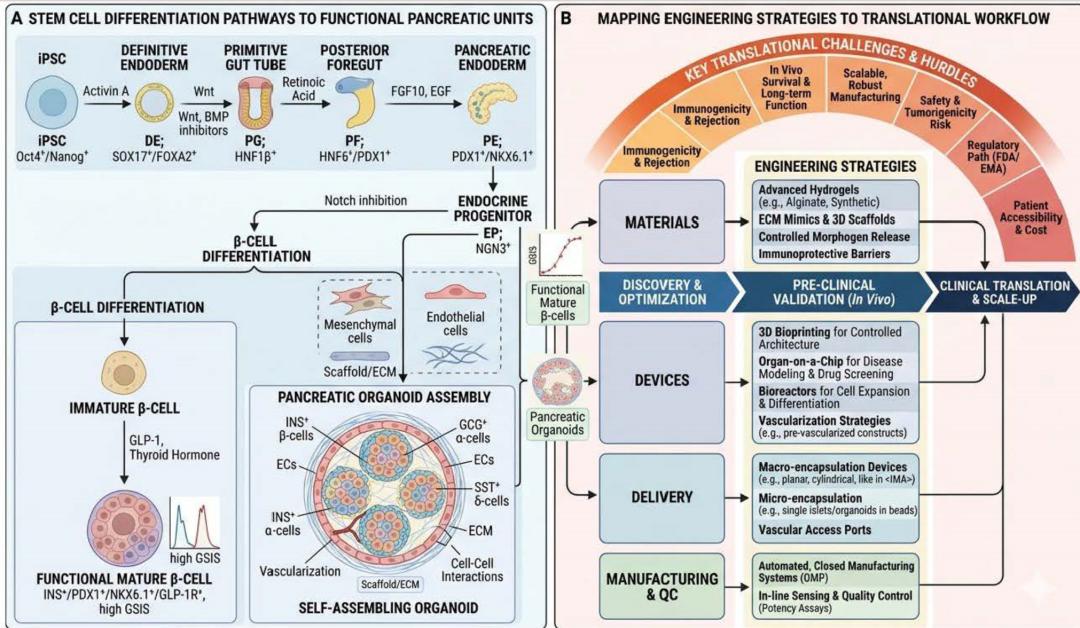
(A)部分通过模拟胚胎发育的连续信号信号,描绘了从多能干细胞到功能性胰岛素生产单位的复杂生物学旅程。(B)部分描绘了应对转化工作流程、克服免疫原性、可扩展制造和监管审批等重大临床障碍所需的多样工程策略。
基因编辑与材料科学的协同,标准化生产流程的建立,以及非侵入性细胞获取方法的完善,将推动这些技术从实验室走向临床。
随着这些生物工程方案的成熟,我们正迈向一个未来——患者特异性、工程化的胰腺单元能够为糖尿病提供永久且不依赖胰岛素的解决方案。这不仅将彻底改变糖尿病治疗模式,也将为其他器官衰竭性疾病提供可借鉴的再生医学策略。