2月18日,一项发表在《自然》杂志上的研究引发了科学界的广泛关注:针对三阴性乳腺癌新抗原的mRNA疫苗,在一项小型I期试验中,让11名患者在术后长达六年内保持无复发状态。
这一消息无疑为癌症患者带来了新的希望。传统的手术、化疗和放疗,如同外部援军直接攻击肿瘤。而癌症疫苗,则旨在训练患者自身的免疫系统,去精准识别并清除癌细胞。
癌细胞因基因突变会产生独特的蛋白质片段,这些“新抗原”如同癌细胞特有的“身份证”,是健康细胞所没有的。癌症疫苗(尤其是治疗性疫苗)的工作原理,就是将这些“身份证”信息呈递给免疫系统,教会T细胞等免疫战士锁定并攻击携带这些标识的癌细胞,实现精准打击。
图片来源于radekcho |stock.adobe.com
近期,多项关键研究为癌症疫苗领域注入了强劲动力,让我们看到其在几种难治癌症中的巨大潜力。
为最难治乳腺癌带来长久的“无复发生存”
发表在《自然》杂志上的早期研究为三阴性乳腺癌患者带来了新曙光。三阴性乳腺癌(TNBC)治疗选择有限,复发率高,是乳腺癌中极具挑战性的亚型之一。
德国美因茨大学医学中心与BioNTech合作,为14名早期TNBC术后患者接种了个性化mRNA新抗原疫苗。每支疫苗最多编码20种由患者肿瘤独有的突变产生的新抗原。
结果令人鼓舞:所有14名患者均产生了针对多种新抗原的强效T细胞免疫反应。更关键的是,在中位随访期内,11名患者在长达6年的时间里保持无复发状态。
HPV相关头颈癌的免疫联合疗法新进展
BioNTech公司开发的BNT113疫苗,是一种专门针对HPV16型E6/E7癌蛋白的mRNA疫苗。2026年1月21日,BioNTech公司宣布美国食品药品监督管理局(FDA)已授予BNT113快速通道认证,用于与帕博利珠单抗联合治疗PD-L1阳性的HPV16+头颈癌。
2024年欧洲肿瘤内科学会(ESMO)上报告了BNT113+帕博利珠单抗在HPV阳性头颈部鳞状细胞癌(HNSCC)中的试验结果:15例患者接受BNT113+帕博利珠单抗治疗,结果显示:4例患者达到完全缓解(CR),2例患者达到部分缓解(PR),中位无进展生存期(PFS)为3.9个月,估计6个月和12个月无进展生存率分别为42%和28%。中位总生存期(OS)达到22.6个月。

这些进展说明,个性化癌症疫苗有望成为免疫治疗版图上的重要拼图,为患者带来更深层、更持久的缓解。
多条赛道竞速:其他癌症疫苗技术进展
除了mRNA疫苗,全球科学家还在多条赛道上竞速:
树突状细胞(DC)疫苗:通过体外“训练”患者自身的DC细胞来指导免疫攻击。如已获批用于前列腺癌的Sipuleucel-T,中位生存期(OS)较安慰剂组长4.1个月。
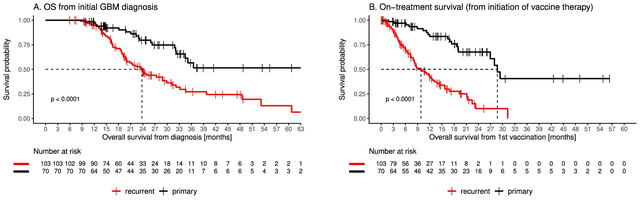
肽疫苗:使用病原体的特定片段(通常是合成肽)来引发免疫反应。2024年8月11日,《自然通讯》发表了胶质母细胞瘤(GBM)患者接受个性化新抗原衍生肽疫苗治疗的研究结果:整个队列中位总生存期(OS)达到了31.9个月,令人印象深刻的是,54%的患者在观察期结束时仍然存活。
虽然癌症疫苗的临床结果令人鼓舞,但仍旧需要更大规模的II/III期随机对照试验验证其临床获益。即使疫苗能激发强烈的免疫反应,也不等同于临床治愈。并且,目前这类治疗仍主要限于临床试验阶段,可及性有限。
结语
癌症治疗正在经历一场深刻变革。从“一刀切”的化疗,到针对特定靶点的精准治疗,再到激活人体自身防御系统的免疫治疗,我们正朝着“个体化、组合化、慢性病化管理”的方向迈进。
癌症疫苗,特别是基于新抗原的个性化疫苗,代表了这一趋势的前沿方向。它们不再试图用一种药物治疗所有患者,而是为每位患者量身定制专属的免疫教育方案。虽然前路仍有挑战,但科学探索的步伐从未停止。
2026年美国癌症协会报告带来了一个振奋人心的消息:所有癌症的五年相对生存率首次达到70%,这意味着在2015年至2021年期间确诊的患者中,十分之七的人在五年后仍然存活。这一数字相比1970年代中期的50%实现了巨大飞跃。晚期癌症的生存率也在持续改善。
这些进步的背后,是无数科研人员、临床医生和患者共同参与的不懈探索。每一次临床试验,无论结果成败,都在推动我们更接近战胜癌症的目标。
随着免疫治疗、靶向治疗和个体化医疗的飞速发展,癌症正逐渐转变为一种可防、可治、可控的慢性疾病。