在我们的高龄备孕群,干细胞是最常出现的讨论内容,干细胞疗法可以说给卵巢早衰和高龄卵巢功能减退姐妹带来的第一缕曙光。
但是,干细胞效果的不稳定性也成了一个核心痛点,所以姐妹们对干细胞效果的说法并不一致,有的认为有效,有的认为是智商税。
这背后是复杂的科学原因,外源性干细胞存活率很低,且大多不能直接转化为卵泡细胞。
近年来,科学家们意识到,干细胞难以在卵巢长期安家,真正起作用的,往往是它们短暂释放的修复信号。
沿着这一颠覆性认知,北京医院王少为医生团队取得了关键进展。
他们不再依赖不太可控的干细胞移植,他们设计出一款纳米级修复生物快递系统,将卵巢发育的关键指令浓度提升了3.5倍。

那么这种全新的治疗思路效果究竟怎样呢?研究者设计了一系列的试验进行验证,赶紧跟着圈姐一起来看看吧!
01卵巢,生命的发源地如果要想理解这项突破性研究的意义,我们首先要了解卵巢如何工作。
我们女性的卵巢在出生时就储存了她一生中所有的卵泡,大约100万到200万个,这些卵泡就是生命的种子,静静地等待被唤醒。
在每个月经周期中,大脑通过分泌促性腺激素释放激素,向垂体发出指令,垂体随即分泌促卵泡激素和黄体生成素。
这些激素抵达卵巢,唤醒一批沉睡的卵泡,通常一次约有20-30个卵泡开始发育,它们内部的卵母细胞开始生长,周围的颗粒细胞开始增殖,形成充满丰富营养的液体腔隙。
在这场唤醒中,通常只有一个卵泡能够完全成熟并排卵,其余则自然闭锁。排卵后,破裂的卵泡转化为黄体,开始分泌孕激素,为可能的妊娠做准备。
如果受精没有发生,黄体退化,月经来潮,新的周期重新开始。
这看似简单的过程背后,是无数分子信号的精密调控,任何一个环节失调,都可能导致整个系统的紊乱。
02卵巢功能衰退女性生育最大挑战现代生活方式下,卵巢功能障碍越来越普遍,生育年龄的推迟,导致高龄生育比例逐年增大,她们面临共同的问题就是卵巢功能的衰退。
这些疾病的成因复杂多样,有遗传因素、自身免疫疾病、化疗或放疗损伤、环境毒素、甚至不明原因的特发性因素。
无论病因如何,其结果都是相似的,卵巢储备减少或质量下降,激素分泌紊乱,生育能力降低,并可能伴随潮热、盗汗、情绪波动、骨质疏松等更年期症状。
传统治疗方法主要是激素替代疗法,这能缓解症状但不能恢复生育能力,且长期使用可能增加某些健康风险。
辅助生殖技术对于卵巢功能严重衰退的女性,成功率也大幅降低。
因此,医学界一直在寻找能够真正修复卵巢功能,而不仅仅是缓解症状或绕过问题的根本性解决方案。
03干细胞治疗的思路在这样的背景下,干细胞治疗成为了研究热点,干细胞具有自我更新和分化为多种细胞类型的潜力,理论上可以替换任何受损的组织细胞,卵巢细胞也不例外。
这个团队发明了一种新方法,这个新方法可以形象地理解为给受损卵巢贴上一个智能修复贴(学术名为卵巢再生补片,英文缩写ORP)。
它是一个安全的人体可吸收医用支架和一层修复精华液构成,这个修复精华提取自新生儿的脐带干细胞。
我们知道干细胞能分泌大量具有修复作用的营养因子和信号分子,研究者把它们浓缩成了精华。
研究者认为这种开创性的方法能够将治疗因子靶向递送至卵巢,促进组织修复与再生。
但研究者很快意识到,干细胞起作用的机制可能比想象中更复杂,移植的干细胞大多不会长期驻留,更少分化为卵巢细胞,尤其是静脉注射使用,利用度更少。
那么如何让干细胞更好地起效呢?研究者认为干细胞主要通过旁分泌作用,即分泌一系列生物活性因子,来调节局部微环境,促进内源性修复。
在这些分泌因子中,一类被称为细胞外囊泡的微小结构,引起了研究者的关注。
04细胞外囊泡,生物快递系统细胞外囊泡,这个名字你可能比较陌生,这是所有细胞都是会释放的纳米级膜泡,直径在30-150纳米之间,大约是头发丝直径的千分之一。
它们不是简单的细胞碎片,而是具有复杂结构和功能的细胞间通讯的工具。
想象一下,每个细胞都是一个信息中心,不断产生和接收信号,当它需要向远处或临近细胞发送复杂信息时,不会至发送单个信号分子,那样容易降解、容易被误解。
它会将一整套信息报打包进微小的膜泡中,这个信息包可能包含蛋白质、脂质、RNA等多种分子,这些物质共同传达一个完整的生物指令。
这些天然存在的生物快递车具有多重优势。
它们体积小,能够穿过生物屏障;
表面带有识别标记,可以靶向特定细胞,就像我们日常见过的闪送,点对点直接送达;
它们的脂质双层膜保护内容物不被降解;
而且由于它们来自人体自身细胞,免疫原性低,安全性高。
然而,天然的细胞外囊泡虽然有上面的那些作用,但还是有局限性,它们是有什么送什么,无法根据疾病需求进行定制。
而且,不同批次、不同来源的细胞外囊泡,其成分和疗效可能差异很大,这就导致了姐妹们观察到的那个现象:
干细胞治疗在不同患者身上效果不同,即便有效但效果可能也不可靠。
05经过改造的细胞外囊泡北京医院王少为团队的创新之处在于,他们不满足于使用干细胞的天然细胞外囊泡,而是决定对其进行改造,制作一款增强版的定制化治疗工具。
他们的设计思路清晰而巧妙,首先确定对卵巢修复最关键的有效成分,然后让干细胞生产富含这种成分的囊泡。
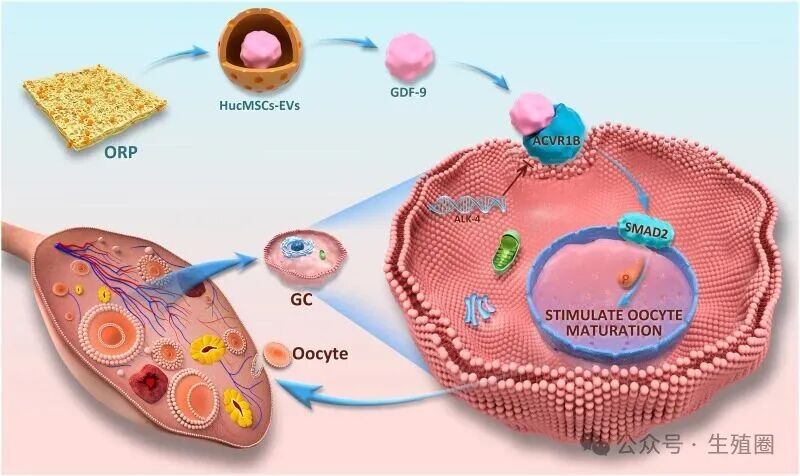
那么哪种成分对卵巢来说最关键呢?研究团队选择了生长分化因子-9(GDF-9)作为他们的明星分子。
这个选择基于坚实的科学依据,GDF-9是转化生长因子-β超家族成员,主要由生长中的卵母细胞产生,对卵泡发育的早期阶段至关重要。
它促进颗粒细胞增殖,抑制其过早黄素化,刺激卵丘细胞扩张,是卵泡正常发育的主调控因子。
然而,GDF-9直接作为药物使用面临挑战,它在体内半衰期短,容易被降解,缺乏靶向性,可能影响非目标组织,单独作用可能不足以激活完整的修复程序。
这就需要一种能够保护它、递送它、并增强其效果的生物快递系统。
细胞外囊泡可以完美承担这项工作。
研究团队从人类脐带中提取间充质干细胞,这是一种来源相对丰富、伦理争议小、免疫原性低的干细胞类型。
然后他们通过基因工程技术,将GDF-9的基因递送到这些干细胞,使它们过表达GDF-9蛋白。
接下来是精密的分离和纯化过程,干细胞培养上清中含有各种成分,需要从中分理处细胞外囊泡。
研究团队采用超速离心结合超滤的方法,将细胞外囊泡沉淀下来,最后通过超滤进行浓缩和纯化。
这种工程化改造的、富含GDF-9的细胞外囊泡,被研究团队命名为GOEs。
 06细胞试验检验效果
06细胞试验检验效果在进入动物研究之前,研究团队首先在细胞水平上验证了GOEs的效果,他们使用人卵巢颗粒细胞作为试验对象,用化疗药物顺铂处理这些细胞,模拟卵巢功能衰退状态。
试验设置了四个组,健康对照组、顺铂损伤组、天然细胞外囊泡治疗组(不特意搭载GDF-9分子)、GOEs治疗组。
结果令人鼓舞,GOEs治疗显著提高了受损细胞的存活率,减少了细胞凋亡,效果优于天然细胞外囊泡。
研究者还观察到了一个有意思的现象,当过表达GDF-9的干细胞与受损颗粒细胞共同培养但不直接接触时,修复效果有限。
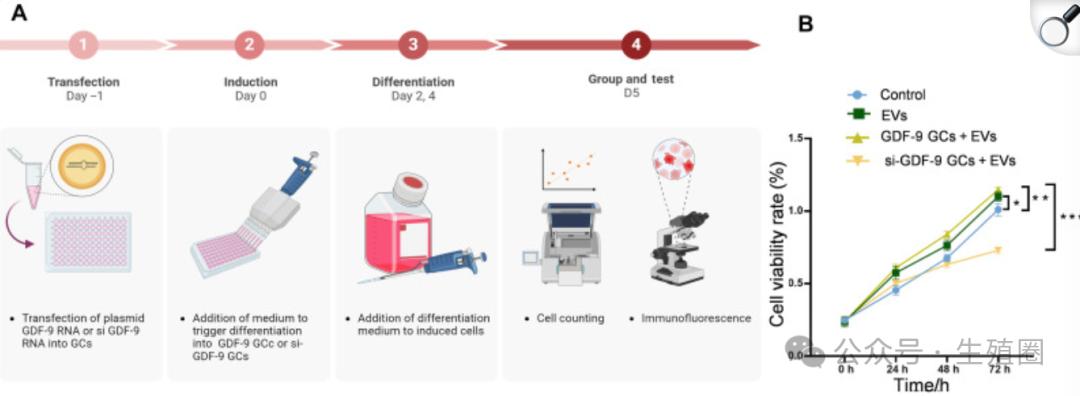
这表明GOEs的疗效主要来自囊泡内携带的GDF-9,而不是干细胞分泌的其他可溶因子。
07真实动物研究结果如何?细胞试验的结果令人鼓舞,但细胞培养环境简化了体内的复杂性,要真正评估GOEs的治疗潜力,需要在动物模型中进行验证。
研究团队建立了化疗诱导的卵巢功能障碍大鼠模型,这很好地模拟了卵巢早衰患者的情况。
他们将大鼠分为四组:健康对照组、模型组、天然细胞外囊泡治疗组、GOEs治疗组。
研究者将普通细胞外囊泡和GOEs细胞外囊泡通过尾静脉或腹腔注射注入卵巢功能障碍大鼠体内。
活体成像显示,注射后这些细胞外囊泡会富集到双侧卵巢,并在48小时内被代谢清除,显微镜下可见它们被卵泡内的颗粒细胞摄取。
效果如何呢?我们来看具体情况。
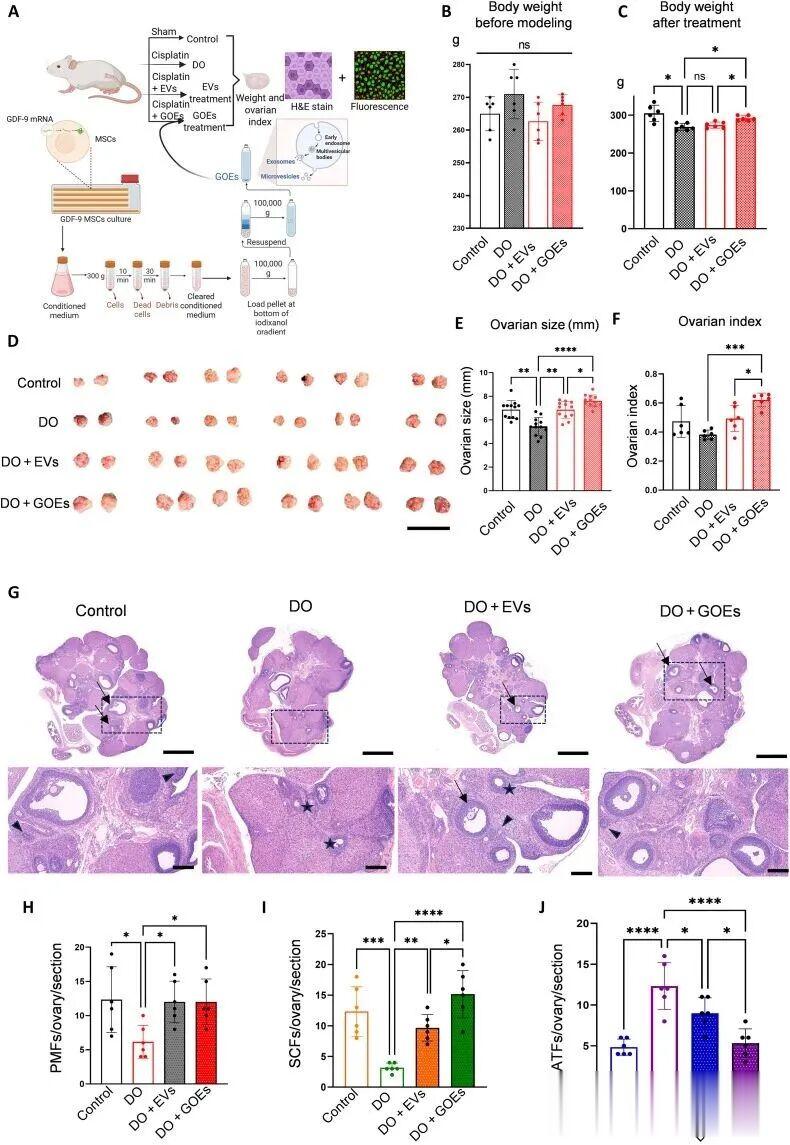
与没有治疗的模型组比较,接受GOEs治疗的大鼠体重、卵巢大小和重量恢复;发情周期变得规律;生殖激素水平(雌激素、AMH、FSH)水平恢复正常。
从大家最关注的生育能力来说,模型组怀孕率为0,而GOEs组怀孕率提升至26.7%;
从每窝产仔数来看,GOEs组一窝平均能生下17只健康幼崽,而普通干细胞组一窝平均能生下7只幼崽。
GOEs组数量显著更多,而且幼崽存活率和健康状况良好。
研究者在显微镜下观察卵巢组织结构发现,治疗组健康的原始卵泡、生长卵泡数量显著增加,而病态的闭锁卵泡减少,这直接证明治疗促进了卵泡的发育和存活。
 08GOEs为什么效果这么好?
08GOEs为什么效果这么好?研究不仅要做到知其然,更要做到知其所以然。GOEs如何起作用的呢?研究团队追踪了从细胞外信号到细胞内响应的完整链条。
通过基因测序技术,研究者比较了正常卵巢和功能障碍卵巢的基因表达差异,发现GDF-9及其受体ACVR1B的表达在功能障碍卵巢中显著下调。
这提示,GDF-9-ACVR1B信号轴可能是关键的治疗靶点。
当GOEs将GDF-9递送到颗粒细胞后,GDF-9与细胞膜上的ACVR1B受体结合,这种结合激活了受体自身的激酶活性,导致细胞内SMAD2蛋白的磷酸化。
磷酸化的SMAD2与SMAD4形成复合物,转运到细胞核内,作为转录因子调节特定基因的表达,最终促进细胞增殖、抑制凋亡、支持卵泡发育。
研究团队还进行了反向验证,当使用抑制剂阻断ACVR1B受体,或敲低SMAD2表达时,GOEs的治疗效果显著减弱,这种正反验证使结论更可靠。
值得注意的是,研究中发现了一个有趣的现象,尽管GOEs在功能上优于天然干细胞产生的细胞囊泡,但两者在提升ACVR1B受体表达方面没有统计学差异。
研究者分析,这可能是因为干细胞分泌的天然细胞囊泡本身就含有一定量的GDF-9,已能部分激活该通路。
09从实验室到临床的漫长之路这项研究为卵巢功能减退的治疗开辟了新的方向,这也是一条优化干细胞治疗的新思路,但从实验室成果到临床还有很长的路要走。
下一步可能涉及到工艺的优化,比如开发更高效、稳定、低成本的细胞外囊泡生产纯化工艺;
比如进一步改造囊泡膜,增强其靶向性、穿膜能力和内容物控释能力;
比如探索GDF-9与其他生长因子(比如BMP-15、AMH等)的联合使用;
比如疾病谱的拓展,不仅针对医源性卵巢损伤,也研究对多囊卵巢综合征、特发性早衰等的疗效;
比如机制继续深化,更全面解析GOEs调控卵巢功能的全网络机制,寻找生物标志物。
总之,这项技术的意义可能超出卵巢疾病治疗本身,它代表了一种全新的药物递达和治疗理念,利用人体自身的生物递送系统,进行工程化改造,实现精准、高效、低毒的治疗。
这种策略可应用于多种难治性疾病,比如神经退行性疾病、心肌损伤、肝纤维化、骨关节炎等。
回到我们最初的问题,为什么干细胞效果不稳定?如何能更有效地修复卵巢?这项研究给出了一个清晰的科学应答——
绕过细胞定居的难题,直接递送浓缩的修复指令,是实现质效突破的关键。
从移植干细胞到递送囊泡,这不仅是技术的升级,更是治疗逻辑的进化,26.7%的怀孕率,是这条路上第一个坚实的里程碑。
诶来,随着生物囊泡技术的不断优化,我们有理由期待,更多人的生育希望将不再被年龄或机能衰退轻易定义。
科学的意义,正是将不可能,一步步变为可能,加油吧!
全文完!现在流量为王的年代,围观也是一份力量,转发就是一份担当,希望动动您发财的小手,给我点个赞,如果您能转发到微信群或朋友圈,就会让更多孕育困难的小家庭受益,谢谢您!
郑重声明
本账号发表的内容仅作为科普分享,不对所引用文献的准确性和完整性作出任何承诺和保证,亦不承担因该内容已过时、所引用资料可能的不准确或不完整等情况引起的任何责任,请相关各方在采用或者以此作为决策依据时另行核查。本账号不做任何形式的营销推广,在采取任何预防或治疗措施前,请与你的医疗保健提供者沟通。
不传小道消息和谣言
不做只为转发量而存在的公众号
永远在意真实数据和文献论证
抱娃路上,我愿意陪你一起走过最无助的岁月
——THE END——
参考文献
Repair of female reproductive function by GDF-9-overexpressing extracellular vesicles via ACVR1B/SMAD2 regulation in ovarian granulosa. Sci Adv. 2025 Dec 12;11(50):eadw9006. doi: 10.1126/sciadv.adw9006. Epub 2025 Dec 10.