导读:代谢功能障碍相关性脂肪肝(MASLD)是全球最常见的慢性肝病,影响着全球三分之一的人口。大多数患者表现为单纯性脂肪变性,而高达 20%的患者会发展为代谢功能障碍相关性脂肪性肝炎(MASH),最终可能发展为肝硬化和肝细胞癌。多种平行机制共同促成 MASH 的发生,这些机制受到肝脏脂毒性、肠道菌群失调以及影响先天性和适应性免疫反应的促炎饮食的刺激。
⭐首发于超能文献(Suppr.ai):中文搜文献|用文献做科普
拿到体检报告,看到“轻度脂肪肝”或“中度脂肪肝”这几个字时,你是不是觉得“大家都这样”,根本没放在心上?
确实,代谢功能障碍相关脂肪性肝病(MASLD,即我们常说的脂肪肝)已经成为全球最常见的慢性肝病,影响着全球三分之一的人口。
2026年3月发表于《Cell Metabolism》(影响因子30.9)的《The many pathways driving liver inflammation in MASH》的研究揭示了一个令人担忧的真相:其中20%的最终发展为代谢功能障碍相关性脂肪性肝炎(MASH),最终可能发展为肝硬化和肝细胞癌。

图1:2026年3月发表于《Cell Metabolism》(影响因子30.9)的文章,揭示多种平行机制共同促成代谢功能障碍相关性脂肪型肝炎,PubMed截图
尽管有高达80%的患者仅仅是单纯的肝脏脂肪堆积,但仍有高达20%的患者会发展为代谢功能障碍相关脂肪性肝炎(MASH)。多出来的这个“炎”字,意味着肝脏开始发炎、受损,如果任由其发展,甚至可能走向肝纤维化、肝硬化,乃至肝癌。

图2:代谢功能障碍相关性脂肪肝(MASLD) vs 代谢功能障碍相关性脂肪性肝炎(MASH),结合2023年指南,由豆包生成
那么,究竟是什么打破了单纯的脂肪堆积,引发了肝脏乃至全身的炎症?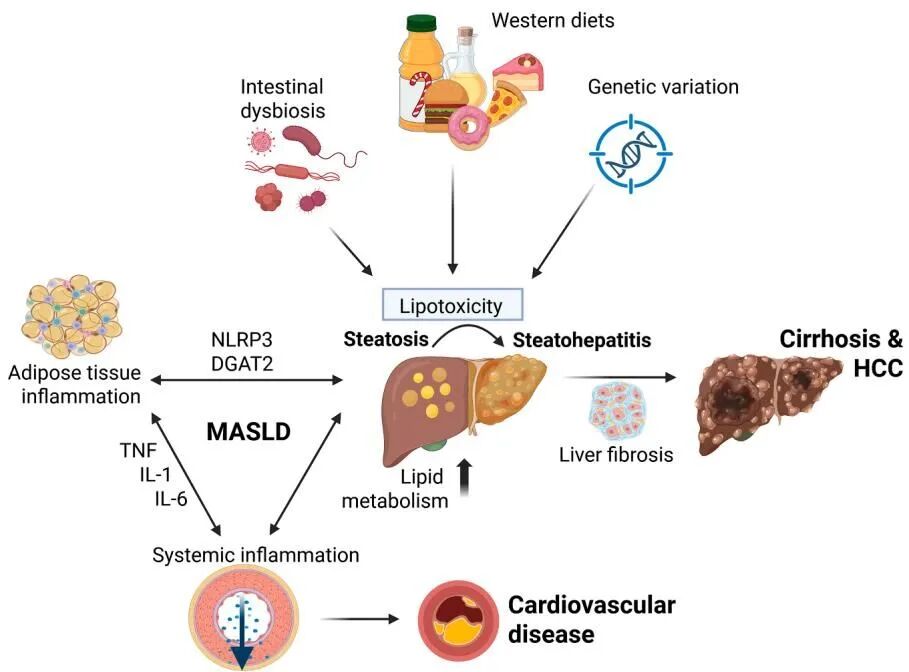
图3:脂肪肝走向MASH的多因素的过程,来源于《The many pathways driving liver inflammation in MASH》
如图3所示,脂肪肝及其并发症的发生是一个多因素交织的复杂过程:
从图中我们可以清晰地看到,西方饮食习惯(高油高糖)、肠道菌群失调以及遗传基因的变异,共同构成了代谢压力的源头。这些压力最终在肝脏汇聚,引发了“脂毒性”,导致单纯的脂肪肝(Steatosis)恶化为脂肪性肝炎(Steatohepatitis)。
这种持续的炎症不仅会在肝脏内部引发肝纤维化,最终导致肝硬化和肝细胞癌(HCC),还会引发脂肪组织乃至全身的炎症反应,进而导致冠心病等严重的心血管疾病。
可以说,控制肝脏炎症,就是切断这条危险链条的关键。
1. 脂毒性:堆积的脂质如何直接引发肝脏发炎?
长期以来,我们可能以为肝脏里的脂肪只是单纯的能量储备。但实际上,当脂肪积累到一定程度时,它们会表现出极强的“脂毒性”。久坐不动的生活方式加上过量摄入饱和脂肪酸、葡萄糖和果糖,为肝脏大量制造脂肪提供了充足的原料。在这个过程中,有几种特殊的脂质成为暴引发肝脏炎症的核心因素。
1.1 甘油三酯:不仅是指标异常,更是病情恶化的推手
甘油三酯是肝脏内最主要的脂质类型。过去,科学家们曾认为它只是被动堆积的产物,不会直接引起肝脏发炎。但近期的研究推翻了这一认知。当我们摄入过多游离脂肪酸时,它们会在肝脏内合成甘油三酯。研究发现,如果在动物模型或临床试验中,使用特定药物抑制甘油三酯的合成(例如抑制一种名为DGAT2的限速酶),不仅能显著降低肝脏内的脂肪酸含量,还能改善肝脏的炎症和氧化应激反应。这就证明,甘油三酯的异常积累本身就是驱动脂肪肝恶化的重要因素。
1.2 游离胆固醇:除了堵塞血管,还会直接毒害肝细胞
我们都知道血液中胆固醇过高(尤其是低密度脂蛋白胆固醇LDL)是心血管疾病的重大风险因素,它会引起血管发炎。但在肝脏里,多余的胆固醇同样具有破坏力。
研究发现,当肝细胞的线粒体(细胞的能量工厂)中积累了过多的游离胆固醇时,会耗尽细胞内的抗氧化物质,使肝脏对炎症和细胞死亡的信号变得极其敏感。更有趣的是,将长期喂食高胆固醇饮食的小鼠的肠道粪便移植给无菌小鼠后,这些原本健康的小鼠也出现了肝脏脂肪变性和炎症。
目前广泛使用的降胆固醇药物(他汀类药物),在临床上已被观察到能够降低肝脏内的脂质、减轻炎症和纤维化。虽然还需要更大规模的临床试验来最终确认,但降胆固醇治疗很可能是脂肪肝患者保护心血管与肝脏的双重策略。
1.3 游离脂肪酸与神经酰胺:直接激活细胞内的炎症通路
日常饮食中摄入的脂肪,以及在我们身体出现胰岛素抵抗时(即身体对胰岛素不敏感,这在脂肪肝患者中极其常见)由全身皮下脂肪释放到血液中的脂肪酸,被称为游离脂肪酸。其中,像油酸、亚油酸和棕榈酸这样的游离脂肪酸,能够直接激活细胞内的多种炎症通路。
它们能够激活一种名为NLRP3的炎症小体。这个炎症复合体一旦被激活,就会释放出大量的促炎因子(如白细胞介素-1β),导致代谢性炎症的全面暴发。此外,脂质代谢过程中产生的一种名为“神经酰胺”的物质,也被证实是具有高度脂毒性的脂质。在脂肪肝患者体内,神经酰胺的浓度显著升高,并且与肝脏的胰岛素抵抗程度直接相关。
可见,过剩的脂质并不是简单地处于静止状态,它们以各种微观的形式潜入肝脏细胞,释放毒性,引发强烈的炎症反应。
但肝脏发炎,仅仅是因为脂质过多吗?科学家们把目光投向了另一个重要的生理系统——我们的肠道。
2. 肠道菌群失调:肚子里的细菌如何让肝脏“遭殃”?
肠道不仅仅是消化器官,它的黏膜还是阻挡有害物质进入血液的重要屏障。研究发现,脂肪肝患者的肠道屏障往往受损(即通透性增加,俗称“肠漏”),且受损程度与肝脏脂肪变性的严重程度密切相关。
我们的肠道里居住着数以万亿计的微生物。在健康的身体里,它们安分守己,甚至帮助我们维持肠道屏障的完整。但在脂肪肝患者体内,肠道菌群的平衡被打破了。这种“菌群失调”会导致肠道里的有害物质(比如某些致病菌产生的内毒素)穿过受损的肠道屏障,顺着静脉血液直接流入肝脏。
不仅如此,有些肠道细菌甚至能在我们的肚子里直接产生酒精。研究人员在脂肪肝患者的粪便中发现了大量能产生酒精的细菌(如肺炎克雷伯菌),这导致患者血液和进入肝脏的血管中的酒精浓度异常偏高。无论是渗漏进来的内毒素,还是细菌产生的酒精,都是极强的致炎物质。它们源源不断地刺激肝脏,让肝脏始终处于发炎的警戒状态。
3. 饮食的另一面:高脂与高果糖是肝脏发炎的直接诱因
我们每天吃进去的食物,深刻地影响着肝脏的命运。高脂、高糖的西式饮食不仅是导致全球脂肪肝大流行的罪魁祸首,更是直接引发机体发炎的危险因素。
科学实验表明,仅仅连续一个月的高脂饮食,就能在健康志愿者体内引发轻度的内毒素血症和免疫系统的异常激活。高脂饮食会破坏肠道屏障,让更多致炎物质进入血液。
此外,现代饮食中无处不在的“果糖”也是一大隐患。与普通的葡萄糖不同,果糖在体内的代谢会绕过正常的胰岛素调节机制,直接进入肝脏大量合成脂肪。过量摄入果糖不仅加剧了肝脏的“脂毒性”,还会促使肠道内产生更多有害的促炎细菌群(如大肠杆菌等)。毫无节制地喝含糖饮料、吃高脂加工食品,实质上是在给肝脏不断施加代谢压力。
4. 免疫系统警报全开:从局部发炎到全身受累
无论是肝脏内部堆积的毒性脂质,还是从肠道漏进来的细菌产物,最终都会触发我们身体的防御机制——免疫系统。
首先出动的是“先天免疫系统”。肝脏内驻扎着大量负责吞噬病原体的巨噬细胞。当它们感知到脂质过载和细菌毒素后,会迅速释放出大量的促炎因子(如肿瘤坏死因子TNF、白细胞介素-1β等)。这些促炎因子不仅在肝脏局部搞破坏,还会随着血液流向全身,导致血液中的C反应蛋白(CRP)或铁蛋白水平显著升高,引发全身性的低度炎症。
随着病情的发展,“后天免疫系统”(主要是T细胞)也会加入战局。科学家发现,在脂肪肝向肝炎恶化的过程中,肝脏内会聚集大量原本用来杀灭受感染细胞的T细胞。但在代谢紊乱的状态下,它们开始表现出异常的攻击性,进一步加剧肝脏的组织损伤和纤维化进程。
5. 基因的底牌:为什么有些人的脂肪肝更容易恶化?
面对同样的高脂高糖饮食和脂肪堆积,为什么有的人只是一直处于单纯的脂肪肝阶段,而有的人却迅速恶化为肝炎甚至肝硬化?答案可能藏在我们的基因里。
如图4所示,宿主的基因变异深刻影响着肝细胞内的脂质代谢和免疫反应。以人群中最常见的一个名为PNPLA3的基因突变(I148M)为例,这种突变产生的异常蛋白质会像顽固的塞子一样附着在脂肪滴表面,阻碍脂肪的正常分解,导致脂肪和胆固醇在肝脏内大量囤积。
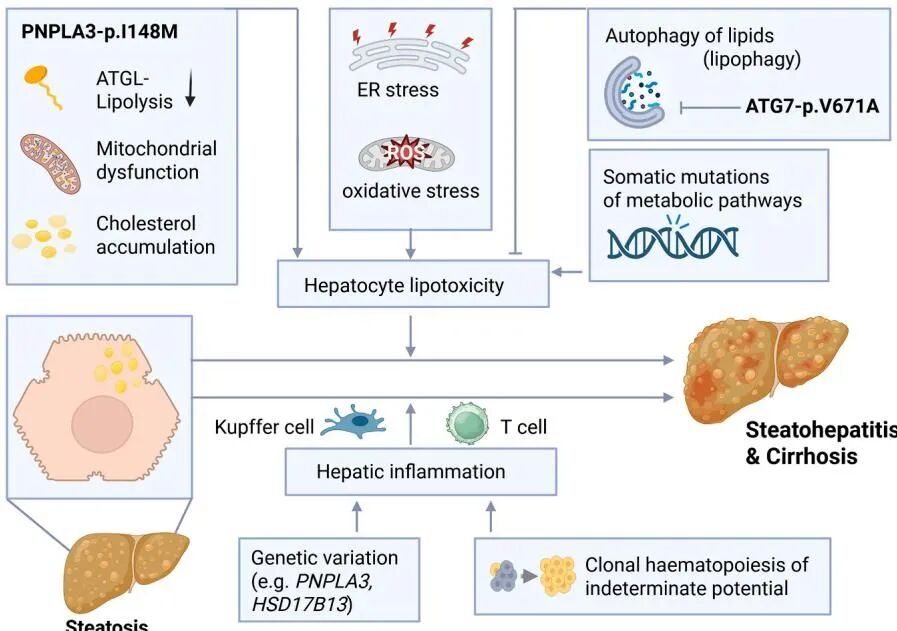
图4:基因表达于脂质代谢障碍,来源于《The many pathways driving liver inflammation in MASH》
从图4中我们可以清晰地看到这一恶化路径:基因缺陷引起的脂质代谢障碍,会直接导致肝细胞内的内质网应激和线粒体功能受损,产生大量的氧化应激(ROS)。为了应对这种恶劣的细胞内环境,部分肝细胞甚至被迫发生体细胞突变(Somatic mutations)以求自保。与此同时,脂毒性发出的求救信号唤醒了肝脏内的巨噬细胞(Kupffer细胞)和T细胞。在基因变异、代谢压力和脂毒性的多重夹击下,原本旨在清除代谢废物的免疫反应,最终演变成了持续的肝脏炎症(Hepatic inflammation),一步步将原本单纯的脂肪肝(Steatosis)推向脂肪性肝炎(Steatohepatitis)乃至肝硬化(Cirrhosis)的深渊。
6. 脂肪组织与全身联动:肝脏发炎不仅仅是肝脏的事
我们往往认为长胖只是皮下多了一层肉,但在肥胖和脂肪肝患者体内,脂肪组织(尤其是腹部的内脏脂肪)其实已经变成了一个巨大的、持续向全身释放毒素的“发炎工厂”。
科学研究证实,脂肪组织中含有大量的免疫细胞。当脂肪囤积过多时,这些脂肪组织本身就会发生强烈的炎症反应,并向血液中持续释放大量的炎症因子。人体血液中高达35%的白细胞介素-6(一种关键的促炎分子)都可能来源于全身发炎的脂肪组织。这些炎症信号会顺着血液循环“火上浇油”,直接加重肝脏的胰岛素抵抗和炎症反应。这也解释了为什么减肥手术或积极减重对脂肪肝有着立竿见影的抗炎效果——因为减脂实质上是极大地消除了全身炎症的源头。
7. 致命的连锁反应:心血管疾病与肝外癌症风险激增
当肝脏和脂肪组织持续处于这种“低度发炎”状态时,整个身体的免疫系统都在超负荷运转。这就解释了文章开头提到的现象:为什么脂肪肝患者最常见的死因不是肝病,而是心血管疾病。
血液中长期存在的炎症因子(如高敏C反应蛋白)会持续破坏血管内皮,这与动脉粥样硬化、心肌梗死和中风等严重心血管事件的发生密切相关。此外,这种长期的慢性全身性炎症,还为癌细胞的生长提供了温床。
数据表明,排除肥胖因素后,脂肪肝患者罹患胃肠道癌、乳腺癌和妇科癌症等“肝外癌症”的风险足足翻了一倍。可以说,脂肪肝实际上是一个波及全身的“发炎综合征”。
8. 破局之道:既调代谢又抗炎的新型治疗药物
既然脂肪肝是一个涉及全身代谢与炎症的复杂网络,那么未来的治疗方案就不能只局限于保肝。目前,多种处于临床试验后期或刚刚获批的新型药物,展现出了令人振奋的“一石多鸟”效应——它们在修复代谢紊乱的同时,还具备强大的抗炎作用。
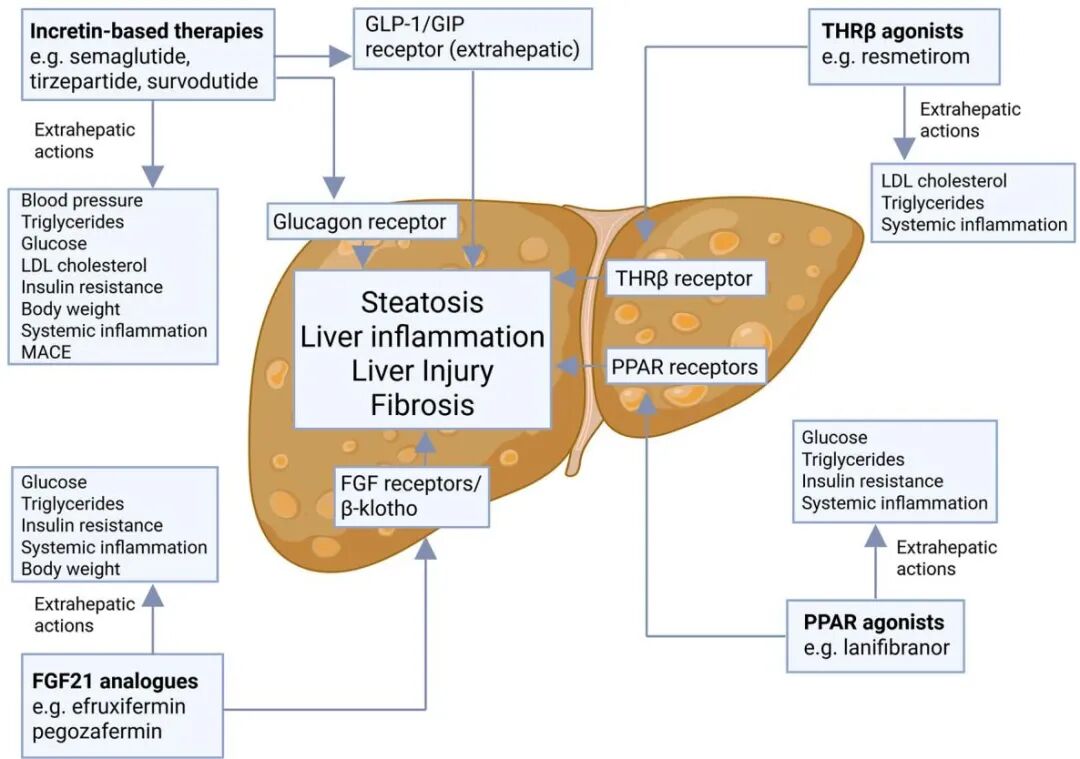
图5:来源于《The many pathways driving liver inflammation in MASH》
如图5所示,近年来涌现的多种新兴药物不仅能直接靶向肝脏,还在全身代谢中发挥着多重功效。从图中我们可以看到,像Resmetirom(甲状腺激素受体β激动剂,近期已获批用于MASH)和FGF-21类似物,它们能够精准结合并激活肝脏内部的特异性受体,直接改善肝细胞的脂质代谢,从而有效逆转肝脏脂肪变性、减轻肝脏炎症(Liver inflammation)甚至改善肝纤维化。而另一大类备受瞩目的药物——肠促胰岛素类药物(如大热的降糖减重药司美格鲁肽、Tirzepatide等GLP-1受体激动剂),虽然在肝脏中并没有直接的靶点受体,但它们通过在肝外组织(Extrahepatic)发挥强大的减重、降糖降脂和改善胰岛素抵抗的作用,间接地为肝脏“减负”,极大地减轻了全身炎症,最终甚至能带来降低重大心血管不良事件(MACE)的额外临床获益。
9. 结语
科学界对脂肪肝的认知已经发生了翻天覆地的变化。它不再只是体检报告上一个提示“少吃多动”的简单结论,而是一个由脂毒性、肠道菌群失调、不健康饮食和遗传易感性共同驱动的复杂全身性疾病。
尽管目前仍有许多未解之谜——比如究竟如何精准预测那20%会恶化为肝炎的高危人群?但未来,随着多组学和基因检测技术的发展,我们有望对脂肪肝患者进行更精细的分类,并利用能够同时纠正代谢与炎症的新型药物进行精准打击。在这些前沿医学彻底改变临床现状之前,管住嘴、迈开腿,减少摄入高脂高糖的“促炎饮食”,依然是我们每个人阻断这场全身性炎症风暴最有效的生活方式投资。
论文信息标题:The many pathways driving liver inflammation in MASH.
论文链接:https://doi.org/10.1016/j.cmet.2026.02.018
发表时间:2026-3-23
期刊/会议:Cell metabolism
作者:Herbert Tilg, Timon E Adolph, Stefano Romeo, Rohit Loomba