1型糖尿病(T1D)与其他糖尿病不同,它不是代谢问题主导,而是免疫系统“认错了人”——自身免疫细胞错误地攻击胰岛β细胞,导致胰岛素分泌几乎枯竭。患者终身依赖外源性胰岛素,但这只是补充激素,无法纠正免疫紊乱,更阻止不了β细胞的持续损伤。

近年来,肠道微生态研究为1型糖尿病带来了全新视角。肠道是人体最大的免疫器官,菌群的平衡直接决定免疫系统的稳态。而“肠道菌群–胆汁酸–免疫”三角的失衡,正是1型糖尿病发病的核心机制。
19岁的小雯(化名),确诊1型糖尿病已经7年。每天注射38单位胰岛素,糖化血红蛋白(HbA1c)仍然高达8.5%。更折磨人的是频繁的低血糖发作,让她时刻提心吊胆,无法正常上学和生活。
免疫指标检测显示,她的调节性T细胞(Treg)比例偏低,而Th17促炎细胞过度活化——免疫系统处于严重的失衡状态。
2025年2月,小雯接受了肠菌移植(FMT)治疗。供体是一名26岁健康女性,无自身免疫病家族史。按照标准方案,她接受了3次移植,每次间隔4周。
变化在3个月后开始显现:C肽水平从低于0.1ng/mL升至0.18ng/mL,胰岛素用量降至24单位/天(减少35%),HbA1c降至6.8%,低血糖发生率减少70%。
6个月时,更根本的改变发生了:调节性T细胞比例提升了2.3倍,Th17细胞比例下降了45%。免疫耐受被重新建立,血糖控制趋于平稳,她的生活质量大幅提升。
其实,小雯的案例不是孤例。它揭示了一个核心机制:1型糖尿病不是单纯的胰岛局部病变,而是“肠–胆汁酸–免疫轴”的系统性紊乱。
第一步:菌群失衡。
1型糖尿病患者肠道中,双歧杆菌、乳酸菌等有益菌显著减少,而肠球菌、葡萄球菌等促炎菌异常富集。菌群多样性大幅下降。
第二步:胆汁酸代谢异常。
菌群失衡直接影响胆汁酸转化。初级胆汁酸无法有效转化为次级胆汁酸(如LCA、DCA),导致次级胆汁酸水平显著降低。
第三步:免疫崩塌。
次级胆汁酸是调节免疫稳态的关键信号分子。它们的缺乏,导致调节性T细胞(Treg)分化不足,而Th1、Th17等促炎细胞过度活化。自身免疫细胞开始错误攻击胰岛β细胞。
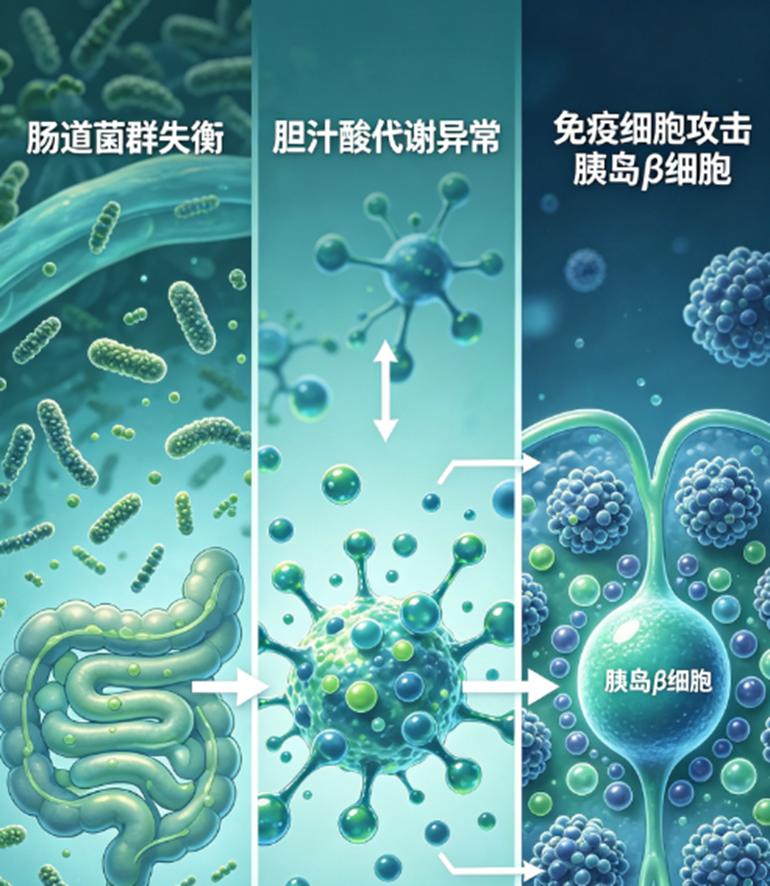
这就形成了一个恶性循环:菌群失衡→胆汁酸异常→免疫紊乱→β细胞损伤。
肠菌移植的逻辑不是压制免疫,而是重建平衡。
健康供体的肠道菌群进入患者体内后,会逐步定植并占据生态位。有益菌(如双歧杆菌、乳酸菌)重新富集,促炎菌被抑制。菌群多样性恢复后,胆汁酸代谢通路随之修复:次级胆汁酸水平回升。
次级胆汁酸回升后,调节性T细胞的分化得到支持。Treg比例上升,Th17比例下降,免疫耐受重新建立。免疫系统不再疯狂攻击胰岛β细胞,残余的β细胞得以保存,部分休眠的β细胞甚至被激活,重新分泌胰岛素。
最终呈现出来的临床效果就是:C肽水平提升,胰岛素用量减少,血糖波动缩小,低血糖风险下降,远期并发症风险也随之降低。
传统治疗把1型糖尿病看作胰岛局部的“胰岛素缺乏”,解决方案是终身注射外源胰岛素。这当然能救命,但它没有解决“谁在破坏胰岛”这个根本问题。
肠菌移植的逻辑完全不同。它不是补充缺失的激素,而是修复引发免疫紊乱的上游病因——肠道菌群失衡。通过重建“肠–胆汁酸–免疫轴”,让免疫系统重新学会识别“自己人”,停止对β细胞的攻击。

小雯在接受移植6个月后,调节性T细胞比例提升了2.3倍。这不是药物的临时效果,而是免疫系统本身发生了可测量的、持久的改变。
当然,肠菌移植不是“一次治疗就告别胰岛素”。对于已经失去绝大部分β细胞的长期患者,完全脱离胰岛素仍不现实。但“减胰岛素、稳血糖、防并发症”这三个目标,已经足以让无数患者的生活质量发生质变。
更重要的是,这项治疗颠覆了1型糖尿病的治疗逻辑——从“终身替代”到“免疫修复”。这个转向,为患者提供了一条真正从上游干预的路径,也为其他自身免疫性疾病的治疗提供了宝贵的借鉴。
1型糖尿病不是终身判决。那些被错误攻击的β细胞,有些只是被“围困”而非消失。而唤醒它们的关键,也许就藏在我们的肠道里。