免疫治疗已在越来越多的恶性肿瘤中改善了患者生存期,但在胰腺导管腺癌(PDAC)患者中诱导有效的抗肿瘤T细胞免疫应答仍极为困难。
PDAC对免疫治疗产生耐药性的原因是多方面的,包括靶抗原表达水平低下,以及免疫抑制分子的频繁产生或上调,进而形成“冷”肿瘤微环境(TME)。即便存在可靶向的抗原,其异质性表达也会导致肿瘤快速适应及靶抗原调变,从而削弱T细胞单药治疗的抗肿瘤效果。
2026年1月,来自美国得克萨斯儿童医院和休斯顿卫理公会医院的研究者在《Nature Medicine》杂志上发表了题为《Autologous multiantigen-targeted T cell therapy for pancreatic cancer: a phase 1/2 trial》的文章,报告了TACTOPS试验的结果,这项三臂、非随机、1/2期临床试验(编号NCT03192462)在PDAC患者中评估了一种体外扩增、多克隆、Th1细胞极化的T细胞制剂。
这种T细胞制剂可靶向5种肿瘤相关抗原:PRAME、SSX2、MAGEA4、Survivin和NY-ESO-1。这些抗原的选择基于的是其肿瘤特异性、致癌性、免疫原性及表达水平。
研究设计
试验中对晚期PDAC患者给予该自体非基因编辑T细胞制剂(每次输注剂量为1×10⁷个细胞/m²,每月1次):
A组:一线化疗有效者(n=13) B组:一线化疗难治者(n=12) C组:可切除病灶者(n=12)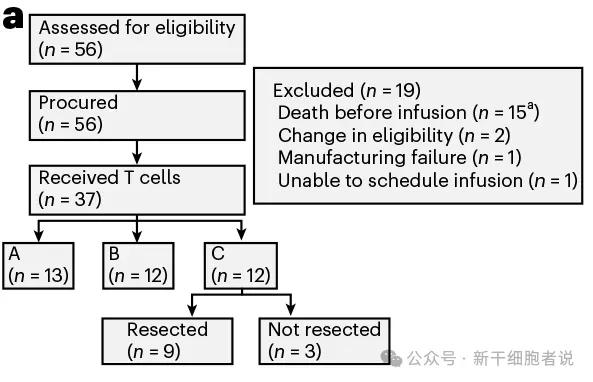
CONSORT流程图展示了三个研究组中入组与接受治疗的患者情况
主要研究终点为安全性及完成6次输注的可行性。探索性疗效终点包括:输注后T细胞的体内持续性、临床获益与输注效应T细胞扩增的相关性,以及新生免疫应答的诱导情况。
结果分析
在招募的56名受试者中,37人接受了细胞输注,仅发生1例与治疗相关的严重不良事件。
A组疾病控制率为84.6%(95%置信区间:54.6%–98.1%) B组疾病控制率为25%(95%置信区间:5.5%–57.2%) C组中,9例接受手术切除的受试者中有2例在随访66个月后仍保持无病状态。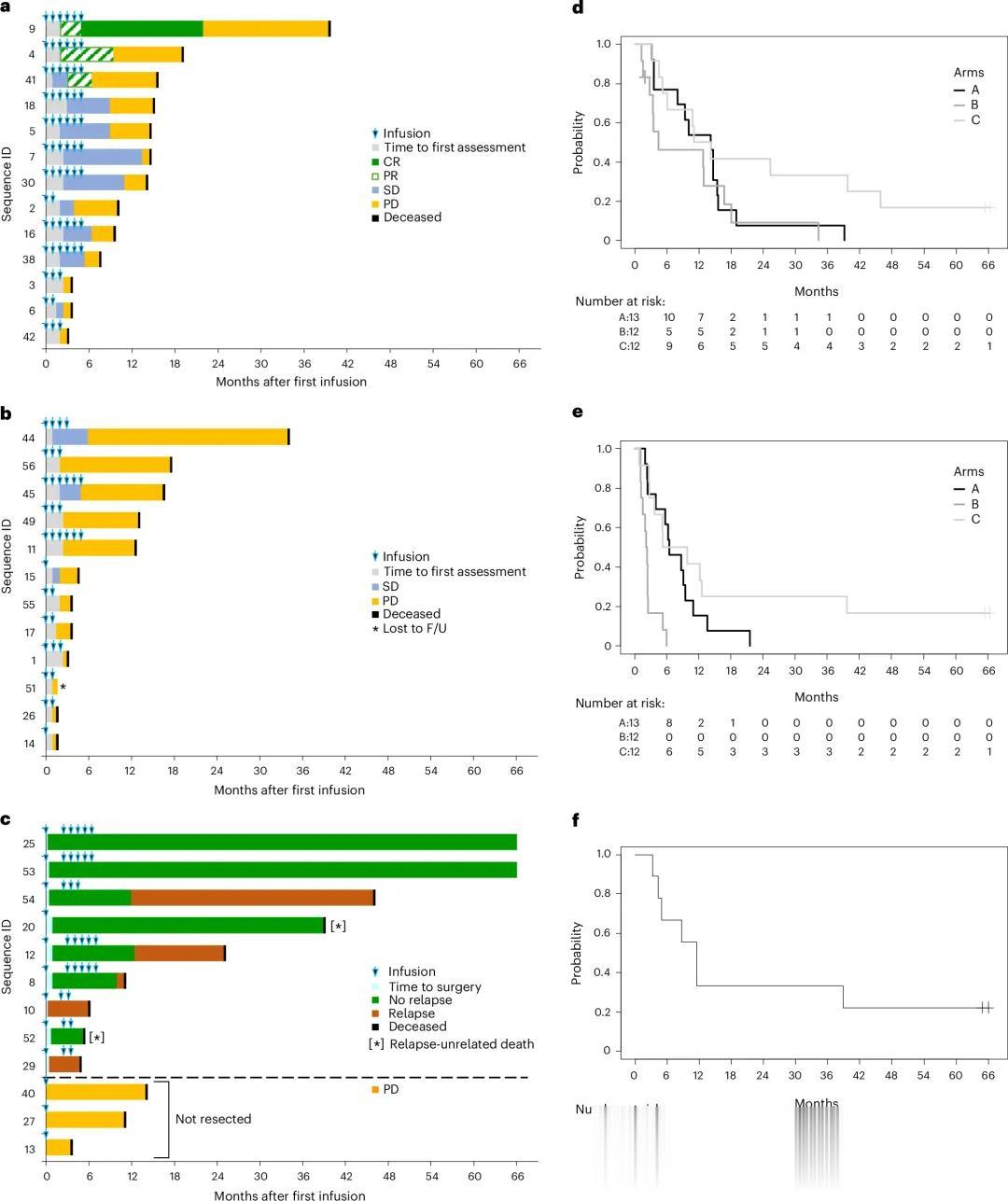
临床结果
输注的细胞在治疗后可持续存在长达12个月。与无应答者相比,应答者在给药期间(P=0.027)及随访期间可检测到肿瘤靶向T细胞水平升高。临床结局与功能性肿瘤相关抗原靶向T细胞克隆的外周扩增及治疗诱导的抗原扩散相关。
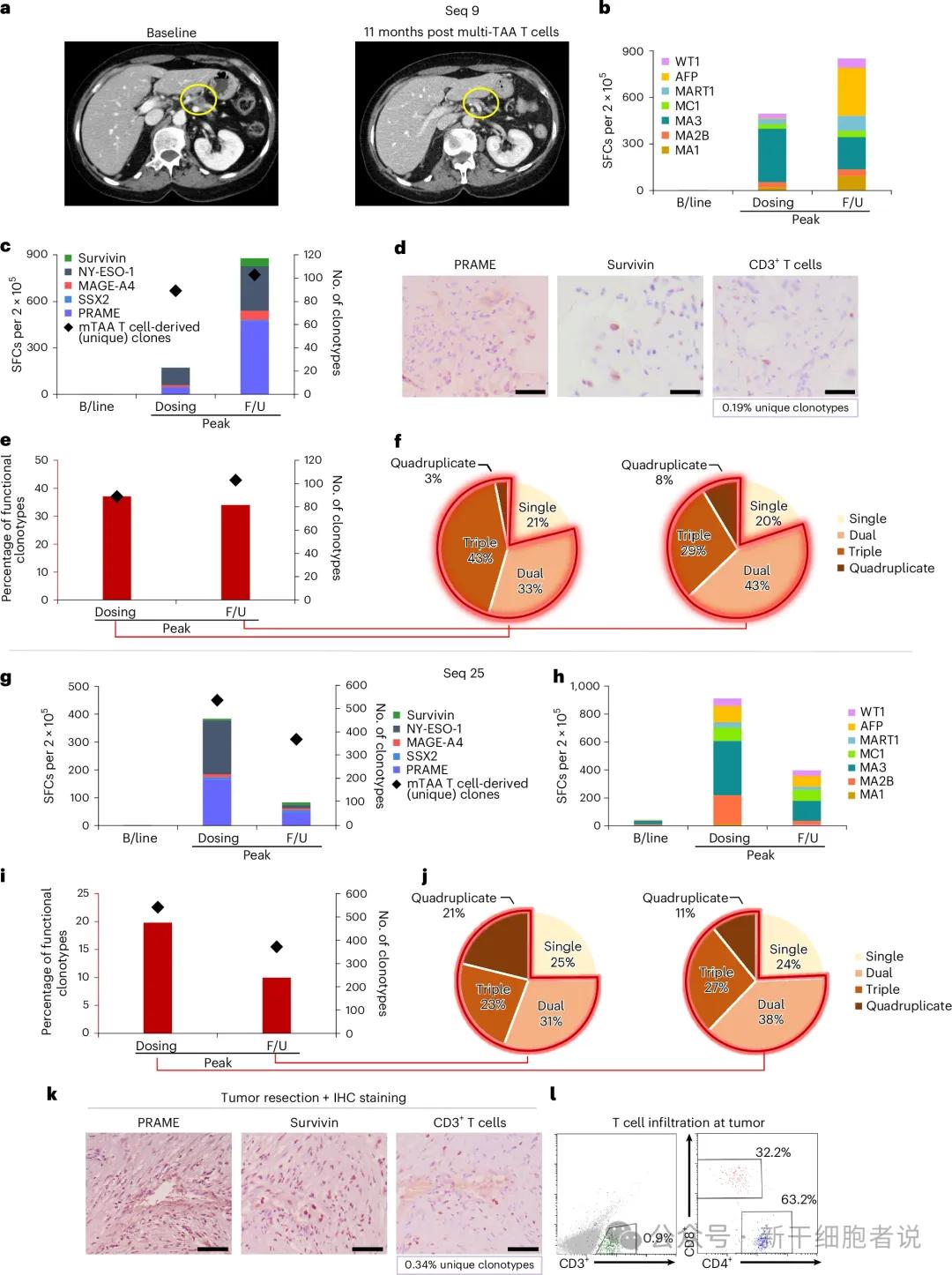
个体临床及免疫相关数据
讨论
这项研究评估了在胰腺癌各疾病分期及各线治疗患者中,连续输注自体多肿瘤相关抗原(mTAA)T细胞的安全性与可行性。在经过多线预治疗的受试者中,制备足够数量的T细胞以完成6次细胞输注仍具备可行性。且单独输注或联合胰腺癌标准靶向化疗均耐受性良好,仅报告1例3级治疗相关严重不良事件(一过性脂肪酶升高),未出现细胞因子释放综合征(CRS)病例。
虽然疗效并非本试验的主要研究终点,但仍观察到客观临床缓解,且主要出现在同时接受化疗的A组患者中。这些患者在启动T细胞输注前已接受了3~4个月化疗,不过其疾病控制率(84.6%)、中位缓解持续时间(7.5个月)及中位总生存期(14.1个月)结果令人鼓舞。
从免疫学角度来看,有明确证据表明:靶向肿瘤相关抗原及非靶向抗原的肿瘤抗原特异性T细胞可在体内持续存在、扩增并被持续检测到(抗原表位扩散)。而且,T细胞应答(强度、广度及功能)与临床结局显著相关。
这项小型非随机研究存在一定的局限性。只有通过随机对照试验,才能证实输注的T细胞对疾病缓解和生存期存在独立贡献。未来,有必要对该治疗方案开展进一步研究,包括单药应用或与其他互补性疗法联合使用。
— END —

新干细胞者说
- 科普 情怀 责任 -