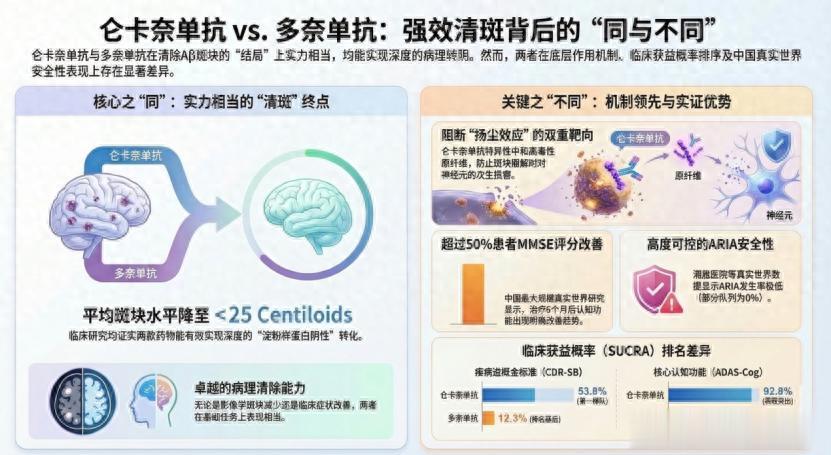
随着抗淀粉样蛋白(Aβ)靶向药物相继进入中国临床,阿尔茨海默病(AD)的疾病修饰治疗正式迈入了精准时代。面对目前临床上备受关注的两款单克隆抗体,医生在处方选择时常聚焦于一个核心议题:它们究竟有哪些“同与不同”?
有效清除大脑中的淀粉样蛋白斑块,是阻断AD病理级联反应的必由之路。在肯定“清斑”核心地位的前提下,我们需要回归严谨的循证医学与真实世界数据:在同样具备强效清斑能力(同)的基础上,不同单抗在病理机制干预、基础研究获益以及真实世界临床应用方面(不同),究竟展现出了怎样的差异化特征?
一、 核心之“同”:两款单抗在“清斑结局”上实力相当
以往在评价抗Aβ单抗药物时,淀粉样蛋白正电子发射断层扫描(PET)的数值变化常被作为最直观的重要参考。然而,基于目前对AD发病机制的最新理解,PET所能检测到的已沉积的成熟斑块可能并非最具神经毒性的成分;真正对突触损害最大、最有害的,恰恰是目前PET尚无法直接检测到的聚集形式的可溶性淀粉样蛋白(如原纤维)。因此,能够全面清除可溶性和不可溶性Aβ聚集体的药物,在理论上是更优的病理学解决方案。
但即使聚焦于PET可见的斑块清除这一基础任务,目前获批的仑卡奈单抗与多奈单抗在各自的III期核心临床研究中,均展现出了卓越的病理清除能力。无论是在患者最终的Aβ斑块清除结果方面,还是在医生、患者和家属感受最深的临床症状改善方面,两者都表现出了相当的疗效。
为了更科学、客观地评估这两款药物的实际清斑效能,我们应当超越不同临床试验间难以直接跨界对比的设计差异,直接聚焦于具有核心临床意义的最终清除结局:
清除深度高度一致: 仑卡奈单抗在Clarity AD研究中显示,治疗18个月时患者平均淀粉样蛋白水平降至 22.8 Centiloids ,且随着治疗延续至36个月(OLE研究),病理负荷进一步降低。另一方面,多奈单抗的III期研究同样显示其能将患者的淀粉样蛋白水平降至 <25 Centiloids 的低水平。这表明,从最终的清斑结局上来看,两者的病理清除能力是相当的,均能有效实现深度的“淀粉样蛋白阴性”转化。
综合疗效排名彰显优势: 一项2025年发表于《Frontiers in Neuroscience》、涵盖23项RCT的网络荟萃分析,通过SUCRA值对疗效进行了概率排序:
· CDR-SB(疾病进展金标准):仑卡奈单抗的SUCRA值为53.8%(排名第一梯队),多奈单抗为12.3%(排名靠后)。
· ADAS-Cog(核心认知功能):仑卡奈单抗的SUCRA值为92.8%,多奈单抗为12.3%(排名靠后)。
该分析明确指出,仑卡奈单抗在提供稳健且确切的临床获益方面更具优势。
既然在“清斑”这一基础任务上两者实力相当,且网络荟萃分析已提示了临床获益排名上的差异,那么进一步决定临床优选的核心,便落在了机制的底层差异与真实世界的表现上。
二、 机制之“不同”:靶向“毒性原纤维”与微环境重塑的深层保护
虽然两者的终极目标都是降低脑内斑块负荷,但其结合靶点的特异性差异,造就了截然不同的病理生理学获益。
多奈单抗主要高度特异性结合已沉积的N端焦谷氨酸修饰的Aβ斑块。而 仑卡奈单抗则具备独特的“双重靶向”机制:在同等高效清除不溶性斑块的同时,对前文提到的高毒性可溶性Aβ原纤维具有极高的亲和力。 这一机制在近期的基础研究中展现出了超越影像学的多重获益:
精准诱导小胶质细胞功能重塑: 2025年发表于《Nature Neuroscience》的重磅基础研究通过单细胞测序揭示,仑卡奈单抗并未引发导致严重副作用的广泛促炎风暴,而是 诱导小胶质细胞进行转录程序的“功能重塑”,使其进入一种高效、以清除为导向的吞噬状态。
成功阻断“扬尘效应”: 临床病理数据证实,当巨大的淀粉样蛋白斑块被抗体崩解时,会向脑微环境中释放大量具有神经毒性的原纤维(即扬尘效应)。 仑卡奈单抗凭借对原纤维的高亲和力,能够在其释放的瞬间发挥特异性中和作用,成功阻断其对周围神经元突触的次生损伤。 这种既清斑块、又控毒性原纤维的能力,提供了更为全面的神经保护。

三、 临床实证之“不同”:最大规模中国队列确证疗效与安全性
机制的先进性最终需要通过真实世界的临床数据来检验。在真实世界更为复杂的用药环境下(患者年龄跨度更大、伴随疾病更多),仑卡奈单抗交出了迄今为止全球范围内、尤其是中国最大规模的真实世界答卷。
近期由国内顶尖医学中心牵头、发表于国际权威神经科学期刊《Brain》的多中心前瞻性队列研究,详细披露了 407例 接受仑卡奈单抗治疗的中国早期AD患者数据,展现了其在真实世界中的显著差异化优势:
疗效表现迅速且显著: 真实世界研究结果不仅复现了三期临床的获益趋势,更在特定指标上展现了积极的疗效。数据显示, 超过50%的患者在接受仑卡奈单抗治疗6个月后,其简易智力状态检查量表(MMSE)评分出现了明确的改善趋势。 这一在真实世界中立竿见影的临床获益,有力证实了全面控制淀粉样蛋白病理(存量斑块+增量原纤维)的优越性。
安全性高度可控,护航长期治疗: 淀粉样蛋白相关影像学异常(ARIA)是限制抗Aβ治疗长期应用的主要顾虑。 仑卡奈单抗在多项间接比较中均展现出了相对更低的总体ARIA风险(三期临床ARIA-E发生率为12.6%)。 令人振奋的是,中国真实世界数据进一步证实了其出色的安全性表现。例如, 中南大学湘雅医院沈璐教授团队发布的真实世界队列数据显示,患者在接受仑卡奈单抗治疗6个月时的ARIA发生率为0% 。总体而言,真实世界应用中呈现出ARIA风险更低,且发生的 绝大多数为无症状、轻度且可逆的影像学改变 。这种高度可控的安全性特征,为其长期持续用药提供了最坚实的保障。
总结
阿尔茨海默病的抗淀粉样蛋白治疗并非一场单纯比拼数字的短期冲刺,而是一项需要综合考量长期获益与风险的系统工程。
在“强效清斑”这一核心指标上,两款单抗展现出了同样卓越的实力(同)。但在同等清斑的基础上,两者的综合临床获益与应用价值却呈现出显著差异(不同)。仑卡奈单抗不仅在网络荟萃分析中展现出更优的临床获益概率排名,更通过额外靶向毒性原纤维、重塑免疫微环境,在理论与基础病理层面提供了更周全的保护;同时,其在中国最大规模真实世界队列中所展现出的显著认知改善趋势与高度可控的安全屏障,为临床医生制定长期、安全、有效的个体化治疗策略,提供了不可替代的循证医学支撑。
参考文献:
1. van Dyck CH, Swanson CJ, Aisen P, et al. Lecanemab in Early Alzheimer's Disease. N Engl J Med . 2023;388(1):9-21.
2. Sims JR, Zimmer JA, Evans CD, et al. Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial. JAMA . 2023;330(6):512-527.
3. Network meta-analysis of 23 randomized controlled trials on the efficacy of anti-amyloid treatments. Front Neurosci . 2025.
4. De Strooper B, et al. Lecanemab induces microglia transformation and promotes tissue repair in Alzheimer's disease. Nature Neuroscience . 2025.
5. Rao Y, Yu J, et al. Real-world effectiveness and safety of lecanemab in Chinese patients with Alzheimer's disease: a multicenter prospective cohort study. Brain . 2025.
6. Mao C, Wang W, et al. Real world clinical practice of lecanemab at PUMCH dementia cohort: focus on dynamic imaging and biomarker evolution. Alzheimer's Research & Therapy . 2025.
7. Welikovitch L, et al. Amyloid Immunotherapy Affects Multiple Alzheimer’s Pathologies. Presented at: Clinical Trials on Alzheimer's Disease (CTAD).