很多人都有定期体检的好习惯,但拿到体检报告后往往“一脸懵”,尤其是看到肺部检查那一栏出现一些专业术语时,心里疑问无数:这是啥意思?会不会是肺癌?而体检报告上出现下面这3个“字眼”,很可能不是偶然发现,它可能是肺癌早期的影像表现或预警信号,如果医生建议进一步检查,那就不要拖!
 一、体检报告出现哪3个“字眼”,多半是肺癌前兆?
一、体检报告出现哪3个“字眼”,多半是肺癌前兆?其实肺癌早期并非无迹可寻,体检中的胸部CT、痰液检查等项目,往往能捕捉到细微异常,这3个字眼看似普通,却被临床医生列为肺癌高危预警,每一个都值得我们高度警惕。
1、磨玻璃结节(GGO)
磨玻璃结节是胸部CT上看到的一种影像表现,看起来像半透明的雾或磨砂玻璃,密度略高,边缘有时清晰、有时模糊,这也正是它名字的由来。形成这种影像表现的原因,通常是因为肺泡腔内被少量渗出物、炎性细胞、纤维组织或肿瘤细胞所替代,导致CT图像上透光性降低。
这个影像表现本身既可能出现在良性病变(如感染性炎症、局部纤维化)中,也可能是早期原位癌、微浸润性腺癌等恶性肿瘤的影像学起始表现,因此不能简单等同于炎症表现或“没什么大不了”。
根据《中华肺部疾病杂志》2023年第16卷第2期综述,肺磨玻璃结节(GGN)可分为纯磨玻璃结节(pGGN)和混合性磨玻璃结节(mGGN),两者在病理类型和恶性风险上存在显著差异。
依据WHO2021版肺肿瘤分类,GGN相关病变可划分为前驱腺体病变(非典型腺瘤样增生AAH、原位腺癌AIS)和更高风险的恶性病变(微浸润腺癌MIA、浸润性腺癌IAC),这些病变常遵循AAH→AIS→MIA→IAC的自然进展,说明影像学上的GGN可能处于连续的病理演变过程中。
研究显示,pGGN大多为AAH或AIS,生长缓慢,恶性进展风险低;mGGN因含实性成分,更易发展为MIA或IAC,恶性概率显著增加。

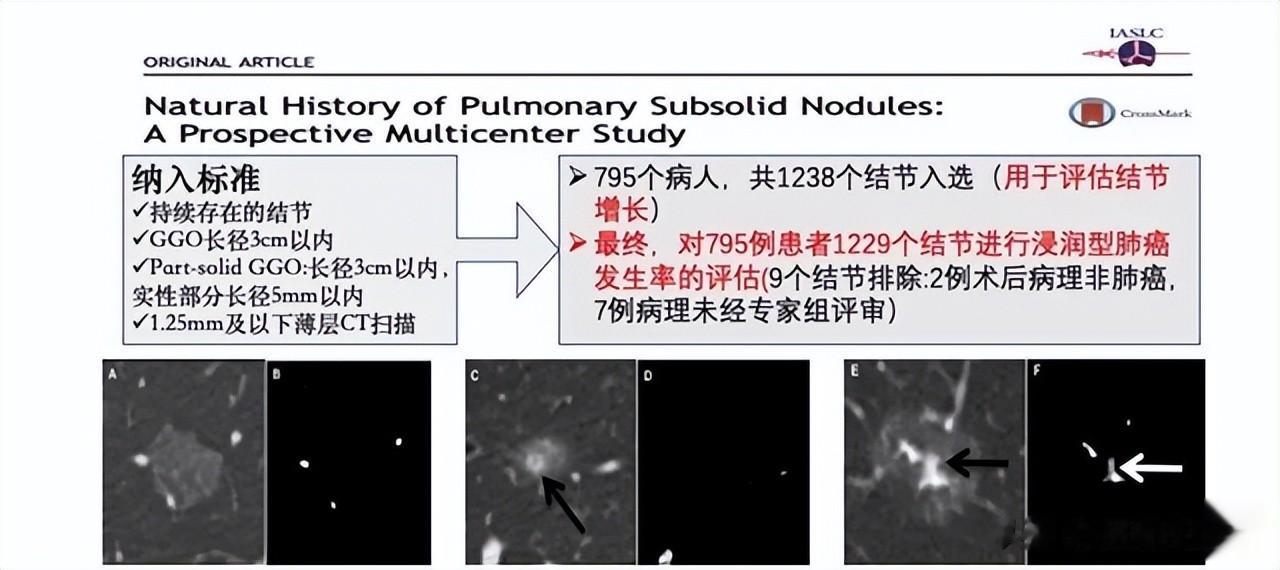
在一项795例GGN随访研究中,pGGN仅6.6%出现密度变化,切除标本中约74.3%为AAH或AIS,MIA极少,IAC未见;而mGGN中MIA和IAC比例分别约为53.1%和24.5%,这些数据说明实性成分的出现显著提升结节的侵袭性风险。
临床上通常采用分级管理策略小于6mm的磨玻璃结节,可以先每半年到一年看看;6到8mm或者冒出实心部分的,要每几个月复查一次;一旦大于8mm、形状怪或实心部分明显,就得赶紧做增强CT、PET-CT或者穿刺活检,弄清楚到底是不是有问题,别拖了。
2、占位性病变
体检报告出现 “占位性病变(肺部肿块)” 这个词时,实际上意味着胸部CT影像上发现了一个明显占据肺组织空间、原本不存在的实体阴影。在医学上,这类病灶若直径大于3 cm通常被称为 “肺部肿块(肺肿物)”,区别于直径 ≤ 3 cm的孤立结节,两者在临床处理和恶性风险评估上有明确区分,根据临床指南与肺癌诊断标准,这一阈值既是筛查参考,也是恶性风险判断的重要分界线。
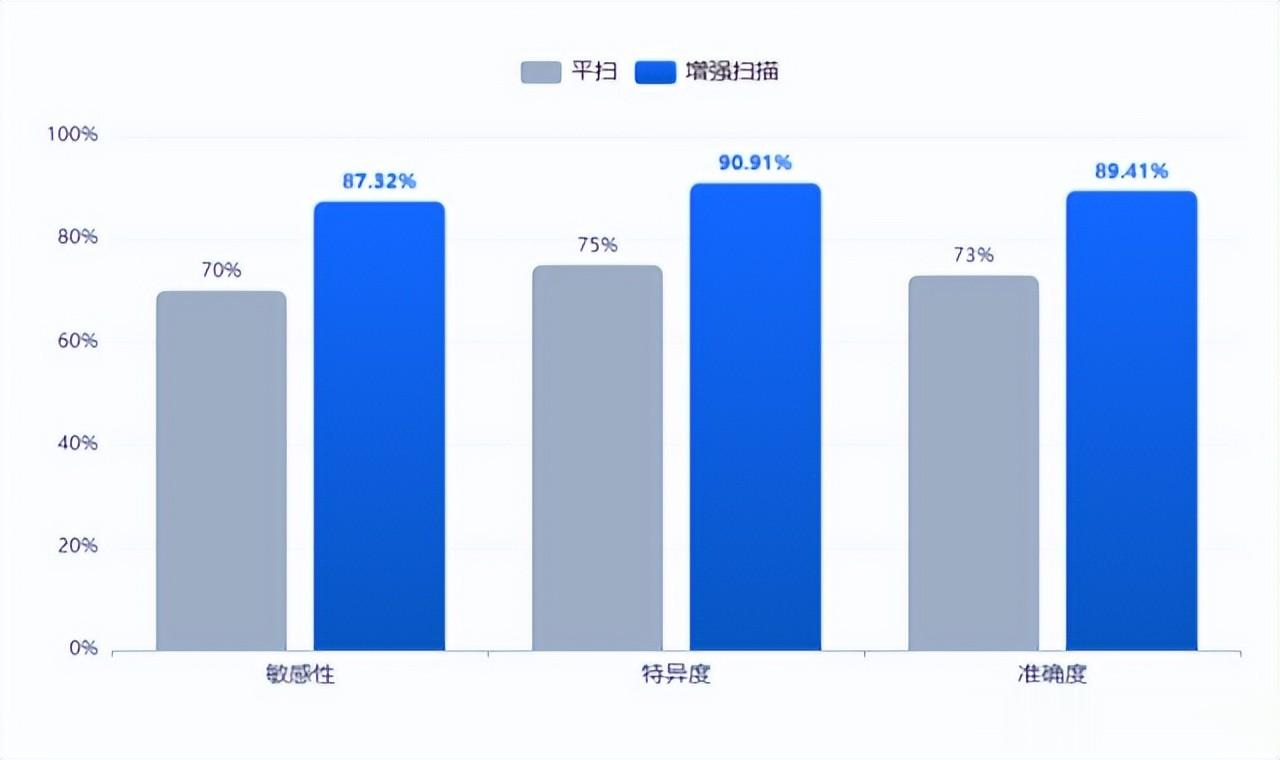
一项名为《多层螺旋CT评估肺部占位性病变的临床价值分析》发表在《中国继续医学教育》期刊对170例经病理确诊的肺占位性病变进行了回顾性分析,结果发现在采用多层螺旋CT(MSCT)进行平扫及增强扫描评估时,针对肺部占位性病变的影像学特征能够有效辅助鉴别良恶性病灶,增强扫描对肺癌的敏感性高达约87.32%、特异度约90.91%,准确度近89.41%,明显优于普通平扫,该研究强调了影像特征与病理确诊联合判断的重要性。
在医学影像学判断恶性风险时,一些定量影像征象是判断良恶性的关键指标,特别是在胸部增强CT或高分辨率CT(HRCT)检查中被广泛采用。
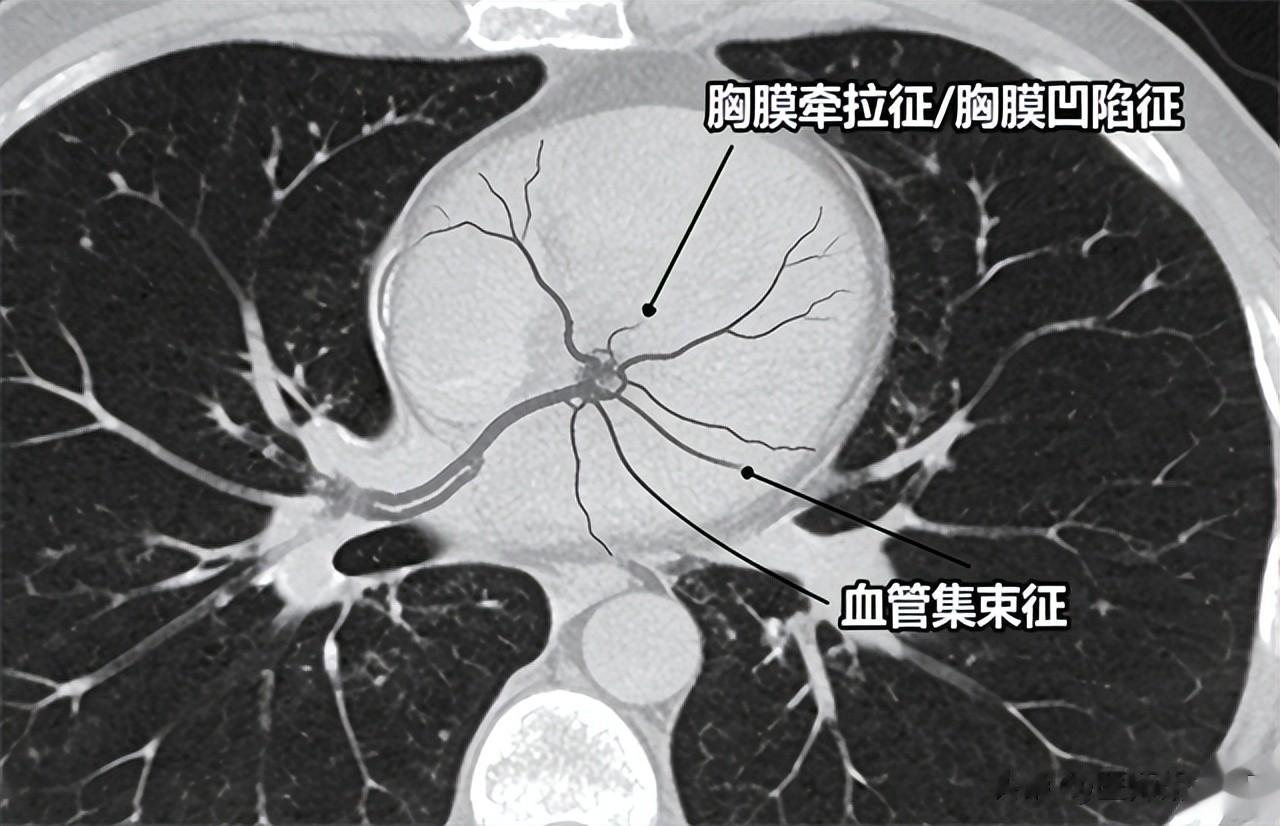
例如研究指出,影像上出现“胸膜牵拉征/胸膜凹陷征”和“血管集束征”与肺癌高度相关:这些征象表现为肿块牵拉胸膜或周围血管向病灶聚集,提示病灶具有侵袭性结构改变。
这些影像学征象背后的核心逻辑正是所谓的“占位效应”,占位性病变不仅在空间上“占据位置”,还可能压迫、牵拉周围组织结构(如血管、胸膜及肺叶),形成典型体征。
相比之下,磨玻璃结节边缘模糊、密度低,占位性病变实性密度高、形态明确,对肺功能及邻近组织影响更显著。早期占位性病变症状轻微,常被误认为感冒或支气管炎;良性病灶(如肺囊肿、肺脓肿)通常伴随感染症状,抗感染后可缩小;而恶性病灶(如肺癌)体积持续增大,可能出现牵拉征、集束征及侵袭或转移迹象。
国内外专家认为,影像学是良恶性初筛关键,但最终判断仍依赖病理活检这一金标准,发现占位性病变后,无论大小,都需认真评估和随访。

3、痰液隐血阳性
相比磨玻璃结节和占位性病变,“痰液隐血阳性 / 痰中带血”更容易被患者本人或家属察觉,它也是肺癌最具有警示价值的早期症状之一,临床实践中非常值得重视。
《原发性肺癌诊疗指南》指出,大概25%到40%的肺癌患者,确诊的时候都出现过咳血或者痰里带血的情况。一出现这种症状,往往说明肿瘤已经伤到了气道里的黏膜,或者旁边的血管,这可是医生判断肺癌的重要信号之一。
痰里带血的样子五花八门,有的能直接看到痰里混着血丝、血点,有的却一点痕迹都没有,得去医院做痰液隐血检查才能发现,而“痰中带血(咳血)” 是肺癌常见的呼吸道表现,像非小细胞肺癌这类常见类型,肿瘤会侵蚀支气管黏膜、破坏血管壁,造成轻微出血,这些血混在痰里就被咳出来了。

这种症状出现的机制主要是肿瘤组织生长侵蚀支气管黏膜血管、肿瘤表面破溃或局部坏死,使微血管破裂、血液混入痰液中排出体外。由于中央型肺癌(靠近大气道的鳞癌或小细胞肺癌)更容易侵犯大支气管,其痰中带血的发生率明显高于周围型肺癌。
很多人可能会误以为痰中带血只是普通呼吸道炎症、咽喉出血或牙龈出血而不以为意。但需要明确的是:普通炎症引起的痰液出血往往伴随明显感染症状(如咽喉痛、咳脓痰、发热),经抗感染治疗后可改善;肺癌相关的痰中带血则多为反复出现、间断性发作,通常不伴随明显炎症表现,在止血或消炎药物治疗下难以完全缓解。
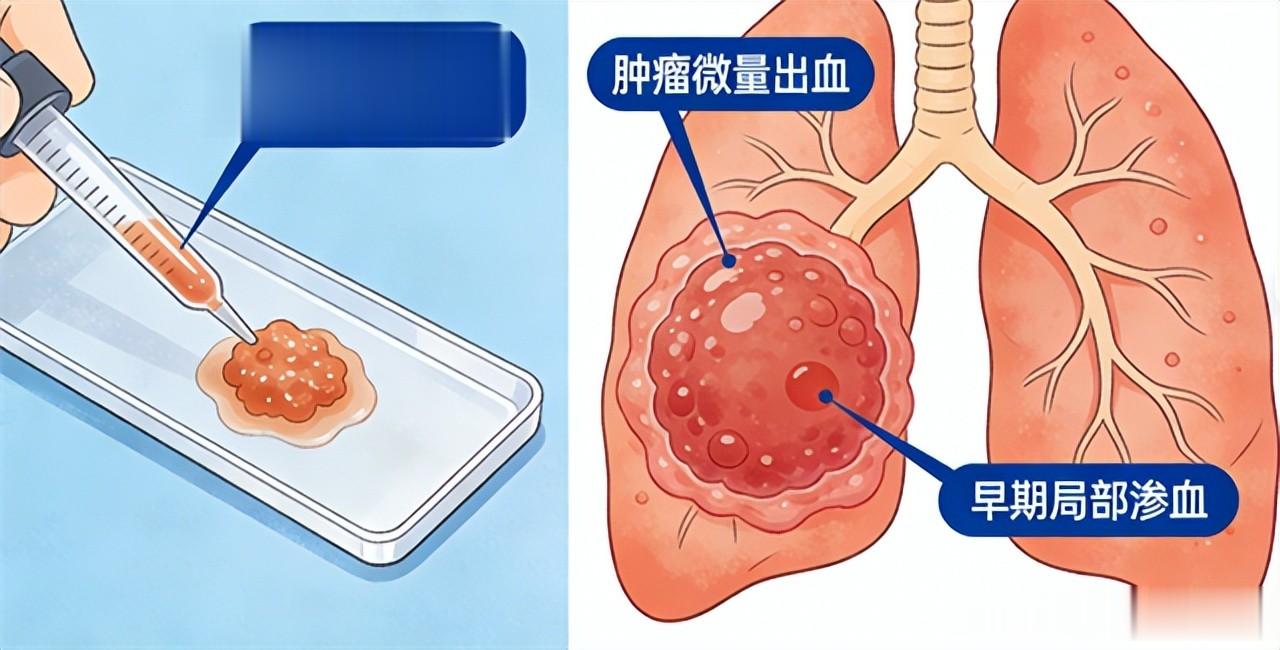
因此,即使是痰液隐血阳性(肉眼未见血),也不能掉以轻心,因为这可能是肿瘤微量出血、肿瘤早期局部渗血的表现。
出现这种情况时,无论是否伴随其他症状,都应尽快做胸部低剂量CT(LDCT)检查、支气管镜检查等进一步评估,排查潜在的肺部病变,而不是简单归咎于普通炎症或感冒。
了解了这3个危险字眼的背后含义,我们更要清楚哪些人是肺癌的高发群体,才能针对性做好筛查和防范,从源头降低患病风险。
 二、肺癌的高发人群有哪些?
二、肺癌的高发人群有哪些?明确肺癌高发人群,能帮助我们判断自身风险等级,制定科学的体检和筛查计划,以下几类人群,肺癌患病风险远高于普通人。
经常吸烟的人,以及长期接触二手烟或三手烟的人,肺癌风险会明显增加,因为吸烟是肺癌最确定、最重要的危险因素。

世界卫生组织(WHO)和《中国肺癌筛查与早诊早治指南(2021年版)》都明确指出,吸烟是导致肺癌发生的首要风险因素,烟草燃烧产生的烟雾中含有至少69种明确致癌物质(如苯并芘、多环芳烃类、亚硝胺等),这些致癌物可造成肺细胞DNA损伤,长期累积会显著提高细胞癌变的风险。抽烟的人比不抽烟的人更容易得肺癌,而且抽得多、抽得久风险就更大,越早开始抽烟、抽了越多年,风险就越高。
一项流行病学总结数据显示,吸烟可使肺癌的发生风险提高约10倍以上,有研究指出当每日吸烟量很大(如每天超过35支)时肺癌风险甚至可能进一步升高到20倍以上。而且在中国,约有超过80%–90%的男性肺癌病例与吸烟密切相关,这进一步说明了吸烟行为本身对肺癌负担的直接影响。
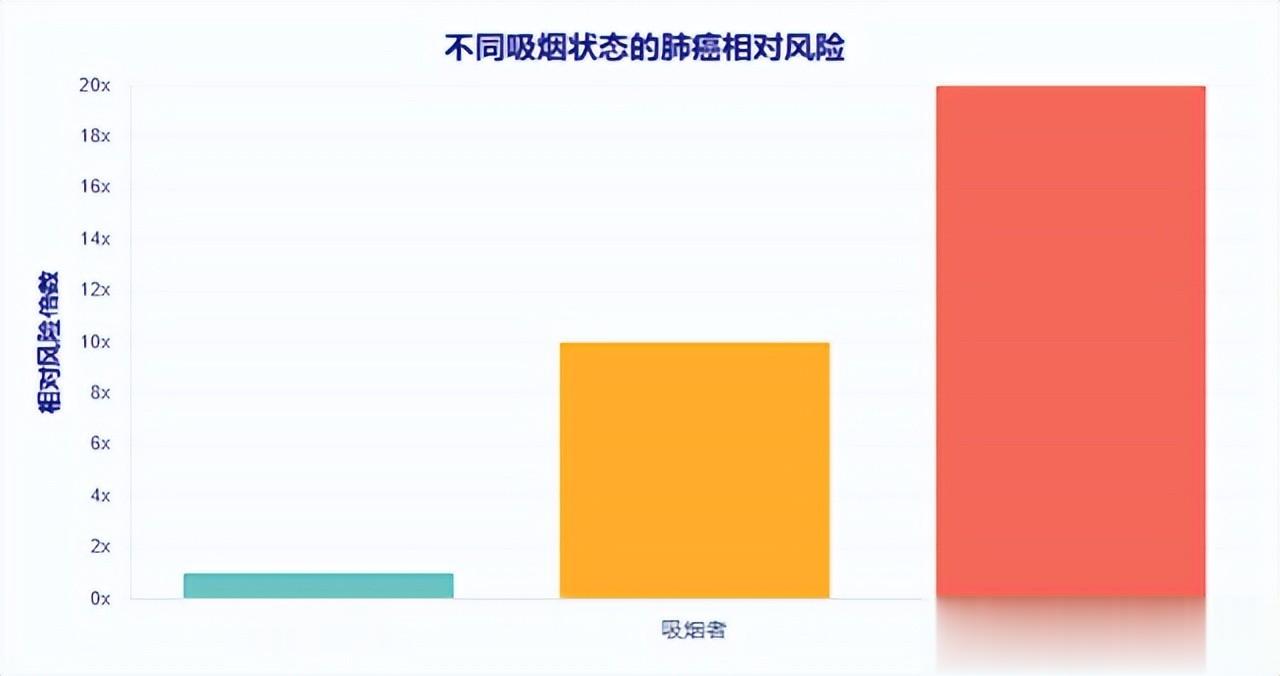
无论自己点烟,还是被动吸入二手烟或三手烟,肺部都在受伤,根本没有安全剂量。吸烟的人像背着重担,肺癌风险很高;不吸烟的人如果长时间待在烟雾里,也会慢慢增加危险。
基于这些,建议大家主动吸烟者应尽早戒烟,吸烟越早停止、风险降低越明显;非吸烟者应尽可能远离烟草烟雾,避免二手烟和三手烟暴露;对于有烟草暴露史的人群,特别是40岁以上,建议定期进行胸部低剂量CT(LDCT)筛查,有助于早期发现潜在病变,提高肺癌早期诊断率与生存率。
患有慢性肺部疾病的人群,慢性肺部疾病并不仅仅是“呼吸不顺”,它会让肺部组织长期处于慢性炎症、损伤和修复循环之中,这种长期的炎症刺激显著增加了肺上皮细胞的基因突变概率,从而显著提高了肺癌的风险。
常见的慢性肺部疾病包括慢性阻塞性肺疾病(慢阻肺/COPD)、肺结核后遗症、肺纤维化、支气管扩张等,它们往往伴随气道持续性炎症和组织破坏。需要通过低剂量胸部CT早期筛查来提高早诊率,慢阻肺和肺癌不仅共享危险因素(如吸烟),本身的炎症与气道结构破坏也使两者在发生机制上密不可分。
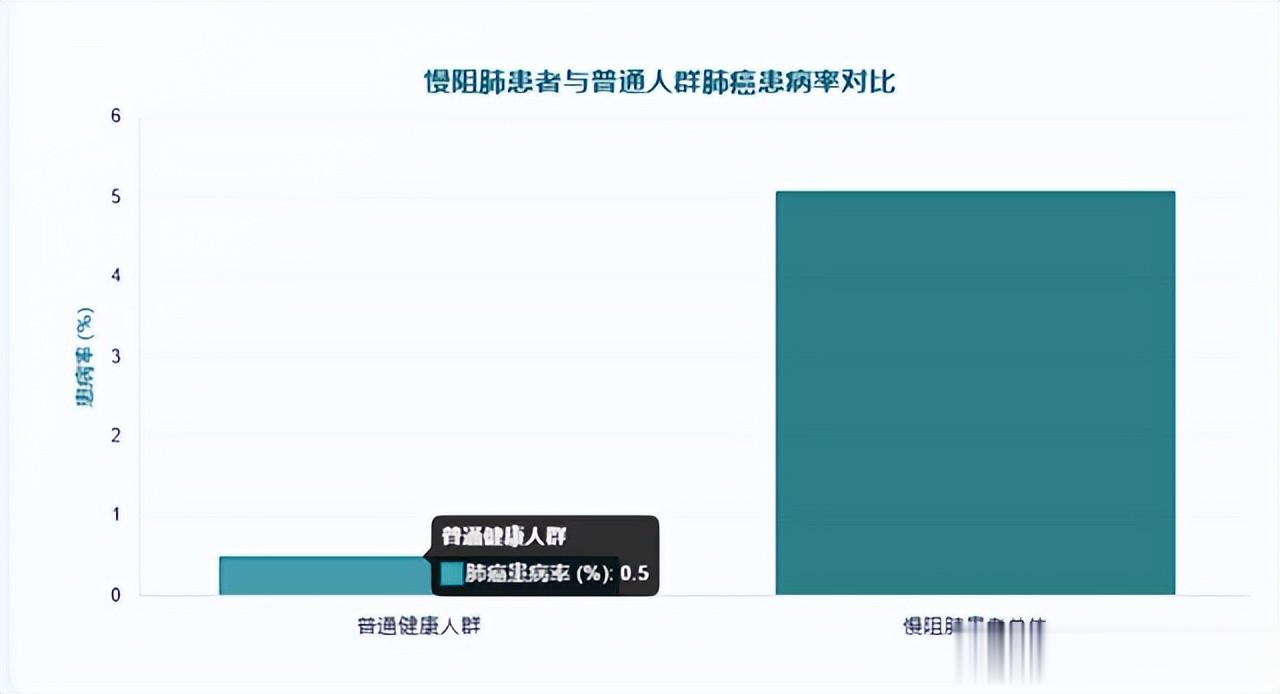
另一项覆盖全球30多个研究的数据分析显示,在慢阻肺人群中,肺癌的发病率明显高于普通健康人群。该系统性综述发现慢阻肺患者中肺癌的总体患病率约为 5.08%(95% CI 4.17‑6.00%),而吸烟或既往吸烟者中的比例甚至更高。
所以,从流行病学与生物病理机制来看,慢性肺部疾病患者的肺癌风险明显高于普通人群。
体检报告中出现“磨玻璃结节”“占位性病变”“痰液隐血阳性”这三个字眼,不能掉以轻心,它们往往是肺癌早期或潜在病变的信号。对于高危人群,如长期吸烟者、慢性肺病患者及40岁以上人群,更应重视定期胸部低剂量CT筛查和专业复查,及时识别可疑病变。体检报告只是提示,不能自行判断或忽视,一旦出现异常,应尽快就医。
参考资料1、中华肺部疾病杂志.肺磨玻璃结节自然衍变规律与CT鉴别诊断研究现状及进展.2023-04
2、PUMCH核医学.关于肺磨玻璃结节的一切.2022-07-31
3、中华流行病学杂志.全球肺癌流行数据解读[J].2024
评论列表