程序性死亡配体 1(PD-L1,又称 CD274 或 B7-H1)是肿瘤免疫治疗领域中最核心、最受关注的靶点之一。作为 I 型跨膜糖蛋白,它隶属于 B7 免疫调控蛋白家族,由 290 个氨基酸构成,结构上包含胞外 IgV 样与 IgC 样结构域、跨膜区以及胞内尾部,是介导免疫抑制、肿瘤逃逸与治疗响应的关键分子。
在正常生理状态下,PD-L1 的表达主要由炎症因子诱导,其中 γ- 干扰素是最主要的调控信号。它广泛表达于抗原递呈细胞、上皮细胞与血管内皮细胞表面,参与维持机体免疫稳态,避免免疫系统过度激活而攻击自身组织,是维持免疫耐受的重要分子。
而在肿瘤微环境中,PD-L1 的异常高表达,成为肿瘤细胞躲避机体免疫监视、实现恶性增殖与侵袭转移的重要 “武器”,也直接决定了免疫检查点抑制剂的治疗效果。
一、PD-L1 的三大核心生物学特征表达具有高度可诱导性PD-L1 的表达并非固定不变,而是受到 IFN-γ、EGFR、NF-κB 等多条信号通路的精密调控。肿瘤细胞可在免疫压力、炎症刺激或治疗干预下快速上调 PD-L1 水平,以此适应肿瘤微环境并增强免疫逃逸能力。
表达呈现时空异质性PD-L1 在肿瘤组织中的分布具有显著不均一性。同一患者的原发灶与转移灶、治疗前后、甚至同一肿瘤内部不同区域,其表达水平均可出现明显差异。这种异质性不仅影响活检检测的准确性,也是免疫治疗疗效差异的重要来源。
功能具有多重性PD-L1 不仅是免疫抑制配体,还具备独立调控肿瘤细胞自身行为的能力。它既可以抑制 T 细胞功能,也能通过信号传导影响肿瘤细胞的增殖、存活、迁移与耐药,在肿瘤进程中扮演着类似内源性致癌因子的角色。
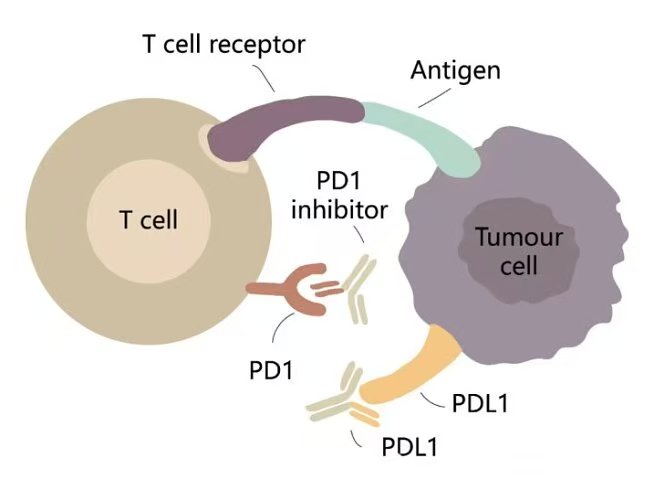
二、PD-L1 介导的三大关键作用机制1. 与 PD-1 结合:经典免疫抑制通路PD-1 是主要表达在活化 T 细胞、B 细胞等免疫细胞表面的抑制性受体。PD-L1 与 PD-1 结合后,会激活胞内抑制信号,阻断 T 细胞活化通路,最终导致 T 细胞耗竭、增殖停止甚至凋亡。这是肿瘤实现免疫逃逸最核心的机制,也是 PD-1/PD-L1 抑制剂发挥疗效的基础。
2. 与 B7-1(CD80)结合:非 PD-1 依赖的免疫抑制B7-1 是调控 T 细胞活化的重要分子,可与 CD28、CTLA-4 结合。近年来研究发现,B7-1 同样可作为 PD-L1 的配体,亲和力虽仅为 PD-1 的三分之一,却能独立介导免疫抑制。PD-L1 通过占据 B7-1,阻断其与 CD28 的结合,从而削弱 T 细胞活化,这也是部分患者出现免疫治疗耐药的重要原因。
3. 反式信号传导:调控肿瘤细胞自身生物学行为除了向免疫细胞传递抑制信号,PD-L1 还可发生反向信号传导。当 PD-L1 与配体结合后,信号会反向传入肿瘤细胞内部,直接调控细胞增殖、抗凋亡、侵袭与转移能力。这一机制为新一代免疫治疗提供了全新方向:既恢复 T 细胞功能,又直接抑制肿瘤生长。
三、总结