如何提升细胞的转染效率呢
[一R]选择合适的细胞类型:首先对于慢病毒的转染我们要选择好合适的细胞系,如HEK293或COS-7细胞;
[二R]细胞活性:
1)为获得良好的转染效率,建议使用活性超过90%的细胞,密度在70%-90%左右,可以通过台盼蓝染色测定细胞活性。
2)不建议使用传代次数超过15次的细胞进行实验。
3)新复苏的细胞在转染实验前需传代2-3次,待细胞恢复正常生长后使用。
[三R]血清和抗生素:在转染过程中,尽量避免使用血清和抗生素,因为它们可能会影响转染效率。但现在市面上的一些转染试剂没有要求一定要用无血清的培养基,具体情况还是要根据实际转染试剂决定。
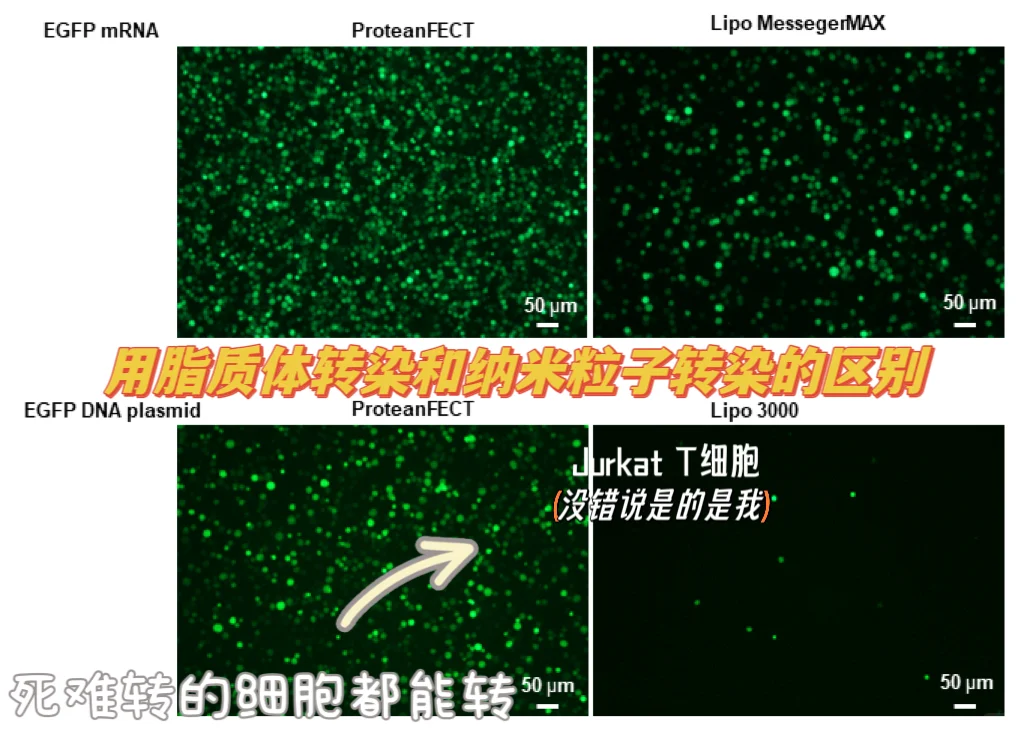
[四R]使用辅助技术:使用电穿孔、核糖体,蛋白纳米颗粒等物理或化学方法辅助转染(P3P4)。
[五R]优化转染时间:确定最佳的转染时间,因为过长或过短的转染时间都可能影响效率。对于脂质体而言,通常在转染后6-8h进行换液;
[六R]质粒DNA能否用于原代细胞转染
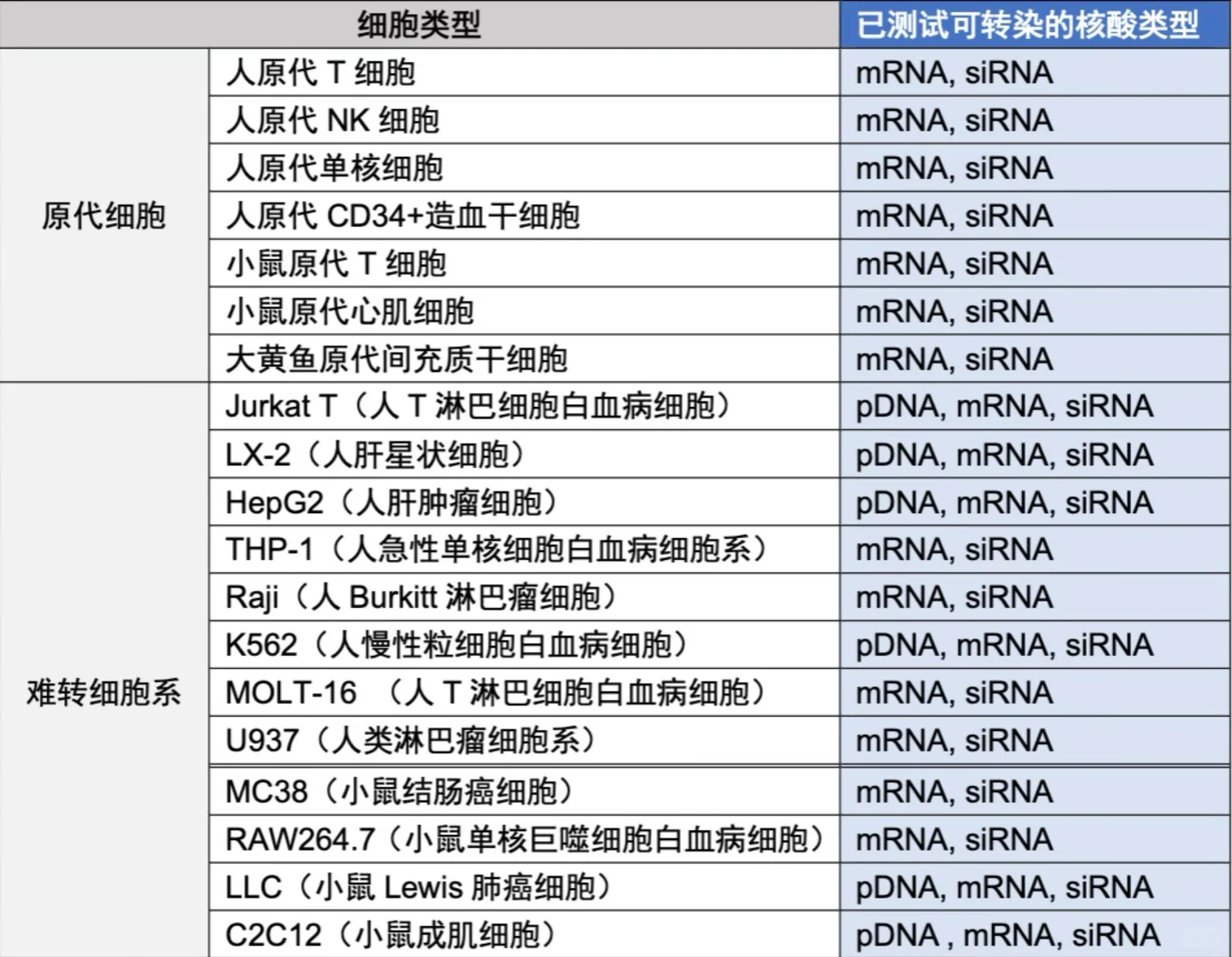
双链DNA转染原代细胞可能引起一定的毒性,例如炎症应激,因此需根据实验目的谨慎选择。以人或小鼠来源的原代T细胞为例,使用质粒DNA转染可能导致显著的细胞毒性,因此不适合此类细胞。而大多细胞系通常经过多代培养,能更有效地应对外源DNA带来的压力,对双链DNA转染的耐受性较高,因此可以使用质粒DNA进行转染。
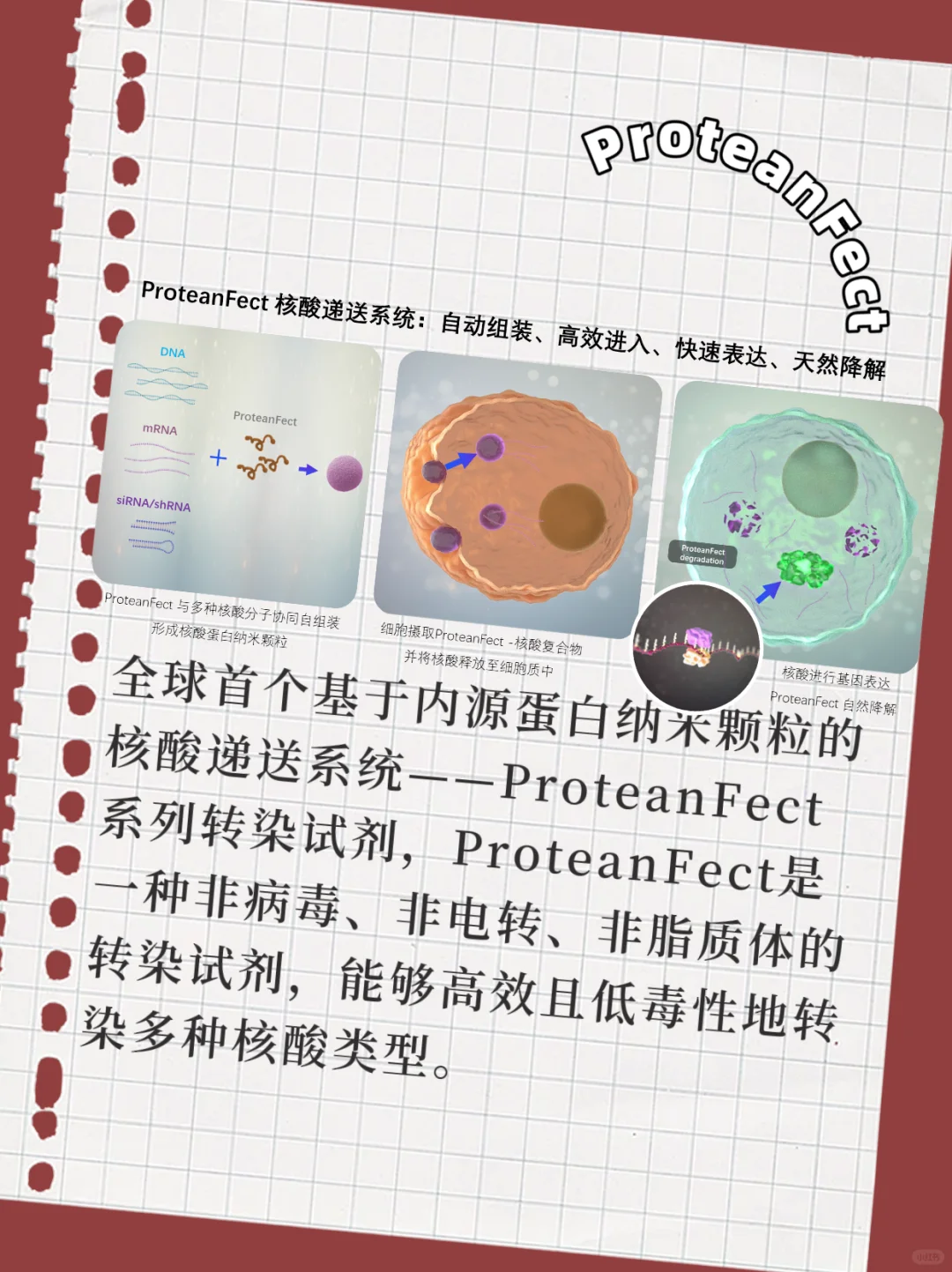
需要转染人或者鼠的原代T细胞的话,可以用[向右R]西湖凝聚体研发的蛋白递送的转染试剂ProteanFect,转mRNA来过表达,转siRNA来敲除.因为是基于内源蛋白纳米颗粒转染的所以刺激性小,细胞活率高。
[七R]质粒DNA转染要求
转染效率受DNA质量影响。建议使用无内毒素试剂盒制备DNA,并确保OD值在1.7-1.9之间;使用无核酸酶纯水将DNA稀释至0.5-2 μg/μL的浓度。












评论列表