近年来,免疫疗法(PD-1/PD-L1抑制剂等)的问世改变了癌症治疗的格局,甚至已成为部分癌种,如肺癌、黑色素瘤、肾癌等的核心治疗选择。然而,理想与现实之间仍有差距——
疗效上,晚期非小细胞肺癌(NSCLC)单药免疫检查点抑制剂(ICIs)的客观缓解率仅39%-45%,黑色素瘤双药ICIs也仅50%-58%,约半数患者对这些方案无应答;即使获得缓解,晚期肾癌患者多数仍会在5年内发生进展;安全性上,许多患者会出现免疫相关不良事件(irAEs),部分是危及生命的毒性,需中断甚至终止治疗,严重影响最终结局。
难道就没有办法让免疫治疗更有效、更安全吗?Nature Medicine最新发表的两项重磅研究给出了惊喜答案[1-2]!既让疗效显著飙升,还能最大限度降低毒性,这位免疫治疗的「黄金搭档」竟然就藏在「粪便」里?!
I期PERFORM试验:为肾癌免疫治疗增效减毒初探在最新一期中,Nature Medicine首先刊发了针对转移性肾癌(mRCC)的I期PERFORM结果。这项开放标签、单中心I期试验,首次探索了健康供体粪便微生物群移植(FMT,LND101)联合免疫治疗在初治中高危肾癌患者中的安全性和效果。
入组患者在首次接受免疫治疗7天前启动封装型健康捐赠者FMT全剂量治疗,随后在第3周和第6周接受两次半剂量FMT。主要终点为安全性,以irAEs的发生率和严重程度定义;次要终点包括临床应答、肠道微生物群及免疫相关性指标,以及患者报告的生活质量等。
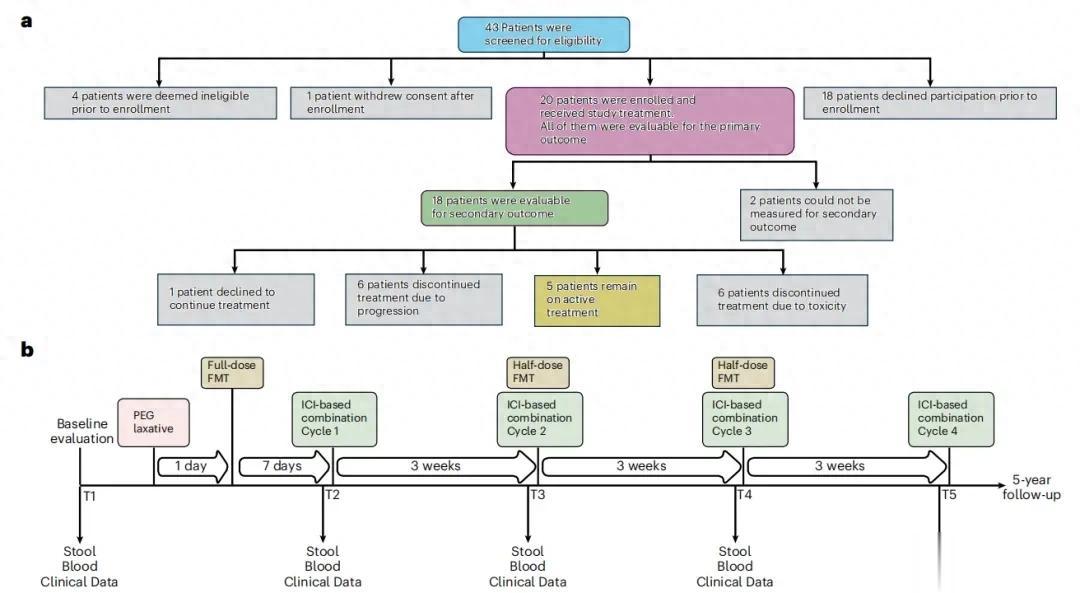
研究流程:a. 筛查、登记和接受研究治疗的患者人数;b.样本采集和治疗管理的研究设计和时间表。
截至数据截止日,中位随访时间为21.9个月,5例患者(25%)仍在接受全身治疗。从首次FMT开始的中位治疗持续时间为13.4个月。20例初治mRCC患者接受了FMT联合伊匹木单抗/纳武利尤单抗(n=16)、帕博利珠单抗/阿昔替尼(n=3)或帕博利珠单抗/仑伐替尼(n=1)治疗。
研究达到了安全性终点。唯一的FMT相关毒性为1例患者(5%)出现1级胃肠道事件,15例患者(75%)完成了全部3剂计划FMT。17例患者(85%)出现任意级别irAEs,10例患者(50%)出现3级irAEs。接受帕博利珠单抗/阿昔替尼或帕博利珠单抗/仑伐替尼治疗的患者(n=4)未出现3级及以上irAEs。未观察到严重FMT相关毒性或4-5级irAEs发生。

治疗相关不良事件(仅FMT相关及FMT联合基于ICI的治疗相关)
疗效方面,18例可评估患者中,ORR达到50%(9例),其中2例(11%)肿瘤完全消失(完全缓解/CR),12例患者(67%)获得临床获益(定义为CR、部分缓解/PR或疾病稳定/SD≥6个月)。
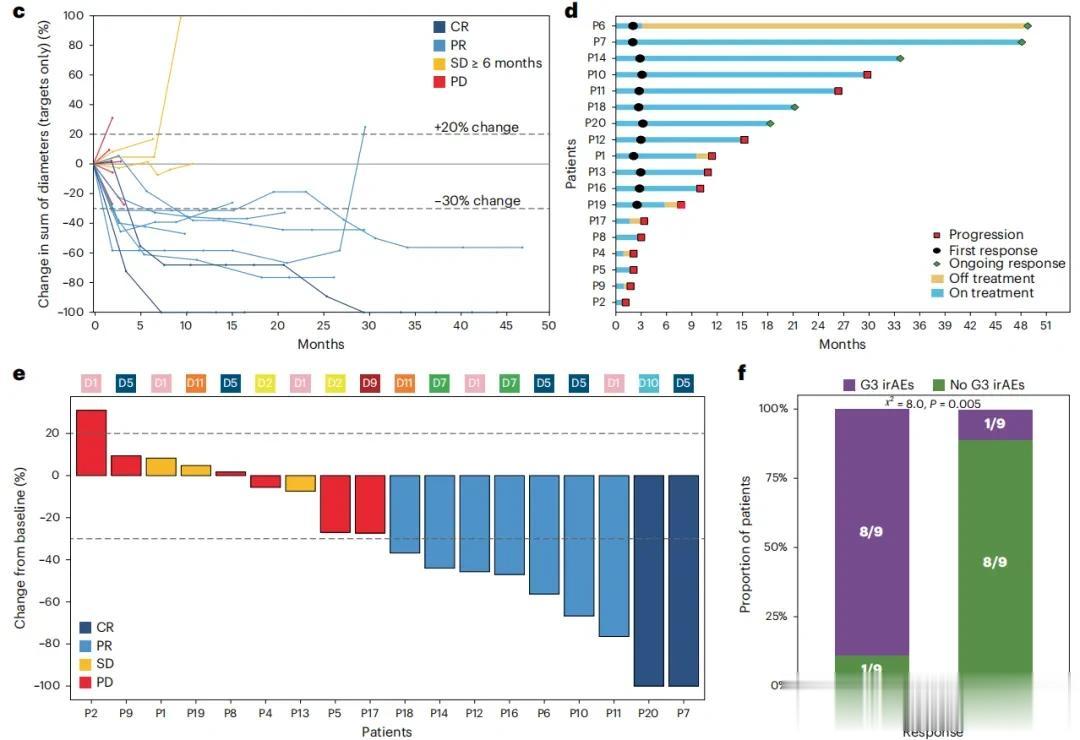
FMT联合一线ICI治疗的临床疗效
值得注意的是,9例应答者中仅1例(11%)出现3级irAEs,而9例无应答者中则有8例(89%)。进一步分析提示疗效与安全性存在显著关联(χ²=8.00,P=0.005)。中位随访21.9个月后,符合方案人群(n=18)的中位PFS为11.15个月,ITT人群(n=20)的中位OS为36个月。
本I期研究证实,FMT联合ICIs的治疗在转移性肾癌中具有安全性和可行性。尽管为中危或高危疾病,大多数患者仍获得临床获益,且大多数应答者未出现严重毒性——这在转移性肾癌中是一项新发现,提示功能性微生物群植入有望优化治疗效果的同时,最大限度地降低毒性。
Ⅱ期FMT-LUMINate研究:两大癌种免疫治疗效果翻倍验证同期登发Nature Medicine的FMT-LUMINate研究则是一项多中心、开放标签Ⅱ期试验,在一线治疗中评估FMT联合免疫治疗用于NSCLC或黑色素瘤的效果。主要终点为NSCLC患者的ORR,次要终点包括疾病控制率(DCR)、黑色素瘤队列的ORR、FMT联合ICI的安全性以及捐赠者-宿主微生物群相似度等。
患者先接受来自健康捐赠者的单次口服胶囊剂型FMT,NSCLC队列在FMT后1周内启动一线抗PD-1单药治疗(帕博利珠单抗),黑色素瘤队列则启动抗PD-1+抗CTLA-4双药治疗(纳武利尤单抗+伊匹木单抗)
结果惊艳全场:
NSCLC队列ORR高达80%(16/20),16例患者达到PR,超过预设的64%主要终点,由此研究达到阳性结果标准;DCR为95%,中位缓解持续时间为8.7个月;1年PFS率为65%,1年OS率达到100%!
在次要终点上,为FMT联合抗PD-1+抗CTLA-4用于黑色素瘤队列的活性亦令人振奋:该队列ORR为75%,其中11例PR、4例CR;DCR同样为75%;中位缓解持续时间为10个月;1年PFS率和1年OS率分别为58%和79%。这些结果证实,FMT联合抗PD-1治疗用于NSCLC、联合抗PD-1+抗CTLA-4治疗用于黑色素瘤均具有临床疗效。

FMT联合免疫治疗未经治疗的非小细胞肺癌和黑色素瘤患者的临床疗效
安全性上,肺癌队列未出现3级及以上严重不良事件,仅少数患者出现轻微腹泻、皮疹;黑色素瘤队列65%患者出现3级及以上AEs,但独立数据安全委员会确认,这些副作用与ICIs的已知毒性一致,FMT并未额外增加风险。
Ⅱ期FMT-LUMINate临床研究首次提供前瞻性证据,证实来自健康捐赠者的FMT可增强NSCLC患者中抗PD-1治疗的疗效,以及黑色素瘤患者中抗PD-1+抗CTLA-4治疗的疗效,表明FMT的疗效在不同肿瘤病理类型和ICsI为基础治疗中具有可重复性。
FMT是什么?凭什么破解免疫治疗耐药和毒性难题?众所周知,免疫治疗是通过增强免疫系统对肿瘤细胞的监视、识别和消灭,从而抑制肿瘤生长,最终延长患者生存期。与此同时,越来越多的研究发现免疫治疗对肿瘤患者的疗效具有个体差异性,而人体肠道菌群就是一个重要的影响因素。
随着微生物组研究的深入,肠道菌群移植(FMT)作为一种新兴的治疗手段,逐渐进入了肿瘤治疗的视野。FMT是一种将健康供体的粪便中的功能菌群经过处理后移植到患者肠道内的治疗方法,核心目的是通过恢复患者肠道菌群的多样性和平衡,来治疗与菌群失调相关的疾病。
说通俗点,FMT就是把健康人肠道里的「抗癌友好菌」,通过口服胶囊的方式「搬家」到癌症患者的肠道中重新「定居」,帮患者重建健康的肠道菌群「社群」。它不直接替代ICIs,而是通过调节肠道环境,为免疫治疗「铺路搭桥」:
01
首先是「赶走捣蛋菌」。两篇文献均证实,疗效好、副作用少的患者,肠道中抑制免疫的「坏细菌」显著减少。比如肺癌和黑色素瘤患者中,肠梭菌属(Enterocloster citroniae、E. lavalensis)、无害梭菌(Clostridium innocuum)等细菌被大量清除,这些细菌原本会导致ICIs耐药、加重炎症反应;肾癌患者中,柯林斯氏拟杆菌(Segatella copri)的富集与3级irAEs密切相关,当它的丰度升高时,接受双免治疗的患者更易出现严重毒性。
02
其次是「请来抗癌菌」。FMT后,肠道会富集有益菌,如肺癌缓解患者的普氏粪杆菌(Faecalibacterium prausnitzii)、Akkermansia菌等增多;黑色素缓解患者中,拟杆菌属(Bacteroides eggerthii、B. faecis)富集;肾癌缓解患者中,普氏粪杆菌、西拉肠球菌(Eubacterium siraeum)增加;这些「抗癌菌」都能激活免疫细胞,增强其抗癌能力。
03
最后是「平衡免疫与代谢」。好细菌不仅能「唤醒」CD8+T细胞、NK细胞等抗癌部队,还能减少「拖后腿」的免疫细胞。同时,FMT能降低喹啉酸、犬尿氨酸等促癌代谢物水平,升高维生素A、硬脂酰肉碱等保护代谢物,为ICIs发挥作用创造良好的代谢环境。
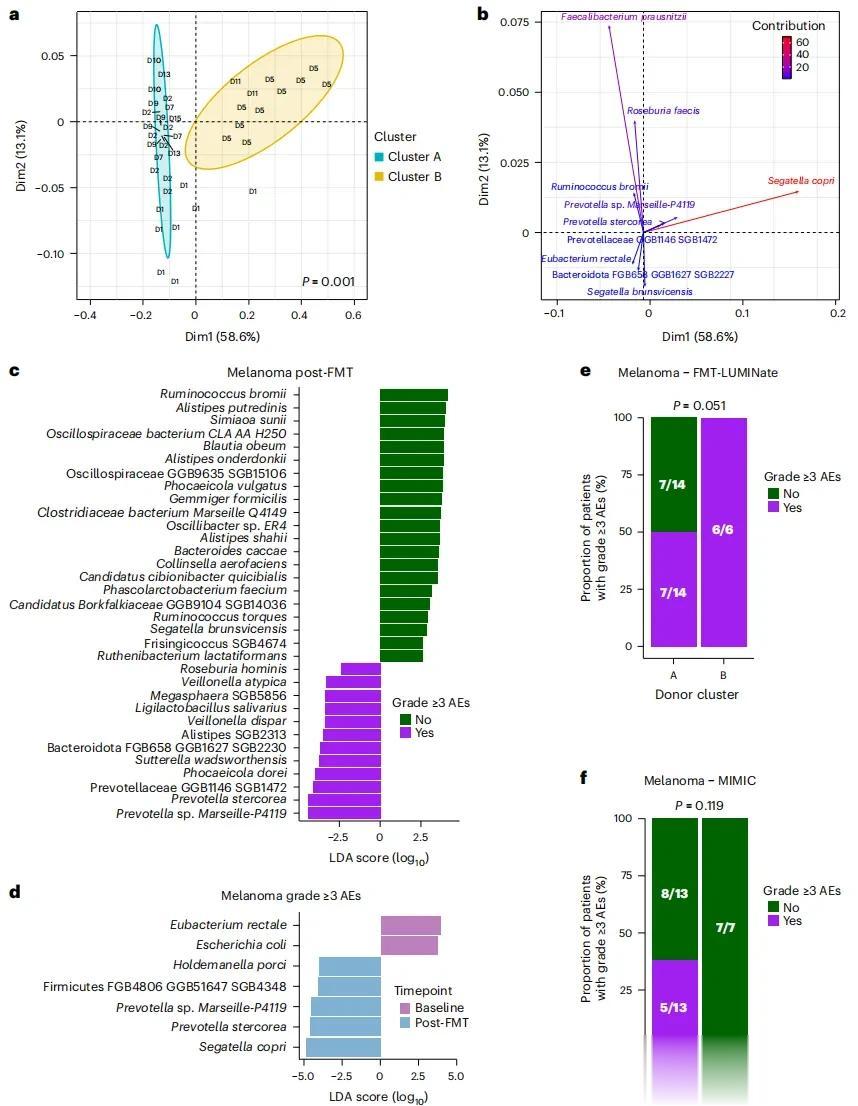
肠道微生物组与3级或更高级别免疫相关不良事件之间的关系
结语Nature Medicine最新发布的两项研究共同证实了FMT作为免疫治疗「增效减毒搭档」的巨大潜力,为免疫治疗耐药、难以耐受毒性的患者提供了新方向。但需要注意的是,目前FMT联合免疫治疗仍处于临床研究阶段,大家切勿自行尝试,需通过正规医院评估是否符合入组条件。
随着研究深入,未来可能会有更多基于肠道菌群的辅助疗法问世,你对这种「肠道菌群搬家」的辅助治疗方式感兴趣吗?欢迎在评论区留言分享你的看法!关注「咚咚癌友圈」,一起追踪最新临床试验进展!
参考文献:
[1]Fernandes, R., Jabbarizadeh, B., Rajeh, A. et al. Fecal microbiota transplantation plus immunotherapy in metastatic renal cell carcinoma: the phase 1 PERFORM trial. Nat Med (2026). https://doi.org/10.1038/s41591-025-04183-8
[2]Duttagupta, S., Messaoudene, M., Hunter, S.et al. Fecal microbiota transplantation plus immunotherapy in non-small cell lung cancer and melanoma: the phase 2 FMT-LUMINate trial. Nat Med (2026). https://doi.org/10.1038/s41591-025-04186-5