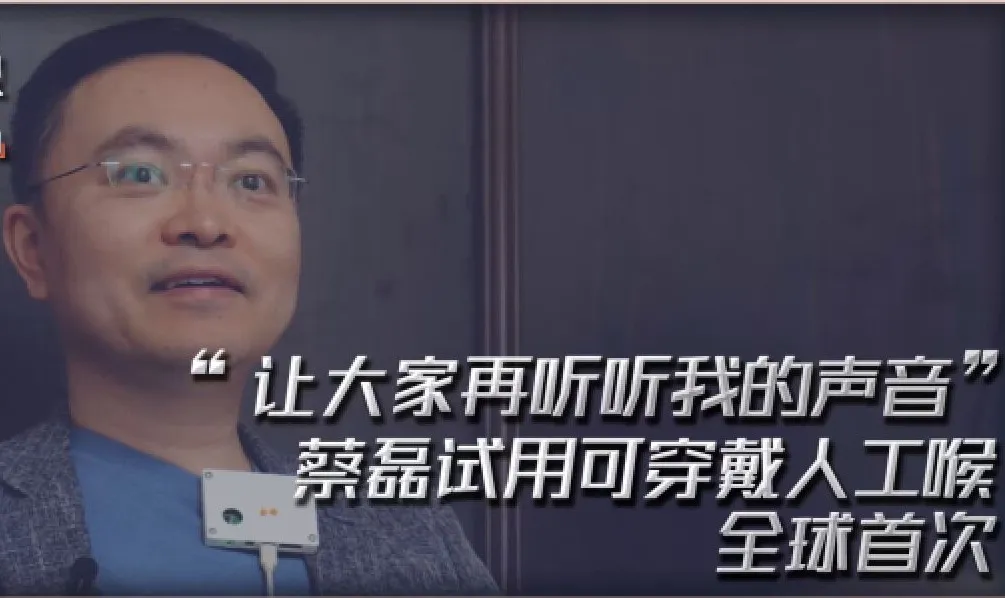
2026 年 4 月,渐冻症(ALS)抗争者、京东原副总裁蔡磊公开披露病情已进入医学定义的终末期,ALSFRS-R 功能评分从满分 48 分降至个位数,全身骨骼肌完全瘫痪、彻底丧失语言与吞咽能力,仅靠眼部肌肉操控眼控仪维持每日超 10 小时的工作,持续推进渐冻症科研转化与器械临床落地。
这不是一个人与绝症的孤军奋战,而是一场撬动中国罕见病医疗器械全产业链、重构 ALS医疗器械注册审评格局、催生百亿级刚性市场的行业变革。从终末期患者赖以生存的呼吸支持设备,到重建沟通能力的可穿戴智能人工喉,从突破身体禁锢的侵入式脑机接口,到精准筛查的基因检测试剂盒,蔡磊七年向死而生的抗冻之路,不仅让渐冻症这一罕见病走进公众视野,更彻底激活了 ALS 医疗器械赛道的研发热情与市场潜力,也让医疗器械注册的合规规划与专业落地,成为医疗器械企业抢占赛道先机的核心生命线。

一、破局之策:根治 ALS 器械供需失衡顽疾,蔡磊推动行业从 0 到 1 实现历史性突破
长期以来,渐冻症(ALS)相关医疗器械赛道始终深陷 “供需双弱、循环闭塞” 的行业顽疾,成为制约产业发展的堵点:
患者端,国内 ALS 患者规模已超 6 万,预计 2030 年将突破 8 万例,全生命周期存在诊断、呼吸支持、吞咽代偿、运动交互、护理康复等数十项刚性需求,但国内适配产品供给严重不足,高端设备依赖进口、价格高昂,基层患者可及性极低,终末期患者的核心需求长期处于空白状态;
产业端,罕见病患者样本分散、病程数据稀缺、临床试验入组难,导致器械研发缺乏核心数据支撑,企业研发投入回报不确定性高,多数企业不愿入局,产品迭代缓慢;
注册端,行业缺乏成熟的临床评价体系与审评标准,企业对罕见病器械注册的政策红利把握不足,申报路径不清晰,大量创新技术卡在注册环节,无法转化为上市产品惠及患者。
蔡磊团队的持续攻坚,打破了这一恶性循环,为行业发展筑牢了底层根基:以 2 万 + 注册患者的 “渐愈互助之家” 平台为核心,建成全球最大的渐冻症民间科研大数据平台与病理基因样本库,破解罕见病研发 “患者分散、数据缺失” 的痛点;以亲身临床验证为抓手,完成可穿戴人工喉、眼控交互系统等创新器械的首例患者试用,具象化全周期临床需求,为企业研发明确了方向;以持续的行业发声与政策推动为支撑,让监管层对 ALS 器械的临床迫切性形成深度认知,推动罕见病医疗器械注册的政策红利持续落地,真正实现了 “临床需求 - 技术研发 - 临床验证 - 注册转化” 的产业闭环,为整个赛道的爆发扫清了核心障碍。

二、市场红利:全周期刚性需求全面爆发,政策支付双轮驱动,赛道迎来确定性高增长
本次行业变革的最终落脚点,是清晰可见的市场增量与确定性的商业机遇,从政策顶层设计到终端患者需求,全维度释放重磅利好,为械企入局提供了坚实的市场底盘。
1.刚性需求底盘筑牢,全链条市场空间广阔
ALS 患者从确诊到终末期,形成了覆盖诊断、治疗、护理、代偿四大环节的全生命周期器械需求,无任何一款产品可覆盖全周期需求,细分赛道空白点极多。2025 年中国 ALS 治疗行业市场规模已达 50 亿元人民币,预计将以 12.5% 的年均复合增长率持续扩张,到 2030 年将突破 150 亿元,其中康复辅助、生命支持、交互代偿类医疗器械市场增速持续领跑,连续三年保持两位数增长,成为整个神经科器械赛道的新增长极。
2.政策红利持续释放,注册上市通道全面提速
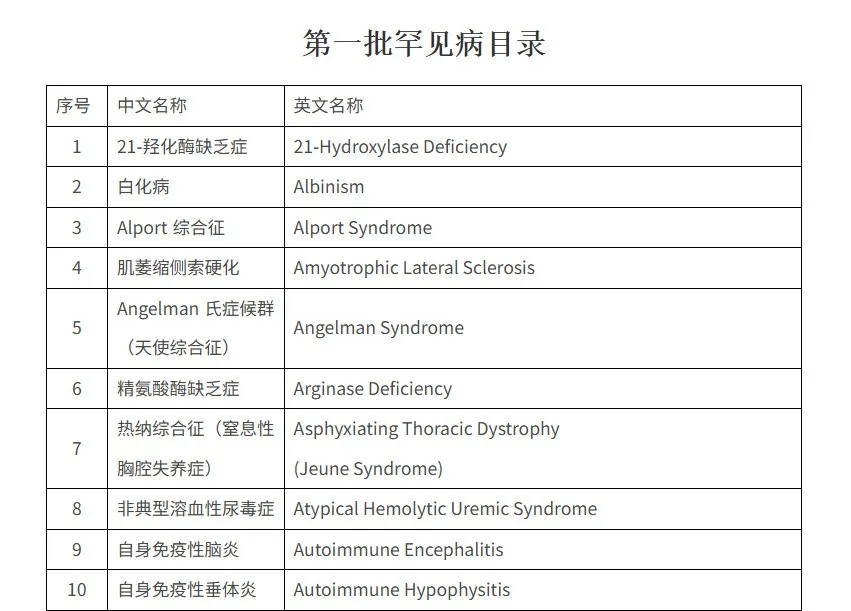
渐冻症,全称为肌萎缩侧索硬化。已正式纳入《中国罕见病目录》。《
3.支付体系持续完善,市场规模化效应加速显现
随着蔡磊团队的持续推动,ALS 相关医疗器械的患者可及性大幅提升,支付端迎来突破性进展:无创呼吸机等核心生命支持设备已逐步纳入全国多省市医保与惠民保报销范围,患者自费比例大幅下降;通过 C2M 反向定制模式,适配 ALS 患者的专用护理器械成本最高降低 80%,市场渗透率快速提升。支付端的完善,彻底打破了罕见病器械 “小众高价、市场规模有限” 的行业魔咒,让产品上市后可快速实现规模化放量,为械企入局提供了稳定的商业回报预期。
三、注册壁垒:全流程门槛持续升级,专业合规成产品拿证的核心生命线
赛道红利清晰可见,但与之对应的,是 ALS 相关医疗器械注册的全流程门槛持续升级,监管体系从 “粗放准入” 迈向 “全周期精准治理”,彻底改变了以往 “重准入、轻管理” 的行业格局。对于械企而言,政策红利不等于自动享受,市场机遇不等于能落地变现,注册环节的专业壁垒,已成为横亘在研发与上市之间的最大鸿沟。
1.临床评价核心难题仍在,方案设计决定注册成败
罕见病器械注册的核心门槛,始终是临床评价数据的合规性与充分性。尽管蔡磊团队搭建了规模化的患者队列,解决了入组难的基础问题,但 ALS 患者病程异质性强、临床终点选择难度大、传统随机对照试验(RCT)难以实施,对临床方案设计提出了极高的专业要求。真实世界数据如何合规应用、临床终点如何匹配审评要求、样本量如何科学论证,都需要对罕见病器械审评规则有深度理解,多数企业自行设计的方案,往往因科学性不足被审评驳回,导致临床试验推倒重来,不仅拉长上市周期,更造成研发成本的巨额浪费。
2.创新器械审评标准空白,前置沟通能力成关键
脑机接口、智能人工喉、AI 护理机器人等 ALS 核心创新器械,属于医疗器械监管的新兴领域,国内尚无成熟的注册技术审查指导原则,审评尺度与合规要求存在极强的个案特殊性。此类产品的注册申报,不仅需要完成严苛的非临床验证与风险管控,更需要在研发早期与器审中心完成多轮前置沟通,确认产品的临床价值、创新属性与注册路径。多数企业缺乏与监管部门的沟通经验,无法精准把握审评尺度,往往出现 “研发完成才发现不符合创新要求”“申报资料反复补正仍无法通过” 的困境,错失市场黄金窗口期。
3.全周期监管趋严,合规瑕疵可导致全盘失效
本次监管体系的核心变革,是构建了 “研发 - 临床 - 注册 - 上市 - 延续” 的全流程强监管体系。对于附条件批准上市的产品,注册证中明确载明上市后研究要求,延续注册时需提交完整的研究资料,未按要求完成的将直接不予延续;同时,医保、卫健、药监三部门协同发力,注册申报资料与临床数据、生产体系全程溯源,任何一个环节的合规瑕疵,都可能导致注册申请被驳回,甚至面临核查不通过、注册证撤销的风险。对于多数缺乏罕见病器械注册经验的企业而言,很难实现全流程的合规管控,一处细节疏漏,就可能导致前期千万级研发投入打水漂。
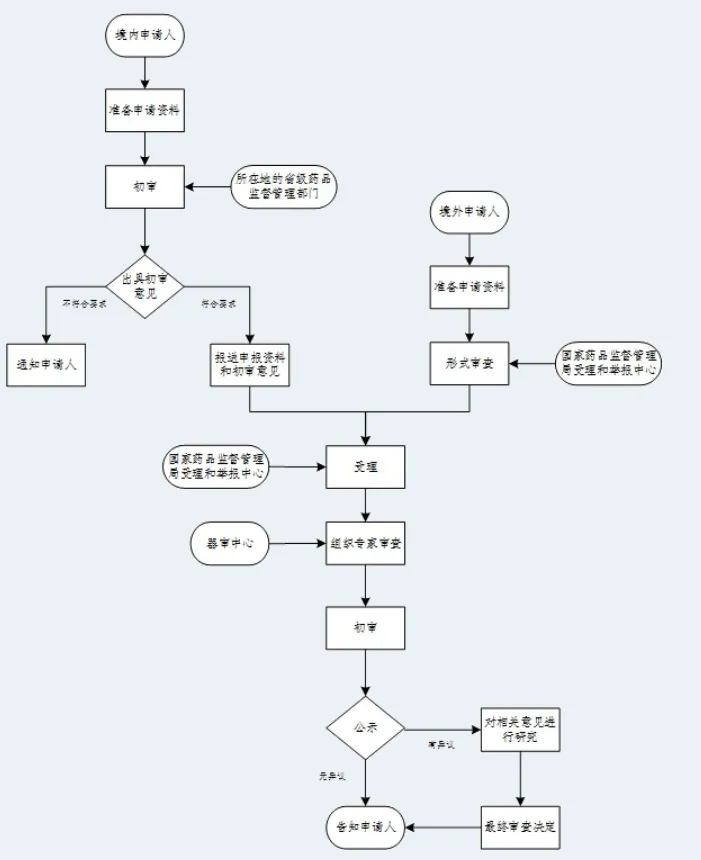
4.政策红利落地门槛极高,路径规划需前置布局
创新通道、优先审批、临床试验减免等政策红利,并非符合基本条件即可自动享受,需要企业提交充分的论证资料,完成多轮审评沟通,才能最终获批。以创新医疗器械特别审查为例,企业不仅需要证明产品 “国内首创、国际领先”,更需要论证产品 “具有显著临床价值”,仅临床价值的论证材料,就需要结合 ALS 疾病特点、现有诊疗短板、产品核心优势形成完整的证据链。多数企业有优质的技术与产品,却因不熟悉申报规则、不会编制论证材料,无法享受政策红利,审评周期较专业规划的产品拉长 1-2 年,彻底丧失市场先发优势。

四、行业机遇:赛道进入黄金窗口期,专业注册代办成医疗器械企业突围核心抓手
随着市场需求全面激活、政策红利持续落地,ALS 医疗器械赛道已正式进入洗牌升级期,入局者数量快速增长,但最终能抢占市场、实现商业变现的,必然是提前完成注册全路径规划、守住合规底线的企业。对于广大械企而言,这既是百年难遇的行业机遇,更是对注册合规能力的全面大考,唯有借力专业力量,才能在新一轮行业格局中站稳脚跟。
1.赛道分化加速,专业能力决定市场位次
当前,ALS 医疗器械赛道已从 “无人问津” 的冷门领域,转变为资本与企业争相布局的黄金赛道,大量拥有核心技术的创新企业、传统械企纷纷入局。但行业的核心矛盾,已从 “有没有产品” 转变为 “能不能快速拿证上市”。同类产品,早 6 个月拿证,就能抢占 70% 以上的市场份额;而注册路径不清晰、反复补正驳回的企业,即便技术领先,也只能错失市场先机。能否精准把握注册规则、实现产品快速获批,已成为企业在赛道中突围的核心竞争力。
2.专业代办前置规划,最大化释放政策红利
我们作为深耕医疗器械注册领域多年的专业代办机构,拥有罕见病医疗器械全链条注册服务经验,深度熟悉 CMDE 对 ALS 相关器械的审评尺度与规则,可在企业研发早期就全面介入,为产品量身定制最优注册路径:精准判断产品是否符合创新医疗器械特别审查、优先审批的申报要求,提前完成创新属性与临床价值的证据链搭建;通过专属通道完成与器审中心的前置沟通,提前确认临床评价路径与审评要求,避免研发走弯路;全程跟进申报全流程,确保资料一次性通过受理,最大化利用政策红利,将产品审评周期缩短 30% 以上,助力企业抢占市场先发优势。
3.全流程风险管控,彻底规避注册陷阱
针对 ALS 相关器械注册的核心难点,我们建立了全流程的合规管控体系,从研发阶段的设计输入与风险分析,到临床方案的科学设计与受试者招募对接,再到注册资料的标准化编制、审评沟通补正、注册核查全程应对,以及上市后变更、延续注册的全周期服务,实现全环节风险前置排查,规避 90% 以上的常见注册陷阱。熟悉临床试验减免、附条件批准的申报要点,能精准解决注册过程中的各类疑难问题,确保企业研发投入顺利转化为上市许可,避免因合规问题造成巨额损失。
4.一站式全链条服务,让企业专注核心研发
罕见病医疗器械注册,涉及研发、临床、审评、核查、生产等多个环节,需要对接监管部门、临床试验机构、检测机构等多个主体,流程繁琐、专业性极强。我们提供一站式全链条代办服务,全流程跟进所有注册相关事宜,企业无需组建专门的注册团队,无需分散精力应对复杂的注册流程,只需专注于产品技术研发与生产优化,真正实现 “省心、省力、省时、省钱”,以最低的成本、最快的速度完成产品上市。
五、未来展望:以专业赋能创新 共赴 ALS 器械行业黄金新征程
蔡磊的抗冻之路,不仅点燃了千万渐冻症患者的生命希望,更开启了中国罕见病医疗器械产业发展的全新时代。从临床需求的具象化,到科研基建的搭建,再到政策红利的落地,蔡磊团队用七年时间,为 ALS 医疗器械赛道扫清了发展的核心障碍,让这个曾经的小众赛道,迎来了确定性的爆发式增长。
随着 “健康中国” 战略持续深化,罕见病医疗器械的政策支持体系将持续完善,患者需求将持续释放,技术创新将持续突破,未来 3-5 年,将是 ALS 医疗器械赛道发展的黄金窗口期,也是医疗器械企业布局入局的最佳时机。而医疗器械注册的专业能力,始终是产品从实验室走向市场的核心桥梁,更是企业抢占赛道先机的生命线。
我们始终以 “赋能器械创新,守护患者健康” 为初心,以深耕行业的专业经验、对罕见病器械审评规则的深度理解、全流程的合规管控能力,助力每一家有技术、有情怀的械企,打通产品从研发到上市的最后一公里。我们不仅是医疗器械注册的代办方,更是企业布局罕见病赛道的全程合作伙伴,与企业一同把握行业黄金机遇,让更多国产创新 ALS 器械快速获批上市,既实现企业的商业价值,也为千万渐冻症患者撑起更可靠、更温暖的健康保护伞,为中国罕见病医疗器械产业的高质量发展,持续贡献专业力量。
