
在肺癌的系统治疗实践中,耐药早已不再是一个新问题。无论是靶向治疗还是免疫治疗,临床医生都已习惯于在治疗进展后寻找新的突变位点、通路替代或联合方案。然而,越来越多研究提示,一个反复出现却长期被低估的事实正在显现:在不少患者中,治疗失败并非源于肿瘤细胞本身发生了决定性的分子改变,而是肿瘤所处的微环境已经不再允许治疗发挥作用。

图源:CMT
这一现象在多种治疗场景中反复出现——驱动突变仍然存在,靶向药物仍可抑制其通路;免疫检查点依旧被阻断,但肿瘤却持续进展。耐药不再呈现为单一突变事件,而更像是一个由免疫抑制、代谢重编程、基质屏障和血管异常共同构成的系统性失效过程。
正是在这样的背景下,一篇发表于International Journal of Oncology的综述系统梳理了肺癌肿瘤微环境(TME)在治疗耐药中的核心作用,并进一步讨论了其潜在的干预方向。与其将TME视为“耐药发生后的背景因素”,作者更倾向于一个更具挑战性的判断:如果耐药是由微环境主导的结果,那么干预逻辑本身就需要从“针对肿瘤细胞”转向“重塑肿瘤生态”。
耐药从“突变事件”走向“系统失效”长期以来,耐药主要被理解为肿瘤细胞内在演化的结果,包括获得性突变、旁路信号通路激活或表观遗传改变。这一框架在解释EGFR-TKI或ALK-TKI耐药时具有重要价值,但该综述指出,它已不足以覆盖当前临床中观察到的全部现象。在不少病例中,肿瘤细胞在分子层面仍对原有治疗保持敏感性,但患者的疾病却在治疗过程中持续进展。这一现象提示,耐药并非完全由肿瘤细胞自治完成。
作者系统总结了多种肿瘤微环境相关机制对治疗结局的影响。免疫抑制性细胞群(包括肿瘤相关巨噬细胞、骨髓来源抑制细胞及调节性T细胞)通过分泌IL-10、TGF-β等因子持续抑制效应T细胞功能;肿瘤相关成纤维细胞通过重塑细胞外基质、分泌HGF等旁路激活因子,为肿瘤细胞提供“保护性环境”、抵抗治疗;异常血管结构和缺氧状态进一步放大免疫抑制和代谢失衡。这些因素相互作用,构成一个可以在不依赖新突变出现的情况下持续削弱治疗效果的系统。正因如此,随着探索的进展,学界逐渐认识到:肺癌耐药不仅是单一通路失效的表现,更是由肿瘤微环境主导的系统性结果。

图1: TME各组成部分如何协同促成耐药
靶向治疗耐药:问题不止发生在“靶点之后”在驱动基因阳性的肺癌中,靶向治疗曾被视为最直接、最具选择性的治疗模式。然而,该综述指出,肿瘤微环境在靶向治疗耐药中的作用长期被低估。即便在EGFR或ALK抑制治疗背景下,肿瘤相关成纤维细胞分泌的HGF、TGF-β,可在不改变肿瘤细胞基因组的情况下削弱药物效果,激活多条旁路信号通路。
更具挑战性的是,靶向治疗本身也可能反过来塑造更不利的微环境。长期通路抑制可诱导免疫抑制细胞浸润增加,或促进异常血管和上皮–间质转化(EMT)相关变化,从而为后续治疗失败创造条件。多细胞模型和类器官研究显示,在加入成纤维细胞和内皮细胞后,肿瘤对EGFR-TKI的耐药谱与单一肿瘤细胞模型存在显著差异。作者强调,靶向治疗耐药并不完全由肿瘤细胞内在改变所驱动,肿瘤微环境的持续演变可能在其中发挥重要作用。
免疫治疗失败:免疫并非“未被激活”,而是因微环境受阻在免疫治疗领域,临床上常用“免疫冷肿瘤”来解释疗效不佳,但该综述指出,这一概念在肺癌中往往过于简化。许多耐药病例并非缺乏免疫细胞,而是免疫细胞处于功能受限、空间隔离或代谢受抑的状态。T细胞可能存在于肿瘤周围,却被基质屏障阻隔;或在长期抗原刺激和慢性炎症环境中迅速耗竭,难以维持有效杀伤。
此外,“代谢竞争”被认为是免疫治疗失败的重要机制之一。肿瘤细胞在缺氧环境下强化糖酵解和脂质代谢,抢占关键营养物质,使浸润免疫细胞处于功能受限状态。多项研究显示,乳酸堆积、色氨酸代谢异常等改变均可通过促进免疫抑制细胞扩增、抑制效应T细胞功能,间接削弱PD-1/PD-L1抑制剂的疗效。这也解释了为何在多项临床研究中,单纯提高免疫检查点阻断强度,未能持续改善患者结局。
从问题走向解法:TME应作为肿瘤耐药的干预对象在系统梳理肿瘤微环境主导耐药的多重机制后,作者提出:如果耐药的本质是由微环境驱动的系统性失效,那么任何试图解决这一问题的策略,都必须超越单药升级的思路。作者反复强调,肿瘤微环境不应再被视为耐药发生后的被动背景,而应被视为与肿瘤细胞同等重要、且具有可干预性的治疗对象。
在这一框架下,作者将当前及在研的干预策略概括为以“组合干预”为核心的多条路径。首先,在免疫治疗领域,抗血管生成治疗被视为改善微环境的重要切入点。通过血管归一化,抗血管内皮生长因子(VEGF)治疗不仅有助于缓解缺氧状态,还可能改善免疫细胞向肿瘤内部的浸润条件,从而为免疫检查点抑制剂恢复效力创造基础。这一逻辑也为免疫治疗联合抗血管生成方案在多项研究中观察到的疗效提供了生物学解释。
其次,作者指出,表观遗传调控是连接肿瘤细胞与微环境的重要枢纽。HDAC或EZH2抑制剂等药物并非以直接杀伤肿瘤细胞为主要目标,而是通过调节染色质状态和转录程序,部分逆转由肿瘤或微环境驱动的免疫抑制状态。这类药物与靶免疫治疗联合使用,理论上有助于打破由TGF-β、EMT或免疫抑制细胞群主导的耐药状态。
在更具探索性的层面,综述也讨论了针对肿瘤相关成纤维细胞(CAF)和细胞外基质(ECM)的干预策略。通过削弱基质屏障、降低组织间压力或干扰CAF介导的旁路信号激活,这类策略有望改善药物在肿瘤中的分布和渗透,从而提升靶向药物或免疫治疗的有效性。
此外,作者对抗体偶联药物(ADC)和双特异性抗体在克服微环境相关耐药中的潜力也给予了关注。ADC通过抗体介导的靶向递送,提高肿瘤局部药物浓度,有可能在一定程度上绕过由异常血管和致密基质造成的药物不可达问题;而双特异性抗体,尤其是同时靶向免疫检查点与免疫抑制通路(如TGF-β)的分子,尝试在单一分子中实现对免疫抑制微环境的多重干预。
作者特别指出,当前这些策略之所以尚未形成明确的临床路径,一个重要原因在于肿瘤微环境的高度异质性尚未被充分刻画。因此,空间转录组、多组学整合等技术被视为未来将“经验性联合”转化为“机制导向联合”的关键工具。解决方案的终点,并非更多药物的叠加,而是在理解微环境差异的基础上,将合适的组合干预应用于真正可能获益的人群。
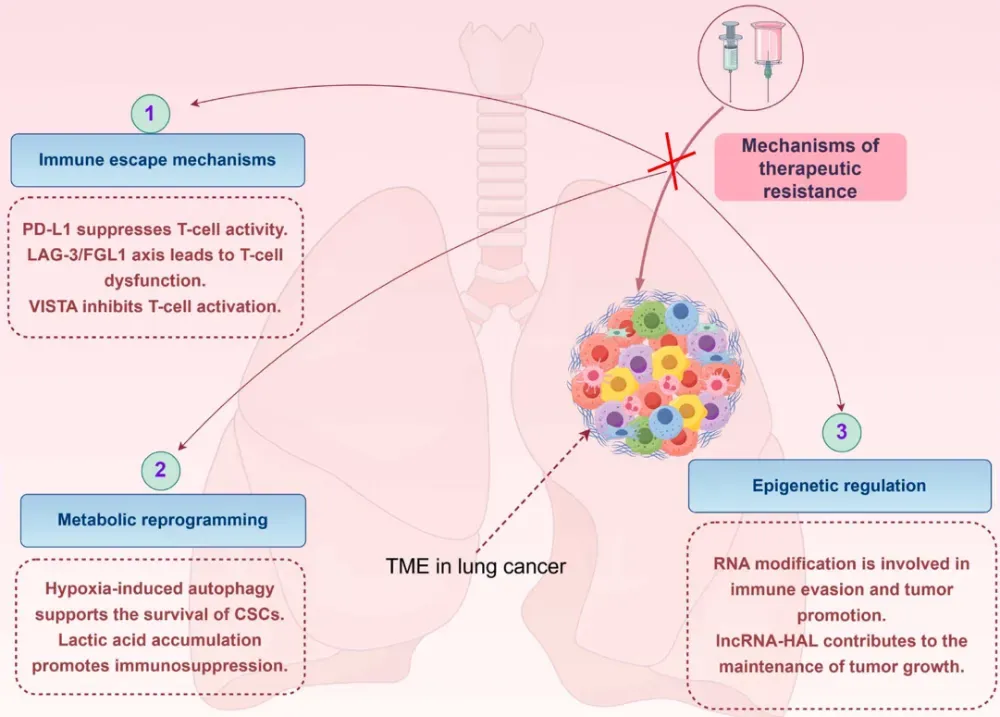
图2:基于肿瘤微环境的潜在干预策略框架
结语:当耐药被重新理解,干预逻辑也必须随之改变这篇综述表明,肺癌治疗耐药的核心挑战,正在从“找到下一个靶点”转向“理解治疗为何失效”。肿瘤微环境不再只是耐药发生后的被动结果,而是主动塑造治疗结局的重要决定因素。
在当前阶段,临床医生或许尚无法直接“治疗微环境”,但这一认识本身已经足以改变治疗思路:当标准治疗失效时,问题不一定出在药物选择,而可能出在治疗所处的生态系统。未来真正具有突破性的治疗策略,或许并非更强的单药,而是能够重塑微环境、恢复治疗可行性的组合干预方案。
文献参考
Liu L, Yang L, Li H, Shang T, Liu L. The tumor microenvironment in lung cancer: Heterogeneity, therapeuticresistanceand emerging treatment strategies (Review). Int J Oncol. 2026 Jan;68(1):11.doi: 10.3892/ijo.2025.5824
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:David Tian
审核:梨九
排版:白术
封面图源:CMT