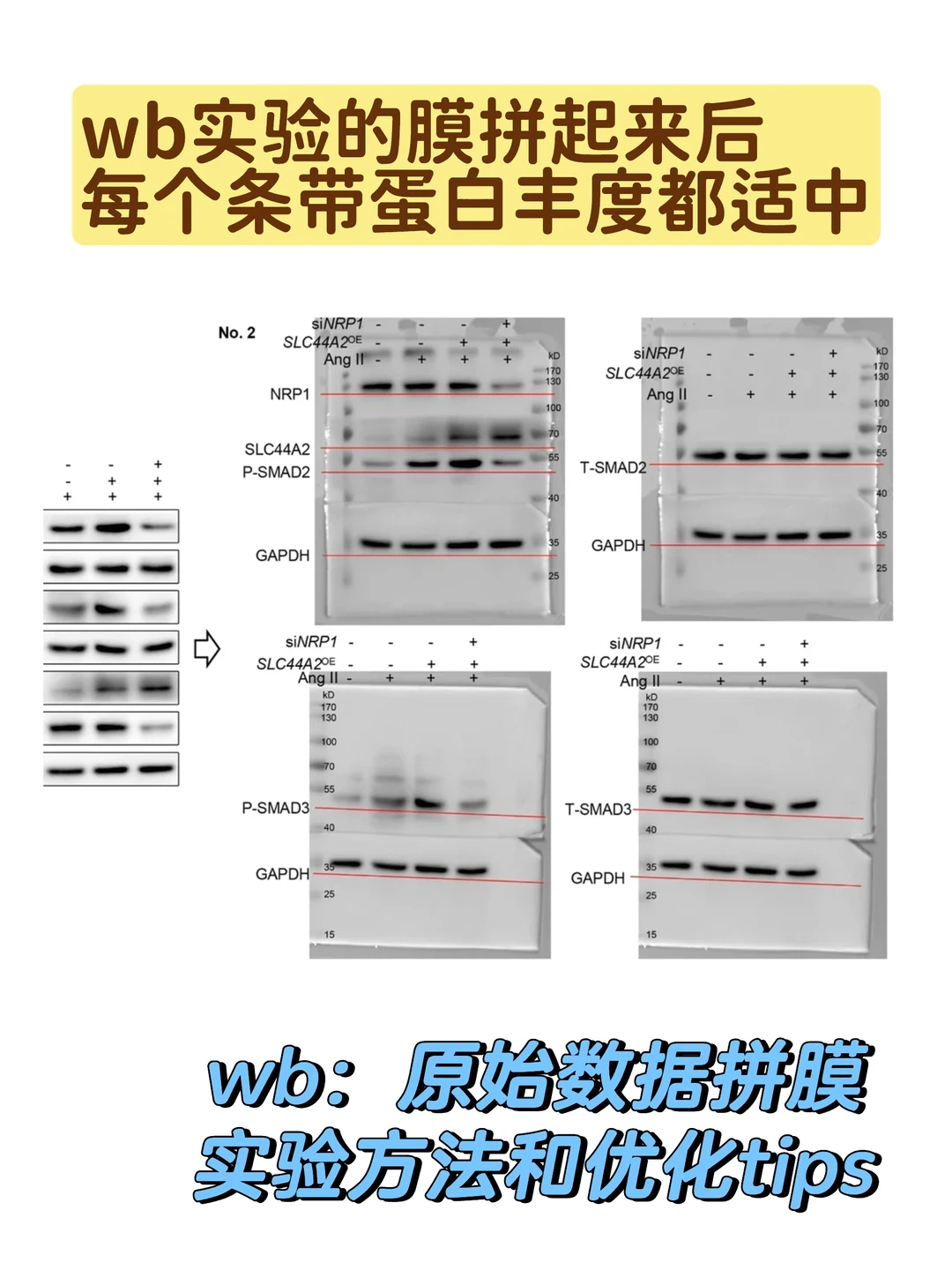
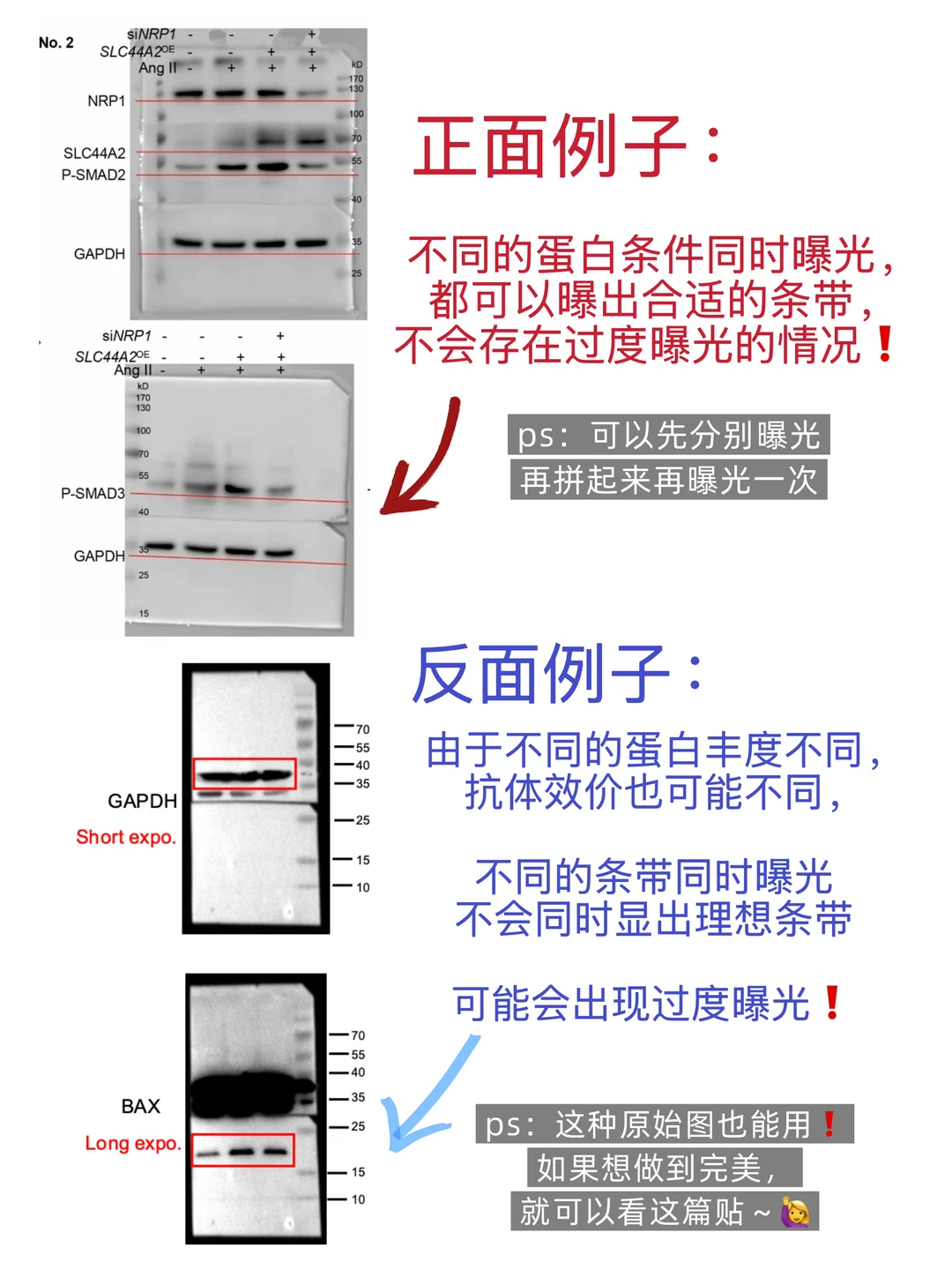
我的做法是:裁膜各自孵育一二抗,然后分开曝光,保存后拼在一起再同时曝光一次,也可以先在期刊上看看已经发表的杂志的原始数据是怎样的。
裁膜各自孵育没啥可说的,按正常操作即可;
[猪头R]但是把膜拼在一起同时曝光容易出现一个情况就是:第一张膜曝出后,另一张没显示信号,或者过曝黑一片,比如图2那样…
这是因为:蛋白丰度不同,或者一抗效价差距大,以及最后发光信号不一样。
遇到这种情况我们怎么操作可以得到图1的那种原始数据呢❓❓❓同时曝光,每个条带都可以显现出来!
因为所有目的蛋白和内参都是同一组样品,所以蛋白浓度是固定的,裁膜拼膜也不是跑平行胶。
解决方法只能从这两个步骤去下手:
[一R]检查一抗效价,调整稀释比例
比如内参蛋白本来细胞和组织内含量就高,一抗稀释比例再高,信号直接盖过所有。
内参一般为1:20000稀释,甚至可以1:40000,目的蛋白根据实际情况调整,一般为1:500~1:5000。蛋白丰度高就调高稀释比例,丰度低就降低!可以先做预实验去调整~
[二R]调整好一抗比例孵育后,第二个优化的点就是发光。
裁开的膜先分别曝光,用每个蛋白各自最合适的时间曝,这样曝出来的就很合适放到figure里,然后保存原始数据。
[三R]拼膜合并曝光时,把曝光时间差别很大的先放一边(这个第二步就可以看到),把曝光时间差不多的放在一起曝光。
信号差异太大的,我们根据曝光时间的差距调整发光液的使用!!!
[向右R]方法:目的蛋白用超敏发光液,内参蛋白或者某些丰度很高的目的蛋白用普通发光液,我们用的是普利莱的ECL超敏发光液P1010,好用
目的蛋白用原始浓度的超敏发光液涮膜,内参采用普通发光液涮膜,然后把膜拼在一起再同时发光,这样大概率可以同时显出~
🌟普利莱ECL化学发光检测试剂选择参照:
➡️常规检测可以使用超敏发光液P1050;
➡️对于表达量较高的目标蛋白例如内参,使用普通发光液P1010就可以;
➡️对于低丰度难检测的,比如磷酸化蛋白,用灵敏度最高的飞克级发光液P1060!
如果目标蛋白丰度适中,不太推荐使用飞克级ECL极敏发光液,容易产生过曝“烧膜”现象!