很多人以为 HIV 只在血液里,其实肠道才是它最大、最顽固的潜伏库。而且有一项足够硬核的研究,直接把 “肠子不同位置的细菌,怎么管着 HIV” 这件事,给分析的明明白白。
这篇是 2025 年 10 月发表在《The Journal of Infectious Diseases》上的研究,名字有点长:HIV Reservoir Dynamics and Bacteriome Composition Along the Gut Axis,中文可以理解成 ——肠道轴上的 HIV 储库动态变化与肠道菌群组成。
我知道你们最关心:这跟我有啥关系?
别急,我用大白话慢慢讲。
研究团队找了24 位 HIV 感染者,在去世后 6 小时内,快速取了十二指肠、空肠、回肠、结肠、直肠,一共 5 段肠道组织,加起来 113 份样本。
他们用了很精准的 ddPCR 技术,一边测HIV DNA(病毒库有多大),一边测HIV RNA(病毒活不活跃),再用16S rRNA测序分析菌群。数据量很大,但他们还做了多重校正——年龄、性别、CD4计数、病毒载量、抗生素使用史、肿瘤这些因素都考虑进去了。
先看菌群的基本盘。下图的热力图很直观:小肠和大肠的菌群,完全是两套班子。
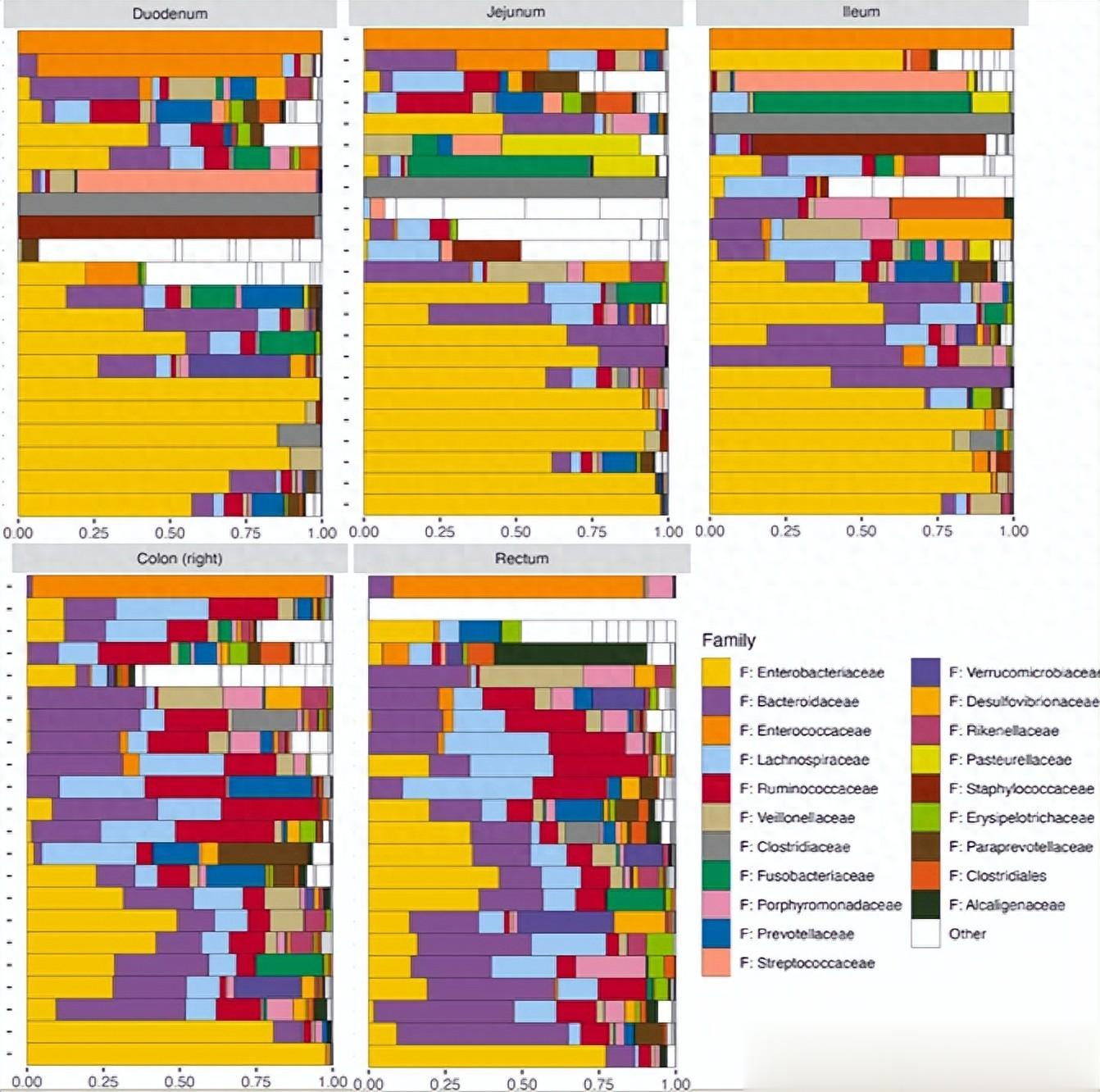
(图1)
小肠上段(十二指肠、空肠)主要是变形菌门的天下,到了下段回肠,厚壁菌门和拟杆菌门开始抬头。一进结肠,彻底变天——厚壁菌门和拟杆菌门成为绝对主角。这种空间分化非常显著,个体差异虽然存在,但整体的南北分界很清楚。

(图2)
图2用箱线图展示了α多样性(物种丰富度)的变化。结论也很干脆:大肠的菌群多样性显著高于小肠(P<0.001)。而且多样性从近端到远端是递增的——越往直肠走,菌群越"热闹"。
这里有个细节:结肠和直肠的物种数和均匀度最高,小肠各段相对"单调"。这跟我们的常识一致——大肠是发酵车间,菌群自然更复杂。
好了,重点来了。HIV DNA和RNA在各肠段怎么分布?

(图3)
图3的数据可能会让你意外:小肠的HIV DNA水平显著高于大肠。空肠是峰值,结肠和直肠反而更低。但注意,这是"总量"的概念——如果考虑到各肠段的细胞总量差异,实际感染比例可能另有说法。
更有意思的是转录活性。虽然小肠的HIV DNA多,但转录活性(RNA水平)在各肠段的差异并不完全跟DNA同步。十二指肠和回肠的转录活性"高于预期"——也就是说,DNA多,RNA也不少,病毒在小肠不仅住得多,还"话多"(活跃)。
研究者用线性模型校正了DNA总量后发现:HIV DNA和转录活性之间,并不是简单的线性关系。这意味着,某些肠段存在"转录调控"——同样的病毒DNA,在某些环境下更愿意"开口说话",在另一些环境下则选择"沉默"。

(图4)
图4的散点图进一步揭示了菌群和病毒的关系:
小肠:菌群多样性越高,HIV转录活性越强(正相关,ρ=0.32,P=0.015)大肠:菌群多样性越高,HIV转录活性越弱(负相关,ρ=-0.41,P=0.013)完全相反的调控方向。 小肠里,菌群越丰富,HIV越"嗨";大肠里,菌群越丰富,HIV越"蔫"。


(图5)
图 5用广义线性模型扒出了"嫌疑人"名单。结论分几点:
第一,关联具有高度节段特异性,没有哪种菌能在全肠道通吃。小肠和大肠的"游戏规则"完全不同。
第二,小肠里,多类菌群促进HIV转录。比如某些变形菌门的成员,在小肠环境下可能通过炎症信号或代谢物,唤醒了沉睡的病毒。
第三,大肠里,毛螺菌科等菌群抑制HIV DNA和转录。这些产短链脂肪酸(SCFA)的细菌,可能通过丁酸等代谢物,让细胞进入一种不利于病毒复制的状态。
第四,同一个菌属,在不同肠段可能发挥相反作用。比如某些梭菌属的成员,在小肠和大肠的表现截然不同。这说明环境上下文比菌种身份更重要。

(图6)
图6按功能分类(SCFA产生、胆汁酸代谢、黏蛋白降解、致病性、一过性定植)做了更系统的梳理。几个核心发现:SCFA/胆汁酸/黏蛋白相关菌:在大肠抑制HIV,在小肠促进HIV转录。一过性/污染菌群:无显著关联,说明结果不是"杂菌干扰"造成的假阳性。功能通路比单一菌种更重要:同一功能的菌群,往往有相似的作用。病毒库大小和转录活性是两个机制:有些菌能减少HIV DNA(缩小病毒库),但会增加RNA(激活转录);另一些则相反。
研究者总结了四个核心结论:
1. HIV病毒库沿肠道呈节段性分布 小肠(尤其空肠)的HIV DNA水平更高,大肠(结肠、直肠)更低。但十二指肠和回肠的转录活性"高于预期",说明小肠是病毒库的核心位点之一,而且病毒在这里更"活跃"。
2. 肠道菌群组成有显著的空间异质性 大肠菌群丰富度、多样性显著高于小肠,菌群组成在小肠与大肠间完全不同。
3. 菌群丰富度与HIV储库/激活的关系,随肠段不同而翻转 小肠:菌群越丰富,HIV转录活性越强。 大肠:菌群越丰富,HIV转录活性越弱。 这种"区域特异性"是这项研究最突出的发现。
4. 功能菌群在不同节段的作用具有特异性 短链脂肪酸(SCFA)产生菌、胆汁酸代谢菌、黏蛋白降解菌在大肠抑制HIV,但在小肠促进HIV转录。这意味着,如果想通过菌群干预来辅助HIV治疗,必须"精准定位"——不能一概而论。
目前研究显示,这些结论基于24例逝者样本,样本量不算大。而且都是横断面数据——我们只能看到"快照",看不到动态变化。另外,体外实验和动物模型还需要验证这些菌群-病毒的因果关系。研究者自己也提到,相关性不等于因果性,某些关联可能是HIV感染本身改变了菌群,而非菌群在主动调控病毒。
本文仅供科普,不构成诊疗建议。 如果你正在考虑益生菌、饮食调整或其他菌群干预手段,请务必咨询你的医生,不要自行尝试。
写在最后:一个值得你思考的问题读到这里,你可能已经意识到:你的肠道不是一个整体,而是一个"分段治理"的复杂生态系统。小肠和大肠的菌群,对HIV的态度截然相反。
那么,问题来了——
如果你的日常饮食、服用的药物、甚至情绪压力,主要影响的是大肠菌群(比如通过粪便检测看到的那些),但HIV的"活跃据点"其实在小肠——那么,我们现在常用的"调节肠道菌群"手段,比如益生菌、膳食纤维补充,真的作用在对的地方了吗?还是说,我们可能一直在"隔着大肠,猜小肠"?
这个问题,目前研究还没有答案。但它是这项研究留给我们每个人的思考:在追求"治愈"或"长期缓解"的路上,精准定位可能比"广撒网"更重要——不仅针对病毒,也针对我们赖以生存的菌群。
参考文献
[1] Yu G, et al. HIV Reservoir Dynamics and Bacteriome Composition Along the Gut Axis. The Journal of Infectious Diseases. 2025;232(4):e123-e135. doi:10.1093/infdis/jiaeXXX