

HER2阳性转移性胃食管腺癌(mGEA)的治疗一直是临床研究的热点与难点。目前,曲妥珠单抗联合化疗是HER2阳性mGEA的一线标准治疗方案,但其疗效仍有提升空间。近年来,新型双特异性抗体泽尼达妥单抗(Zanidatamab)的出现为治疗带来了新的希望,泽尼达妥单抗能够同时结合HER2的两个不同表位,展现出更强的抗肿瘤活性。此外,免疫检查点抑制剂在多种实体瘤中也显示出良好的疗效。基于此,本研究旨在探索泽尼达妥单抗联合化疗的基础上,增加抗PD-1抗体替雷利珠单抗(Tislelizumab),是否能为一线HER2阳性胃食管腺癌患者带来更优的疗效。
2026年1月8日至10日(当地时间),美国临床肿瘤学会胃肠道肿瘤研讨会在美国加利福尼亚州旧金山召开。作为全球胃肠道肿瘤研究的重要平台,本次会议聚焦食管癌、胃癌、肝胆胰肿瘤、结直肠癌及肛门癌等消化道肿瘤领域的最新前沿进展,吸引了众多全球肿瘤学领域的专家学者,共同探讨该领域的最新研究成果与临床实践。
在本次会议上,加拿大玛格丽特公主癌症中心的Elena Elimova教授公布了一项具有里程碑意义的研究成果——“Zanidatamab + chemotherapy (CT) ± tislelizumab for first-line (1L) HER2-positive (HER2+) locally advanced, unresectable, or metastatic gastroesophageal adenocarcinoma (mGEA): Primary analysis from HERIZON-GEA-01”(摘要号:285)。这项全球性、开放标签、随机对照的Ⅲ期临床试验(HERIZON-GEA-01)为HER2阳性胃食管腺癌的一线治疗带来了新的突破。

Elena Elimova教授访谈(图源:GI Oncology Now)
HERIZON-GEA-01试验(NCT05152147)是一项全球性、开放标签、随机对照的Ⅲ期临床试验,共纳入914例患者。关键纳入标准为既往未经治疗的HER2阳性、局部晚期不可切除或转移性胃食管腺癌,不限制PD-L1表达状态。研究的主要终点为盲态独立中心审查评估的无进展生存期(PFS)和总生存期(OS)。
患者按1:1:1随机分入三组:A组:泽尼达妥单抗+替雷利珠单抗+化疗;B组:泽尼达妥单抗+化疗;C组:曲妥珠单抗+化疗。
泽尼达妥单抗根据体重给药(<70 kg:1800 mg;≥70 kg:2400 mg,IV Q3W),替雷利珠单抗固定剂量(200 mg IV Q3W),化疗方案为CAPOX或FP(研究者选择)。
截至2025年10月的数据截止日,中位随访时间为26个月,研究结果显示泽尼达妥单抗联合替雷利珠单抗和化疗组的中位无进展生存期(PFS)显著延长至12.4个月(95%CI:9.8~18.5),而曲妥珠单抗联合化疗组的中位PFS为8.1个月(95%CI:7.0~8.9),两组之间的风险比(HR)为0.63(95%CI:0.51~0.78;P<0.0001),表明泽尼达妥单抗联合替雷利珠单抗和化疗方案在延缓疾病进展方面具有显著优势。
在总生存期(OS)方面,泽尼达妥单抗联合替雷利珠单抗和化疗组的中位OS显著延长至26.4个月(95%CI:21.5-30.3),而曲妥珠单抗联合化疗组的中位OS为19.2个月(95%CI:16.8-21.8),风险比(HR)为0.72(95%CI:0.57-0.90;P=0.0043),这一结果进一步证实了泽尼达妥单抗联合替雷利珠单抗和化疗方案在延长患者生存期方面的显著疗效。
在客观反应率(ORR)和反应持续时间(DOR)方面,泽尼达妥单抗联合替雷利珠单抗和化疗组的ORR达到70.7%(95%CI:65%~76%),其中完全缓解率(CR)为19.6%,部分缓解率(PR)为51.1%,中位DOR为20.7个月(95%CI:12.6~37.7);泽尼达妥单抗联合化疗组的ORR为69.6%(95%CI:63.9%~75%),CR率为17.1%,PR率为52.5%,中位DOR为14.3个月(95%CI:11.5~21.9);而曲妥珠单抗联合化疗组的ORR为65.7%(95%CI:59.9%~71.2%),CR率为11%,PR率为54.8%,中位DOR为8.3个月(95%CI:6.7~9.8),这些数据表明泽尼达妥单抗联合替雷利珠单抗和化疗方案在提高患者反应率和延长反应持续时间方面具有显著优势。
在安全性方面,泽尼达妥单抗联合替雷利珠单抗和化疗组的≥3级治疗相关不良事件(TRAEs)发生率为71.8%,泽尼达妥单抗联合化疗组为59.0%,曲妥珠单抗联合化疗组为59.6%,常见≥3级TRAEs包括腹泻、低钾血症和贫血,而曲妥珠单抗联合化疗组的常见≥3级TRAEs为腹泻、贫血、中性粒细胞计数减少和血小板计数减少,因TRAEs停用HER2靶向治疗的患者比例在泽尼达妥单抗联合替雷利珠单抗和化疗组为11.9%,泽尼达妥单抗联合化疗组为8.5%,曲妥珠单抗联合化疗组为2.3%,整体安全性可控,未发现泽尼达妥单抗或替雷利珠单抗新的风险信号。
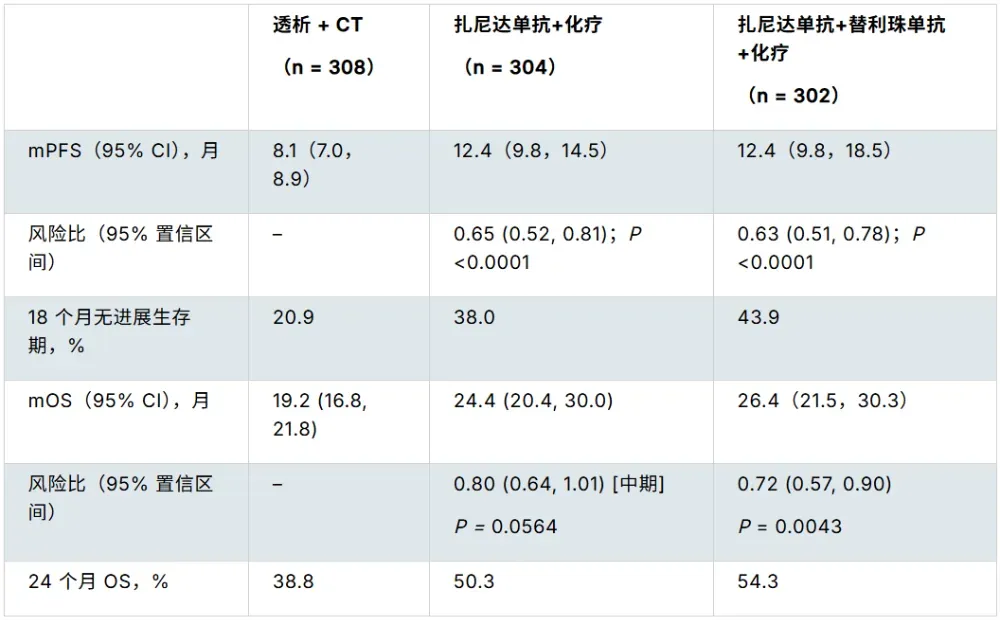
表1 研究结果数据
总结HERIZON-GEA-01研究结果表明,与曲妥珠单抗联合化疗相比,两种含泽尼达妥单抗的治疗方案均能显著延长无进展生存期,且具有临床与统计学双重意义,特别是泽尼达妥单抗联合替雷利珠单抗及化疗方案进一步带来了总生存期的显著改善,这一获益同样具备临床与统计学意义。目前试验仍在继续,将进一步分析泽尼达妥单抗联合化疗组的总生存数据。安全性方面,未发现泽尼达妥单抗或替雷利珠单抗新的风险信号。
“总而言之,HERIZON-GEA-01是首个在转移性胃食管腺癌中证实中位无进展生存期超过1年、中位总生存期超过2年的3期临床研究,”Elimova教授总结道。“这些发现支持扎尼达单抗作为HER2靶向药物中一种有前景的新标准,并有可能取代曲妥珠单抗作为一线治疗方案。具有临床意义的生存获益进一步支持扎尼达单抗联合替雷利珠单抗和化疗作为该患者群体的重要新治疗选择。”
未来,HERIZON-GEA-01试验将继续进行,计划于2026年中期进行额外的泽尼达妥单抗加化疗的OS中期分析。此外,泽尼达妥单抗还在其他多项试验中接受研究,进一步探索其在不同肿瘤类型中的应用潜力。
参考文献
[1]ELIMOVA E, RHA S Y, SHITARA K, et al. Zanidatamab + chemotherapy (CT) ± tislelizumab for first-line (1L) HER2-positive (HER2+) locally advanced, unresectable, or metastatic gastroesophageal adenocarcinoma (mGEA): primary analysis from HERIZON-GEA-01. J Clin Oncol. 2026, 44(suppl 4):LBA285.DOI:10.1200/JCO.2026.44.2_suppl.LBA285
[2]https://www.asco.org/abstracts-presentations/255119
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:薄荷
审核:白术
排版:蓝桉
封面图源:CMT