你是否曾经历过这样的困惑:胚胎评分很好,内膜厚度达标,甚至血流都很不错,可移植后,优质的胚胎却像一颗沉默的种子,始终没有生根发芽。
医生可能将原因归结为胚胎潜力或内膜容受性,可明明这些在目前技术看都是好的,为什么就是没成功呢?
如果再继续追问,那只能是运气不好,或者缘分未到了。
我们常把移植比作播种,但或许,它更像异常需要精准对接的太空对接——
胚胎这艘飞船必须与子宫内膜这个空间站成功完成信号识别、姿态调整和牢固连接,任何一步出错都可能导致失败。
然而,这个过程我们从未亲眼见过。
刚刚,一项来自陈子江院士团队的重磅研究,首次为我们揭开了胚胎着床这个黑箱的内部景象。

研究者首次成功构建了一个微型人造子宫,让人类早期胚胎在其中与活体子宫内膜组织共同发育,并首次全程观测并记录了长达14天的母胎对话。
这对试管婴儿意味着什么呢?这意味着反复移植失败的原因,可能被精准定位到这场对话的某个具体步骤。
这更意味着,未来试管婴儿技术有望从依赖概率和运气的盲投,走向基于分子对话的精准匹配,让每一次移植都不再只是拼运气。
接下来,让我们深入这项突破性原因,看看研究者如何实现这一观测,以及他将如何改变我们的求子之路。
01目前研究的困境与探索过去,研究者成功在实验室里,把人类胚胎培养到着床阶段,这让我们得以看到种子自身是怎么开始发芽、分化的。
这时候的问题是,没有土壤,我们不知道它们之间是如何对话的。
后来研究者用干细胞在培养皿里造出很像早期胚胎的结构(学术用语是胚胎样结构),来研究胚胎发育规律。
这避免了使用真正的胚胎,是重大突破,但问题是它仍然是孤零零的种子,没有土壤环境。
接着有研究者把真正的胚胎和子宫内膜细胞放在同一个培养皿里(二维共培养),就像让种子和土壤在一个平面上挨着。
这样能观察到一些基础交流,但问题是,子宫内膜是立体的、有复杂的结构,而不是这种简单挨着的方式,无法模拟真实情况。
所以核心困境就是缺少一个能真实再现立体土壤与真实种子在着床初期进行全方位、立体互动的研究系统。
为了解决这个问题,研究者开发了两个关键工具。
一个是迷你子宫内膜,它不是真正的器官,而是用人类子宫内膜细胞在实验室培养出来的一个微型3D组织团。
它像一颗肉丸子,但内部结构(各种上皮细胞、基质细胞)和功能都高度模拟了真实的、处于容受性的子宫内膜。
它就像一个为实验量身定做的、活体的、立体的土壤模型。
另一个是3D共培养系统,研究者不再让胚胎在平面上挨着细胞,而是将真正的人类胚胎,小心翼翼地放到这个3D迷你子宫内膜旁边或表面,让它们在一个立体的空间里一起生长和互动。
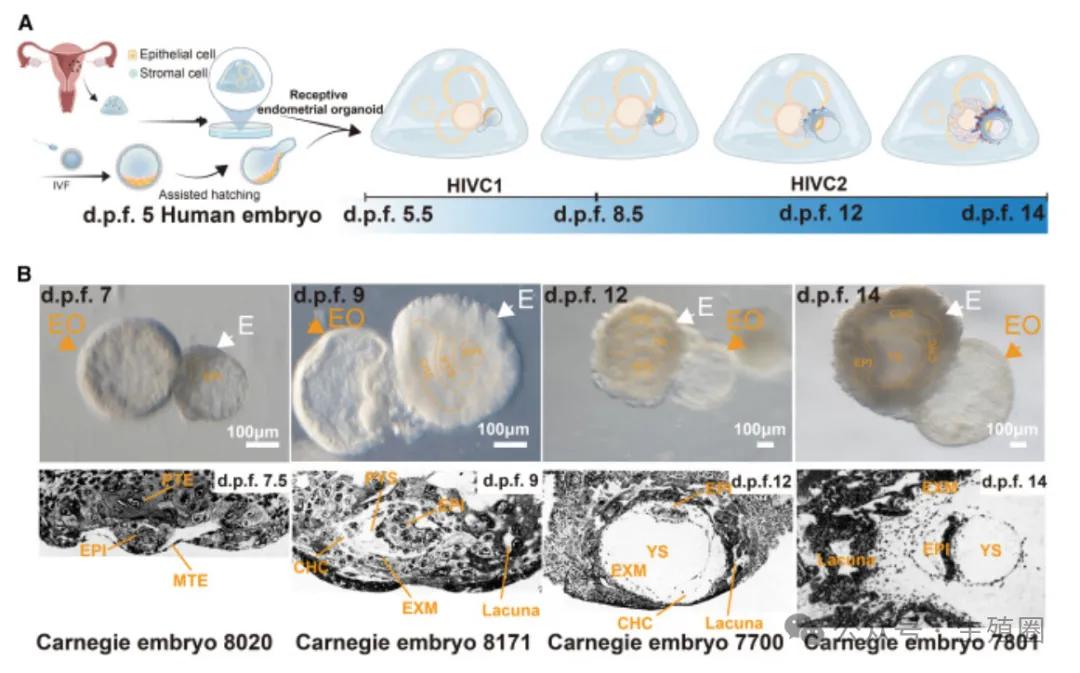
(图A:3D培养模型共培养平台示意图,B:白色箭头是囊胚黄色箭头是子宫内膜)
这样胚胎可以直接接触到、并向器官(土壤)发出化学信号,类器官也会回应。从而可以直接看出着床是如何开始的。
它为我们打开了一个前所未有的窗口,去亲眼目睹人类生命最初、最隐秘的登陆与握手的过程。
02研究的重大发现研究者使用了经过知情同意、捐赠的体外受精第五天的人类囊胚。
用干细胞技术在培养皿里长出一个迷你、立体、有活力的子宫内膜组织(子宫内膜类器官).
然后,他们把囊胚轻轻放在这团“土壤”旁边,给它们提供最接近母体的营养,并用最先进的显微镜连续拍摄了14天。
结果令人震撼,在这个模拟的微型子宫里,胚胎不仅活了下来,而且以近乎完美的方式,重现了在妈妈肚子里最初的发育步骤。
在有“土壤”的环境里,胚胎发育到第14天的存活率高达75%,而在传统的、只有营养液的孤独环境里这个数字只有37.5%;
第14天的胚胎直径达到约700微米,和自然怀孕同阶段的宝宝大小几乎一模一样,远远超过在实验室培养皿孤独长大的胚胎;
在共培养过程中,羊膜腔、卵黄囊这些标志性的早期结构都如期形成。
这说明,子宫内膜不仅是“一张床”,更是一个必需的、活跃的“孵化器”,这更说明仅仅形态达标、血流达标可能远远是不够的。
03母胎对话到底是怎样的?研究最震撼的发现是,胚胎和内膜之间,进行着一场我们之前想象不到的精密对话。
关键发现一:内膜是教练,指导胚胎长出胎盘
胚胎外层的细胞(以后会变成胎盘)里,有一群先锋部队,叫绒毛外滋养细胞,它们的任务就是像树根一样,扎进内膜,建立连接。
在只有营养液的培养皿中,这群先锋部队行动缓慢。
但是,在有内膜的环境里,内膜会主动发出化学信号,命令并训练这些先锋部队提前3天装备好挖掘工具,加速成熟,准备扎根。
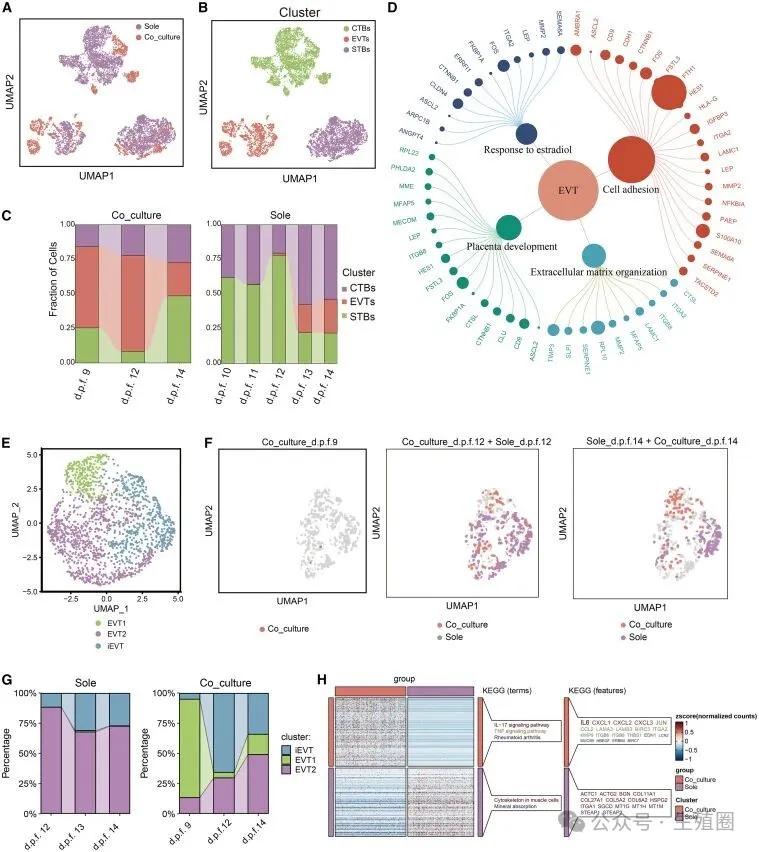
这意味着你的内膜质量,直接决定了胚胎的胎盘细胞能否正常发育和侵入,内膜不好,再好的胚胎也可能无用武之地。
关键发现二:hcg不是报喜信使,而是开门钥匙
我们都知道,怀孕后用试纸测到的就是hcg,但它的作用远比报喜更重要。
研究发现,胚胎一进入子宫,就开始分泌hcg。但是这个hcg不是用来让我们验孕的,而是胚胎递送给内膜的一把生化钥匙。
内膜上有一把对应的“锁”(受体LHCGR,也就是hcg受体),只有当钥匙插进锁眼,转动之后,内膜才会启动容受程序,改变自身结构,接受胚胎。
最直接的证据是,当研究者在试验中用药物“堵住”内膜上的这把锁,没有一个胚胎能够粘上去(粘附率0%),所有胚胎的发育都停止了。
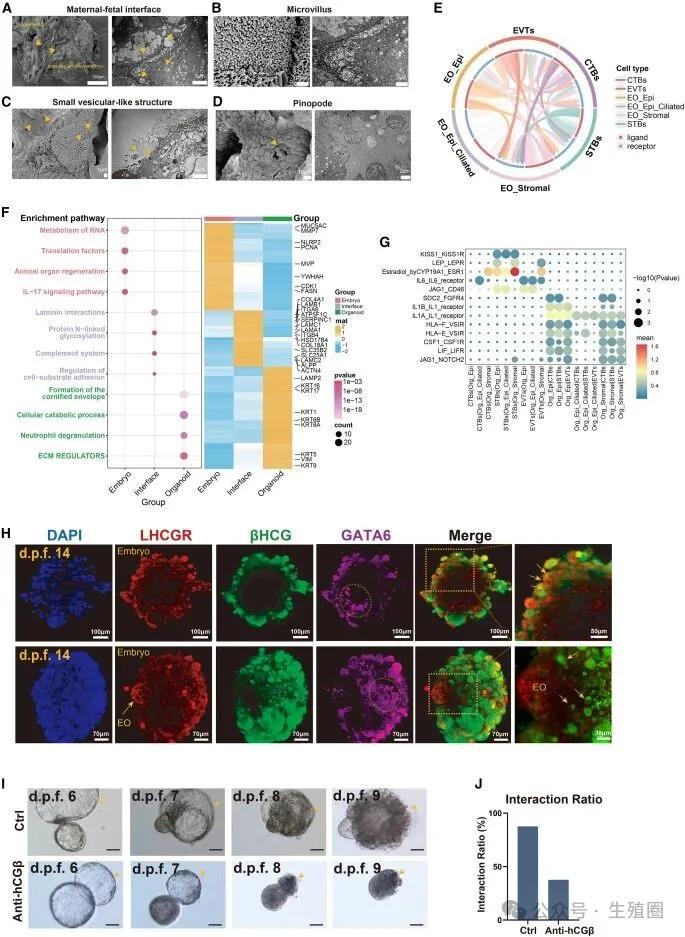
这给我们的启示是,反复种植失败,会不会是胚胎这把钥匙(hcg)不给力?亦或者是内膜这把“锁”反应迟钝?
这为检测和治疗提供了全新的、精准的思路。
圈姐说,所以胚胎移植前进行hcg宫腔灌注,移植后进行hcg的补充有助于胚胎着床是有科学证据的,只是我们之前的研究并没有发现这样的机制。
04这个研究如何改变试管未来大家看了这个研究,可能很难想明白这对试管婴儿到底意味着什么,这个研究虽然在试验室,但它为我们的临床治疗描绘了激动人心的未来蓝图。
未来,你正式移植前可能会做一次着床能力测试。
想象一下,在您正式移植前的一个月,医生可能会取一点您的内膜细胞,在体外培养成一块您个人的、活的内膜模型。
同样,将您通过PGT筛查过的胚胎(或具有相同遗传特征的胚胎模型),与这块个人内膜放在一起共培养几天。
这时候,医生可以观察,它们粘的好不好,对话信号强不强,胚胎的先锋部队进展是不是顺利。
这就像一次移植彩排,直接预测哪个胚胎与您当月的内膜最合拍,从而选择成功率最高的那个进行移植,告别用身体一次次试错的痛苦。
未来,失败原因将能被精准诊断
反复种植失败,可能不再是一个模糊的筐,而是可以被细分为:
胚胎信号问题型(hcg分泌或信号通路异常);
内膜接收问题型(受体表达或反应不佳);
胚胎响应问题型(收到内膜信号后,内部发育程序卡顿)。
每一种类型,都可能对应不同的干预方案,实现精准保胎。
未来,药物干预将有的放矢
通过这个研究,我们知道了hcg信号通路是如此关键的总开关,那么未来是否有企业就能研发出专门增强或模拟这一通路的药物。
这可以在移植前后进行精准的着床支持治疗,而不是像现在一样使用较为笼统的激素支持。
其实,现在知道后,也可以使用hcg在移植前进行宫腔灌注,移植后进行hcg注射进行着床支持,只不过之前没有相关研究支持这样的做法,现在算是有了理论支撑。
当然,最后这一点是圈姐自己的理解,姐妹们可以和医生一起就这一点进行探讨,为自己胚胎顺利着床助力。

亲爱的姐妹们,我知道试管这条路充满艰辛和未知,但你看,科学正在以前所未有的速度,照亮我们曾经完全黑暗的领域。
这项研究告诉我们,每一次失败,都可能是一次精密的生化对话出了细微的差错,而这些差错,正在变得可观察、可测量,未来更可能被纠正。
它让我们看到,试管婴儿技术正从一场依赖形态和经验开盲盒的旅程,迈向了一个可以预览、预演、精准匹配的新时代。
请照顾好彼此,你们所经历的,正推动者科学向前迈进一大步,而科学终将回馈给你们更清晰的道路和更温暖的希望。
最后,祝愿您的胚胎宝宝和内膜的握手,坚实有力,一次成功马上上岸,加油!
全文完!现在流量为王的年代,围观也是一份力量,转发就是一份担当,希望动动您发财的小手,给我点个赞,如果您能转发到微信群或朋友圈,就会让更多孕育困难的小家庭受益,谢谢您!
郑重声明
本账号发表的内容仅作为科普分享,不对所引用文献的准确性和完整性作出任何承诺和保证,亦不承担因该内容已过时、所引用资料可能的不准确或不完整等情况引起的任何责任,请相关各方在采用或者以此作为决策依据时另行核查。本账号不做任何形式的营销推广,在采取任何预防或治疗措施前,请与你的医疗保健提供者沟通。
不传小道消息和谣言
不做只为转发量而存在的公众号
永远在意真实数据和文献论证
抱娃路上,我愿意陪你一起走过最无助的岁月
——THE END——
参考文献
3D post-implantation co-culture of human embryo and endometrium. Cell Stem Cell. 2026 Jan 8;33(1):58-72.e7. doi: 10.1016/j.stem.2025.12.002. Epub 2025 Dec 23.