编者按:慢性乙型肝炎(CHB)的临床治愈是全球肝病领域关注的焦点,传统单一抗病毒治疗难以实现HBsAg清除,探索联合治疗策略成为突破方向。在第五届肝病创新大会上,人畜共患传染病重症诊治全国重点实验室主任、华中科技大学同济医学院附属同济医院宁琴教授在主题报告中,系统阐述了其团队在“病毒抑制+免疫调节”多靶点联合治疗领域的系列研究成果,并介绍了《慢性乙型肝炎临床治愈治疗航线图专家共识2.0》的核心更新要点。
 “病毒抑制+免疫调节”是实现慢乙肝临床治愈的关键策略
“病毒抑制+免疫调节”是实现慢乙肝临床治愈的关键策略慢性乙型肝炎的临床治愈即功能性治愈,定义为抗病毒治疗结束后24周,持续的血清HBsAg消失和血清HBV DNA检测不到,伴或不伴抗-HBs血清学转换。实现这一目标的关键在于同时实现病毒的深度抑制和宿主免疫的有效修复。单一核苷酸类似物治疗虽能有效抑制病毒复制,但HBsAg清除率极低;而聚乙二醇干扰素虽具有免疫调节作用,但在病毒载量高的患者中疗效受限。因此,“病毒抑制+免疫调节”的联合策略成为实现临床治愈的重要方向。
慢乙肝临床治愈探索:OSST里程碑等系列研究基于肝内cccDNA持续存在、HBV感染免疫耐受和免疫耗竭等慢乙肝发病特征和机制,在缺乏靶向cccDNA药物的现状下,宁琴教授团队提出了深度抑制病毒基础上协同免疫调节恢复宿主抗病毒免疫应答,是慢乙肝临床治愈策略的重要研究方向。团队依托国家传染病防治科技重大专项,联合全国50余家同行单位成立中国治愈肝炎联盟CCVHC,成功实施了慢乙肝临床治愈OCEAN海洋计划,围绕打破免疫耐受,集成现有NAs、IFN和其他免疫调节剂的作用机制和优势特征,建立了旨在打破免疫耐受、重塑免疫功能的慢乙肝临床治愈新方案的系列临床研究,包括全国多中心前瞻性随机对照研究OSST、Endeavor和Anchor研究等,率先实现了有限疗程内CHB临床治愈零的突破,并逐步优化提升CHB患者HBsAg阴转率至30%。
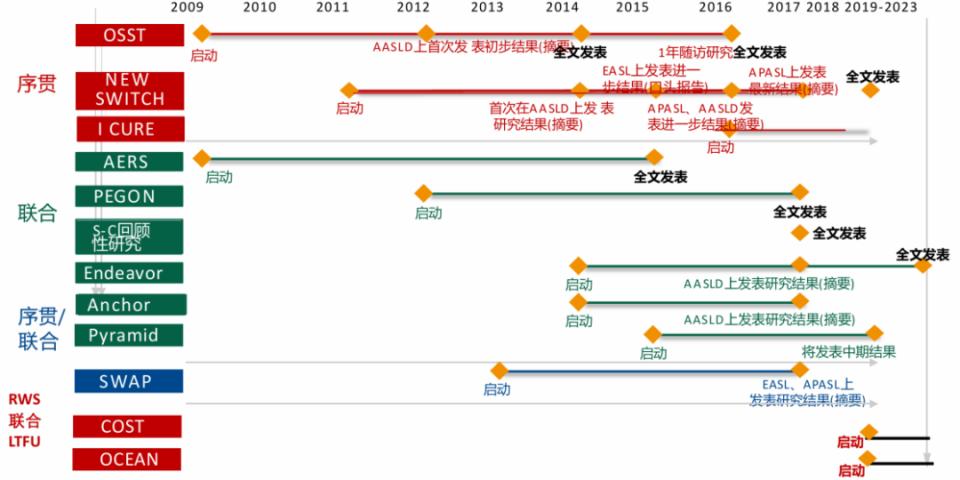
图1. 慢乙肝临床治愈探索:OSST里程碑等系列研究
(引自讲者会议幻灯)
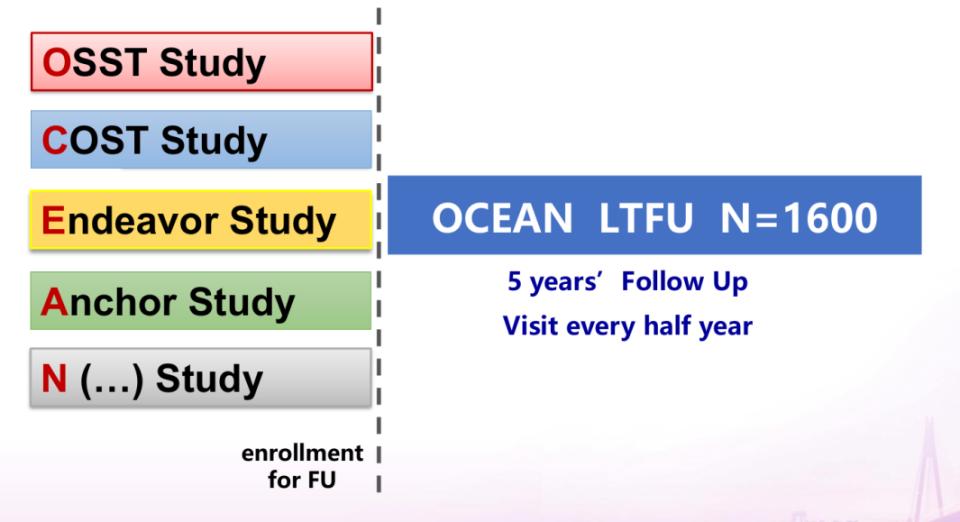
图2. OCEAN研究体系
(引自讲者会议幻灯)
其中,宁琴/吴迪教授团队发起的Anchor研究近期在Hepatology International发表[1]。ANCHOR研究是一项评估Peg-IFNα-2b、恩替卡韦及粒细胞-巨噬细胞集落刺激因子联合治疗慢乙肝疗效的随机对照试验。研究纳入年龄18-65岁、慢性乙型肝炎、入组前接受核苷(酸)类似物(NA)治疗至少1年、HBV DNA≤1000 copies/mL且HBsAg<3000 IU/mL的患者。患者按1:1:1比例随机分为三组,分别接受恩替卡韦(ETV)单药治疗96周(E组);或接受Peg-IFNα-2b联合ETV治疗48周,随后48周Peg-IFNα-2b单药治疗(EP组);或接受Peg-IFNα-2b+ETV+GM-CSF(75 μg,QD,连续5天,每月一次)联合治疗48周,随后48周Peg-IFNα-2b单药治疗(EPG组)。所有患者随访24周,仅E组患者在随访期间继续ETV治疗。主要疗效指标为96周时HBsAg清除率。
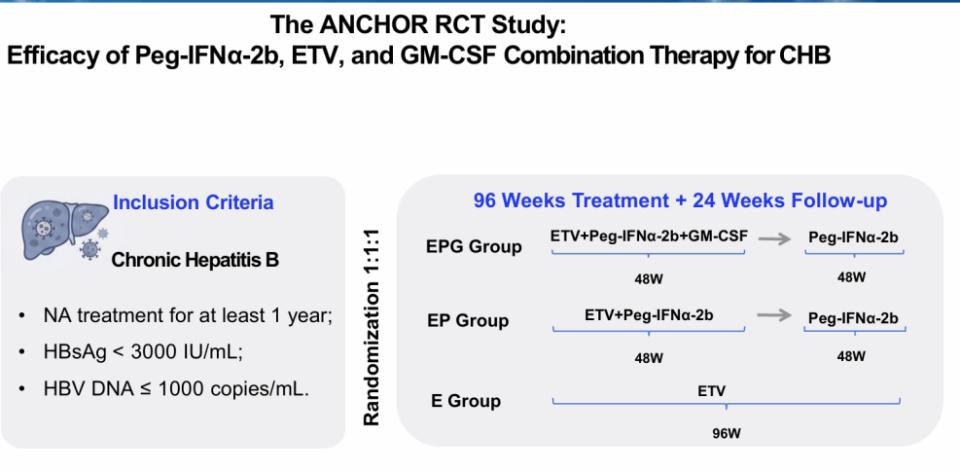
图3. Anchor研究:研究设计
(引自讲者会议幻灯)
结果显示,恩替卡韦联合Peg-IFN治疗组的HBsAg清除率显著高于恩替卡韦单药组,联合治疗组可实现30%的HBsAg清除率,且停药后24周的持久率达88%。而额外加入GM-CSF未能进一步显著提高HBsAg清除率。HBsAg清除的关键预测因素包括年龄较轻、基线HBsAg水平较低,以及治疗24周时HBsAg和HBV RNA的快速下降。Anchor研究为NA经治HBsAg<3000 IU/mL这一更广泛人群的临床治愈策略提供了高级别循证医学证据,在这一患者群体中加用Peg-IFN的策略可显著促进功能性治愈,为联合治疗提供了重要证据。
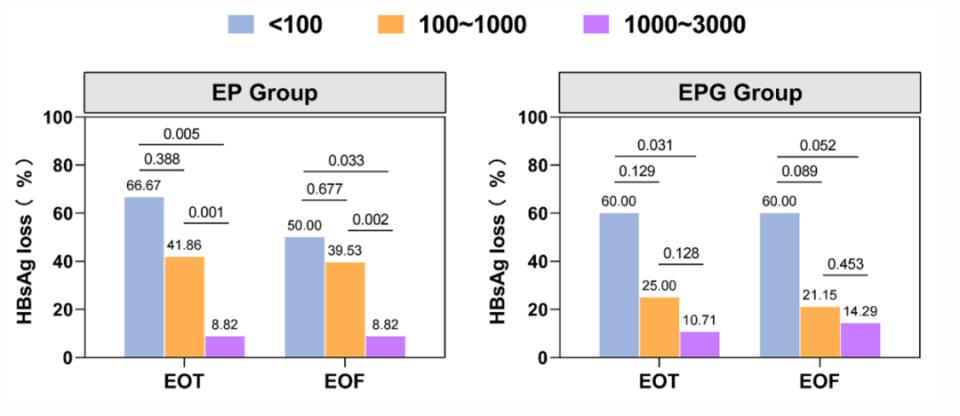
图4.多靶点联合策略显著提高临床治愈率
(引自讲者会议幻灯)
在系列随机对照研究基础上,团队开展了全国多中心前瞻性真实世界COST研究。COST研究旨在对临床治愈新方案进行大样本医院内患者人群推广和验证,初步分析结果显示,治疗48周干扰素联合治疗组HBsAg阴转率由NA单药组的0.80%提高至25.70%,干扰素停药后24周HBsAg阴转率由NA单药组的2.00%提高至35.20%,治疗过程中联合治疗组较单药组相比HBsAg水平显著下降。中期分析显示,联合组较单药治疗组48周HBsAg阴转率显著增高(27.6% vs. 0.5%)。COST研究患者完成疗程后将全部转入OCEAN随访研究。
创建慢乙肝临床治愈疗效预测模型为临床早期制定、及时调整个体化治疗策略提供参考。宁琴教授团队依托规范化CHB临床治愈队列开展病毒/免疫学应答模式研究,创建了CHB临床治愈疗效预测模型。团队研究发现,干扰素治疗结束时,HBcrAg<4 log10 U/mL和抗-HBs>2 log10 IU/L(即HBVCure-crAb模型),反映了较低的肝内cccDNA水平、更稳定的HBV特异性CD8+T淋巴细胞比例,以及持续的滤泡辅助性T细胞和B细胞免疫应答[2]。该模型可用于预测聚乙二醇干扰素治疗后哪些CHB患者可能实现持久的功能性治愈。
此外,基于系列研究数据,团队还创建了用于基线预测临床治愈的BGT模型、用于治疗中预测临床治愈的RGT模型等,并绘制了治疗路线图,为临床医生在不同治疗阶段调整方案提供了可视化指导工具。该路线图明确了不同基线特征患者的治疗路径和疗效监测节点,推动了个体化治疗策略的实施。
创新方案的关键卡点与突破尽管多靶点联合策略取得显著进展,但仍面临关键卡点。核苷经治、病毒抑制的慢乙肝患者联合序贯Peg-IFN治疗可以显著提高临床治愈率。然而,HBV整合与干扰素治疗后HBsAg阴转的关系仍不明确。2025年,韩梅芳、宁琴教授团队的一项研究[3]发现,对于NA经治患者,基线HBV整合位点数大于28是制约其通过Peg-IFN治疗达到临床治愈的不利因素;慢乙肝病程时长、ALT水平与HBV整合水平呈正相关。研究表明,核苷经治、病毒抑制的慢乙肝患者基线时肝组织的整合位点数量与Peg-IFN治疗后能否获得HBsAg阴转相关。这一发现从病毒学角度揭示了部分患者对干扰素应答不佳的内在机制。
同时,宁琴教授团队研究发现,免疫应答修复不足可介导IFN序贯治疗中的病毒学突破,外周/肝脏单核/巨噬细胞TLR2低表达和CD8+T细胞PD-1表达升高是序贯IFN治疗过程中病毒学突破的关键免疫学机制,提示在联合治疗中需要关注免疫功能的全面修复[4]。
宁琴教授团队开展的Ⅱ期RCT探索性研究(OCEAN cure05 研究)显示,免疫调节三联治疗(NAs、TQA3334和TQB2450)具有良好的安全性及耐受性,能使病毒抑制的慢乙肝经治患者产生更为显著且持久的HBsAg下降;能更好地促进特异性CTL功能修复;且在三药治疗组,高剂量TQA3334可促进HBsAg的下降。该研究入选第33届亚太肝脏研究学会年会(APASL 2024)口头报告。
ASO的探索用于慢性乙型肝炎治疗的反义寡核苷酸(ASO)类在研乙肝新药也取得了相应突破。
B-Together研究[5]评估了Bepirovirsen治疗12/24周后序贯Peg-IFN治疗24周,停药随访24周的HBsAg清除率。研究纳入NA经治、HBV DNA<90 IU/mL、HBsAg>100 IU/mL的患者,主要终点为序贯治疗结束后第24周获得HBsAg和HBV DNA<LLOQ的患者比例。结果显示,与BPV单药治疗相比,BPV序贯Peg-IFN治疗可改善治疗结束后的应答,这可能是由Peg-IFN预防BPV应答者复发所驱动;研究期间未观察到新的安全性信号。
另一项研究汇总分析了119例基线HBeAg阴性、HBsAg 100-3000 IU/mL的NA经治患者,接受AHB-137 300 mg或225 mg治疗24周[6]。研究认为,在HBeAg阴性的慢乙肝受试者中,AHB-137治疗在结束24周后实现了显著且持续的抗病毒应答(包括CR和PR),其中24周300 mg方案的应答率最高。对于接受24周300 mg AHB-137治疗的受试者,26.6%在第48周达到持续完全应答(CR),且不同基线HBsAg水平的应答率具有可比性(≤1000 IU/mL: 28.9%;>1000 IU/mL: 23.1%)。其中,71%的完全应答者获得抗-HBs≥10 IU/L。部分应答(PR;HBsAg≥0.05至<10 IU/mL且HBV DNA<10 IU/mL)在29.7%的受试者中实现。疗效在不同基线HBsAg水平间一致。AHB-137耐受性良好,治疗后24周未观察到新的安全性信号。这些结果支持AHB-137在慢乙肝功能性治愈方面的持续开发。
《慢性乙型肝炎临床治愈治疗航线图专家共识2.0》更新要点在系列研究证据基础上,《慢性乙型肝炎临床治愈治疗航线图专家共识2.0》于2025年完成更新[7],旨在助力实现WHO 2030年消除病毒性肝炎的目标。共识2.0版明确了慢乙肝临床治愈的定义,即抗病毒治疗结束后24周持续的血清HBsAg消失和HBV DNA检测不到,伴或不伴抗-HBs血清学转换。对于NA经治患者的序贯联合干扰素治疗,推荐采用干扰素加药联合等策略以提高临床治愈率。对于实现HBsAg阴转的患者,推荐巩固治疗至少12周或诱导抗-HBs产生的治疗方案以提高持续应答率。对于接受NA长期治疗的HBeAg阴性、HBsAg低水平(<100 IU/mL)无肝硬化患者,尽管NA停药可诱导部分患者实现HBsAg阴转,但停药策略需谨慎制定,同时停药后需密切监测。
共识2.0引入了多种新型DAAs和免疫调节剂,如siRNA、ASO、CpAMs、bulevirtide、NAP等,并讨论了其在实现临床治愈中的潜力。特别关注了特殊人群,如低病毒血症患者、MASLD患者、肝硬化患者、HCC患者的治疗策略,为这些复杂情况提出更具体的指导。共识强调了即使实现HBsAg阴转后,仍需定期监测HBV再激活、HCC等肝病事件,以确保患者的长期健康。同时,新型HBV生物标志物如HBcrAg、HBV RNA和HBcAb等在预测治疗反应和疾病结局中的作用得到讨论,为临床医师提供了更全面的监测工具。
中文版慢性乙型肝炎功能性治愈治疗航线图专家共识2.0正在推进中。共识2.0的制定汇聚了国内顶尖专家的智慧,于2025年1月启动,经过多次研讨会,计划于2026年正式发布。共识将基于GRADE分级系统,对证据等级(高质量A、中等质量B、低质量C)和推荐强度(强推荐1、弱推荐2)进行明确标注。
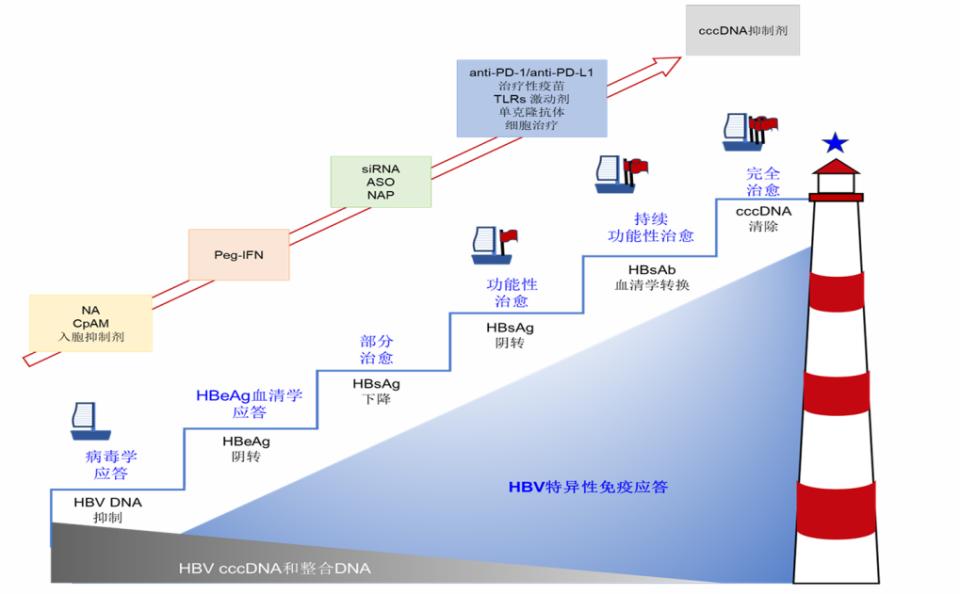
图5. 中文版慢性乙型肝炎功能性治愈治疗航线图
(引自讲者会议幻灯)
总结与展望现有证据充分表明,免疫修复是实现持续应答的关键,“病毒/抗原抑制+免疫调节”的多靶点联合策略是实现慢乙肝临床治愈的重要路径。现有联合方案在优势/优选人群中可获得30%左右的临床治愈率。未来,探索多靶点联合新方案,提高优势人群、非优势人群及特殊人群的临床治愈率仍任重道远。依托全重实验室/国家重大公共卫生事件医学中心及转化医学大楼等平台,我国慢乙肝临床治愈研究将持续深入,为实现WHO 2030年消除病毒性肝炎的目标贡献力量。
参考文献:
1.Wu D, Huang D, Peng S, et al. Efficacy and safety of entecavir, peginterferon alfa-2b and GM-CSF combination therapy: the anchor randomized controlled trial[J]. Hepatol Int. 2026, 20(1):31-45.
2.Huang D, Wu D, Luo XP, Yan WM, Ning Q et al. J Hepotol. 2022
3.Gu MS, Wu D, Han MF, Ning Q et al. Aliment Pharmacol Ther. 2025
4.Huang D, Yan WM, Wu D, Ning Q et al. Antiviral Research. 2021
5.Buti M, et al. J Hepatol. 2024
6.Niu et al. AASLD 2025. Poster 5022.
7.Wu, et al. Update on the Treatment Navigation for Functional Cure of Chronic Hepatitis B: expert consensus 2.0. Clin Mol Hepatol, 2025