前言
介入治疗是一门新兴的临床学科,是微创医学的重要组成部分,独立于临床传统内科学和外科学之外的第三大临床学科。介入治疗在不开刀暴露病灶的情况下,借助先进的影像设备(如DSA、B超、CT等)在皮肤上作直径几毫米的微小通道,将特殊的穿刺针、导管等插到病变器官、组织,通过穿刺针或导管直接注入药物、栓塞剂或置入支架等方式对多种疾病进行治疗。为给广大同道提供肝病介入治疗的前沿进展,《国际肝病》携手四川大学华西医院罗薛峰副教授共同创办“国际肝病-介愈肝胆”栏目,每月定时分享介入领域的最新研究,传达规范治疗理念,追踪介入治疗的最新动态,以期对相关领域专家、研究人员及一线医务工作者的研究或工作有所裨益。
重要研究结果分析及其临床意义研究背景肝硬化心肌病(CCM)是一种由肝硬化继发的特异性心脏功能与结构异常的临床综合征。其核心特征包括应激下收缩反应减弱、心室舒张功能受损(即舒张功能障碍,DD)以及电生理异常。2005年世界胃肠病学大会(WCG)提出了基于传统超声参数的DD诊断标准。随着心血管影像学的发展,2019年肝硬化心肌病联盟(CCC)更新了诊断标准,该标准纳入了更多反映心脏舒张和收缩功能的指标。然而,两种标准的临床效能都缺乏外部验证。
经颈静脉肝内门体分流术(TIPS)通过建立肝内门腔分流道降低门静脉压力,能有效控制肝硬化患者的门脉高压并发症,尤其是难治性腹水和食管胃底静脉曲张出血。但其会增加心脏前负荷,对已有潜在心肌病的患者构成挑战。因此,术前的心脏功能评估对患者的选择至关重要。
Liver International杂志于2025年11月在线发表了一篇题为《舒张功能障碍不同诊断标准对TIPS患者的临床意义》的文章。该文章通过单中心回顾性队列研究,旨在比较新旧诊断标准下DD的检出率,并评估其对TIPS术后心血管及肝脏相关结局的预测价值。
研究设计本研究为一项单中心回顾性队列研究,纳入了2014年1月至2022年12月期间在意大利米兰Niguarda大都会医院接受TIPS治疗的肝硬化患者。研究严格筛选人群:纳入经实验室指标和影像学特征确诊的肝硬化患者。排除标准包括:血管性疾病、非恶性非肝硬化门静脉血栓、已接受肝移植、原发性心脏疾病、缺乏心脏功能评估数据等。最终共纳入184例患者(图1)。
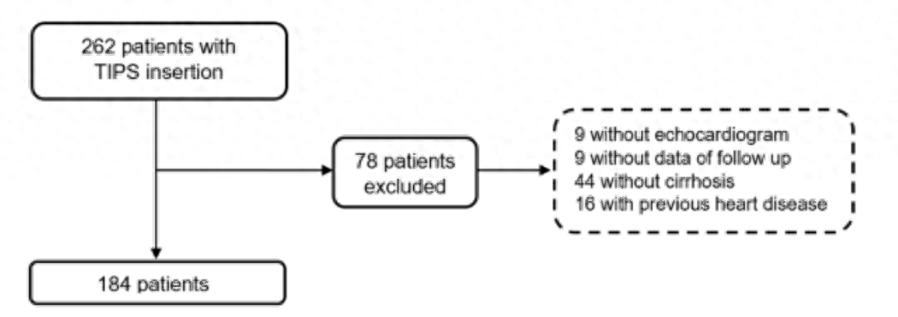
图1.研究人群流程图
研究的核心变量是舒张功能障碍(DD),分别依据2005年WCG标准(满足以下指标之一即可诊断DD:减速时间>200ms;等容舒张时间>80 ms;或E/A<1)和2019年修订后的CCC标准(满足以下≥3项即可诊断为DD:室间隔e′速度<7 cm/s(或侧壁e′速度<10 cm/s);E/e′比值≥15;左心房容积指数>34 mL/m2,或三尖瓣反流速度>2.8 m/s。分级定义:DD Ⅰ级:满足≥3项+充盈压正常+E/A≤0.8;DD Ⅱ级:满足≥1项+充盈压升高+0.8<E/A<2.0;DD Ⅲ级:满足≥1项+充盈压升高+E/A≥2.0)进行诊断,并通过流程图(图2)对DD患者进行分类。
主要结局指标为术后6个月内的复合终点事件,包括:(1)主要不良心血管事件(MACE),包括心力衰竭、心房颤动、冠心病或卒中;(2)肝脏相关事件,包括腹水复发、肝性脑病(HE)发作、术后再出血、无肝移植生存期;(3)死亡或肝移植(LT)的复合终点。
研究还收集了详细的基线人口学、临床数据、超声心动图、NT-proBNP和右心导管检查结果。数据分析采用单因素和多因素回归模型(包括Fine & Gray竞争风险模型和Cox回归),以确定各结局的独立预测因子。
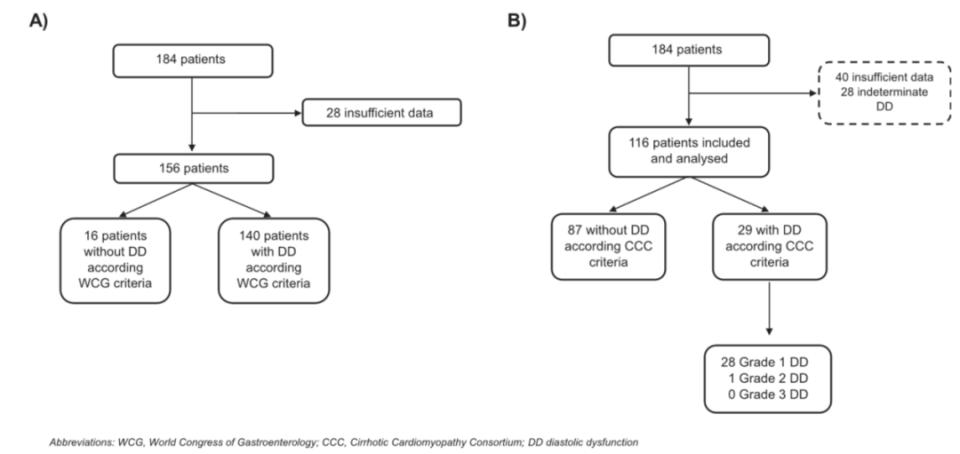
图2.根据WCG标准(A)和CCC标准(B)对DD患者进行分类的流程图
研究结果01
患者基线特征
研究共纳入184例接受TIPS的肝硬化患者,男性占71%,中位年龄56岁。TIPS指征包括难治性腹水(78例,42%)、门静脉血栓(76例,41%)和反复食管胃底静脉曲张出血(73例,40%)。近一半的患者正在接受非选择性β受体阻滞剂(NSBB)治疗(102例,55%),129例(70%)正在使用利尿剂。TIPS术前的中位门静脉压力梯度为18.1 mmHg,术后为9.5 mmHg。术前肝功能以Child-Pugh B级为主(57%),MELD评分中位数为11(表1)。术前超声心动图显示左室射血分数(EF)保留(中位63%),NT-proBNP水平轻度升高(中位140 pg/mL)(表2)。
表1. 研究人群的一般特征
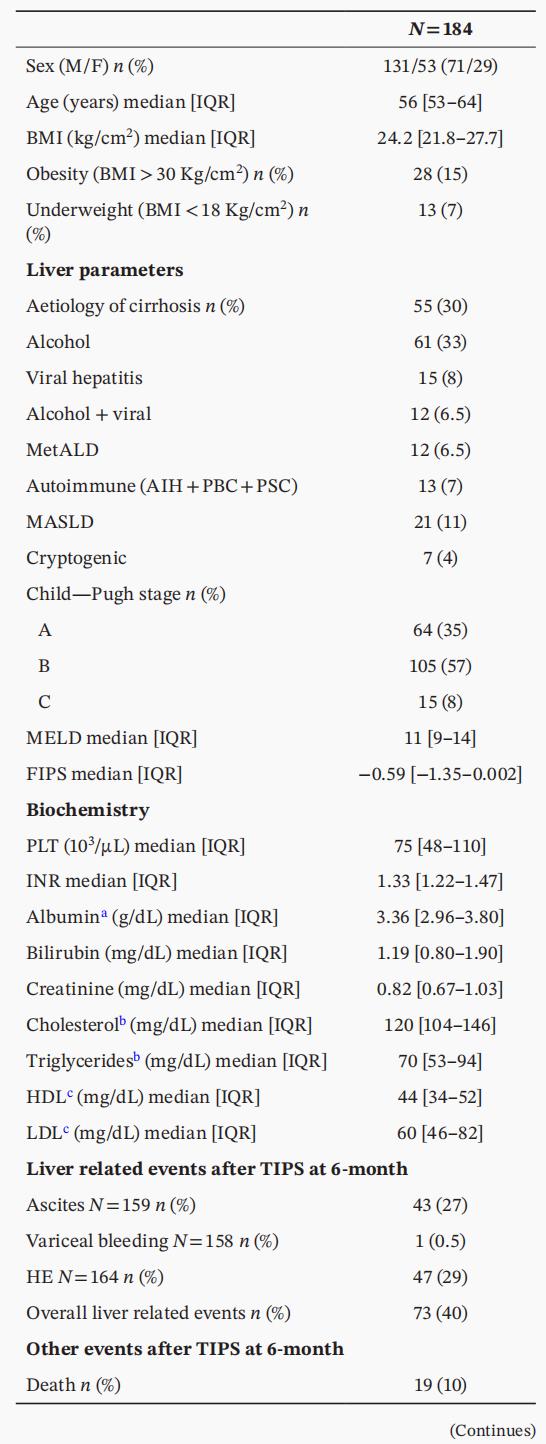

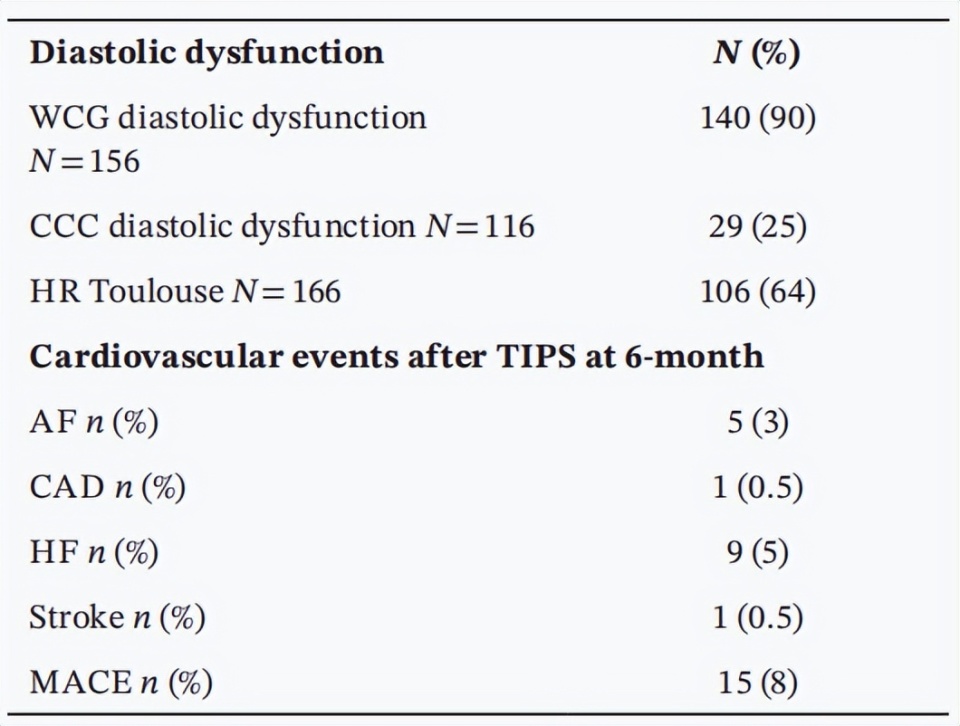
表2. 研究人群的心脏学特征,包括超声心动图和血流动力学特征

02
TIPS术后6个月的随访结果
术后6个月内,MACE总体发生率较低,仅为8%(15/184),且多发生于术后早期(中位时间:28天)。具体包括心力衰竭(9例)、房颤(5例)、心肌梗死和卒中(各1例)。复合终点“死亡或肝移植(LT)”的发生率为15%(27/184),其中19名(10%)患者在TIPS术后6个月内死亡,包括13名(7%)死于肝脏并发症,9名(5%)接受了肝移植。肝移植后观察到1例死亡。
03
不同DD诊断标准的临床意义
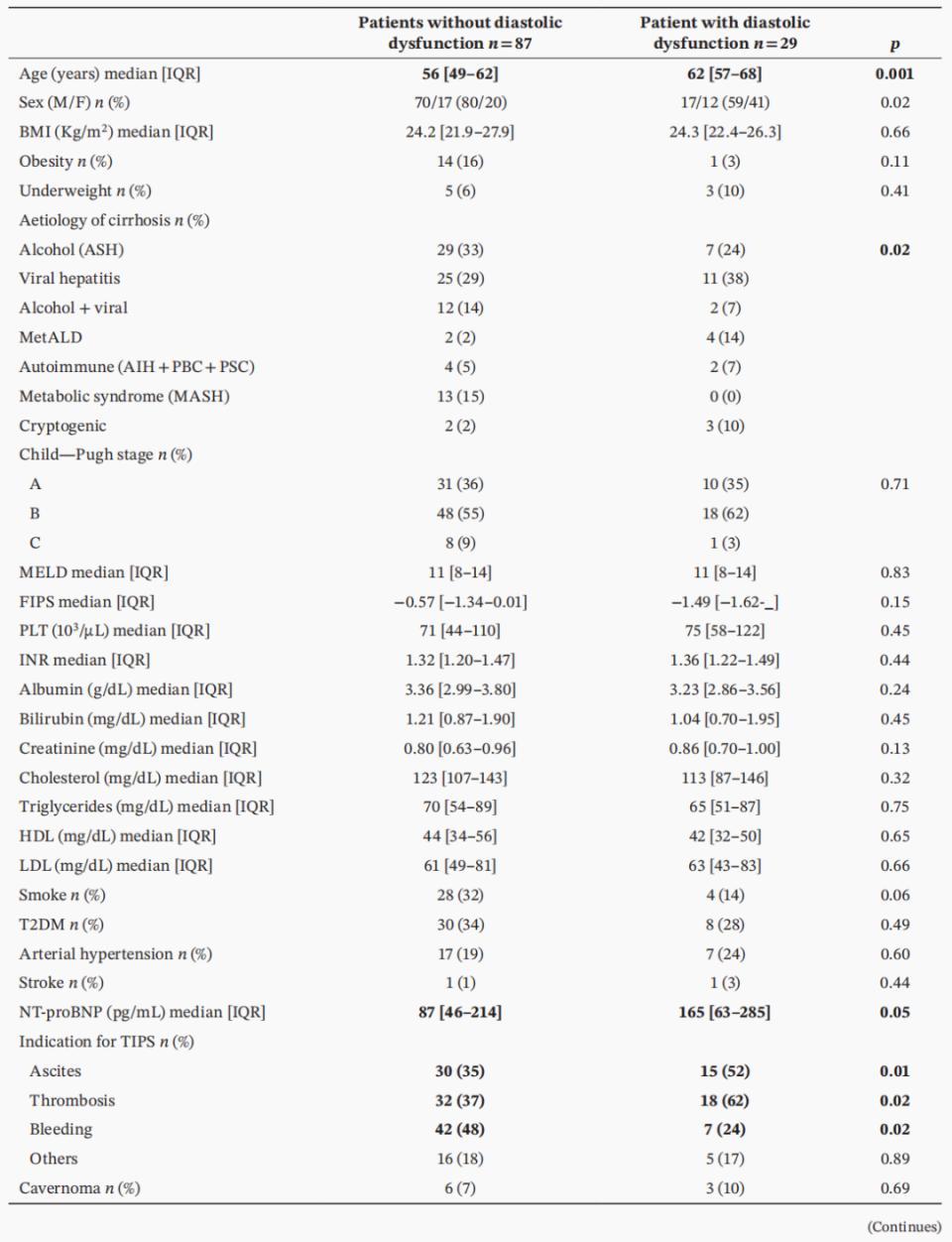
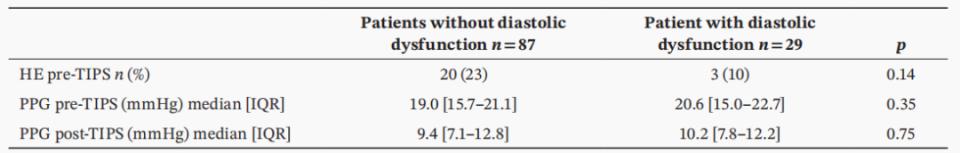
新旧诊断标准对DD的检出率存在巨大差异。按2005年WCG标准,绝大多数患者(90%)被诊断为DD,而采用2019年CCC标准时,DD患病率仅为25%。这表明新标准更为严格,筛选出的人群特征也不同:2019年CCC定义的DD患者年龄更大(62 vs. 56岁,P=0.001),NT-proBNP水平更高(165 vs. 87 pg/mL,P=0.05),且TIPS更常用于腹水(52% vs. 35%;P=0.01)和门静脉血栓(62% vs. 37%;P=0.02)治疗。值得注意的是,在DD患者(按2019年CCC标准)中,HE发生率显著更高(34% vs. 16%,P=0.03),但术后腹水复发、MACE(11% vs. 3%,P=0.29)及死亡/LT(14% vs. 18%,P=0.55)的发生率与非DD患者相比均无统计学差异(表3)。
表3. 根据CCC标准,有或无舒张功能障碍的患者在基线时的一般特征、心脏特征和TIPS特征的比较
04
TIPS术后MACE的风险因素
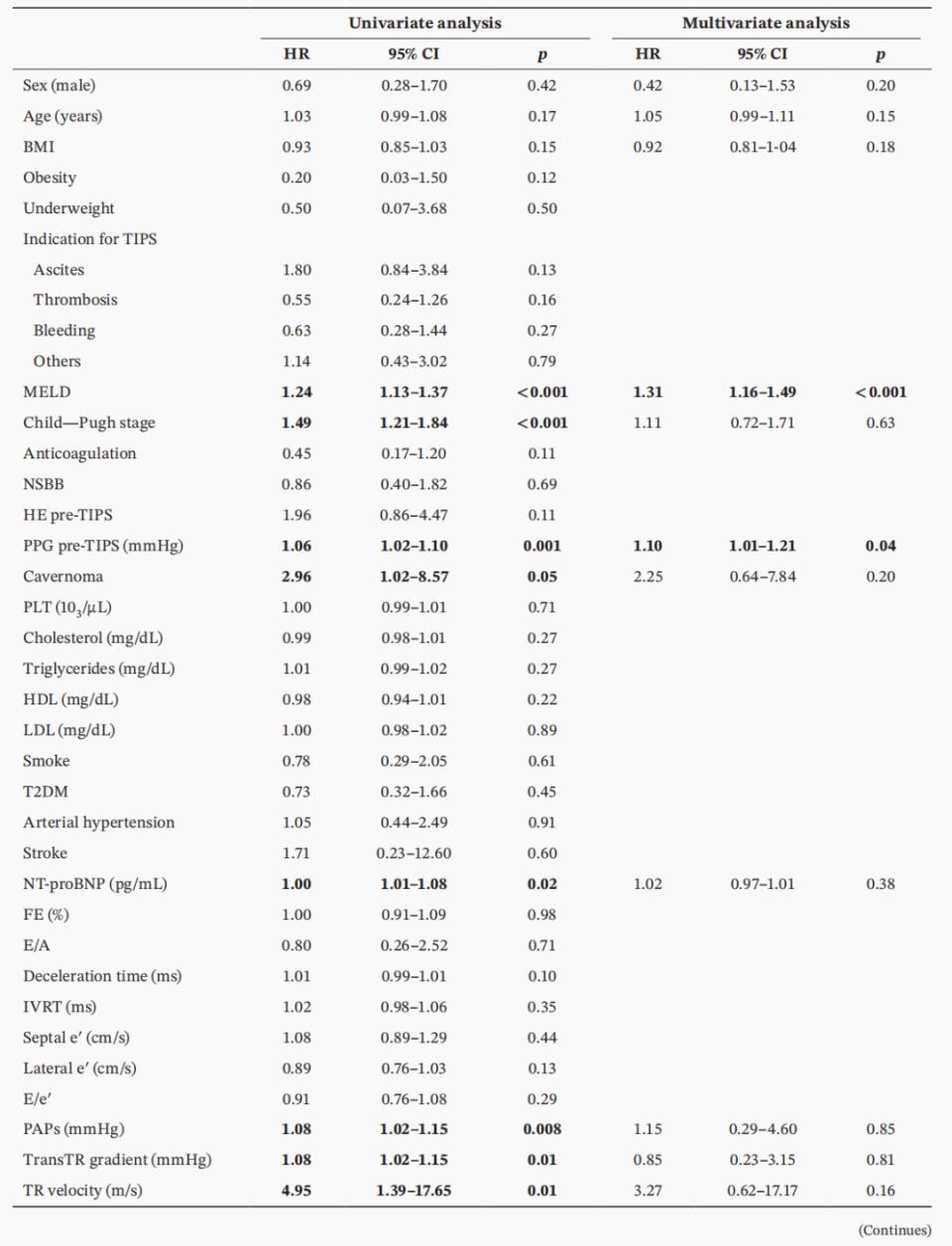
研究通过Fine & Gray竞争风险模型分析了MACE的危险因素。单因素分析(表4)显示,传统心血管危险因素与MACE显著相关,包括甘油三酯(sHR 1.02,95% CI:1.00-1.03;P=0.03)、动脉高血压(sHR=3.47,95%CI:1.27-9.52,P=0.02)、2型糖尿病(T2DM)(sHR=3.01,95% CI:1.04-8.75,P=0.04)以及NT-proBNP水平升高(每增加1 pg/mL的sHR=1.06,95% CI:1.04-1.08,P<0.0001)。
表4. 采用Fine & Gray模型分析的结果,以确定MACE的独立预测因子,并考虑死亡和LT作为竞争事件

然而,在多因素校正模型中(调整年龄、性别、BMI等混杂因素后),上述所有变量的统计学意义均消失(动脉高血压:sHR=2.30,P=0.27;T2DM:sHR=1.72,P=0.40;NT-proBNP:sHR=1.06,P=0.10)。最关键的是,超声心动图评估或右心导管检查的数据均未与MACE相关(数据未显示)。
05
TIPS术后LT和死亡的危险因素
单因素分析发现,反映肝病严重程度的指标如MELD评分、Child-Pugh分级、术前PPG、门静脉海绵样变、NT-proBNP、肺动脉压(PAPs)等均与该终点相关。多因素Cox回归模型(表5)最终确认,仅MELD评分(HR=1.36,95%CI:1.18-1.56,P<0.001)和TIPS术前门静脉压力梯度(HR=1.10,95%CI:1.01-1.21;P=0.038)仍是独立的预测因子。这意味着,患者的预后主要由其肝脏疾病的严重程度决定,而非心脏功能状态。无论采用何种DD诊断标准,DD本身均未进入最终的多变量模型。
表5. Cox-回归分析以确定复合结局LT a的独立预测因子

06
TIPS术后腹水的危险因素
多因素分析中,TIPS术后6个月未能完全缓解腹水与术前总胆固醇水平较低(OR=0.99,95%CI:0.97-1.00,P=0.049)、2型糖尿病(T2DM)(OR=3.72,95%CI:1.41-9.82,P=0.008)、TIPS时舒张压较低(OR=0.95,95%CI:0.91-0.99,P=0.03)、TIPS指征为腹水(OR=6.45,95%CI:2.44-17.03,P<0.001)显著相关。在以腹水为TIPS指征的亚组中,所有超声心动图参数及DD诊断标准(WCG或CCC标准)均与TIPS术后6个月未能完全缓解腹水无关。这表明,术后腹水控制不佳主要与代谢和血流动力学因素相关,而非心肌舒张功能本身。
总结展望本研究通过对184例接受TIPS治疗的肝硬化患者进行系统性分析,有力地挑战了“术前DD是TIPS术后心脏相关不良事件主要驱动因素”的传统观念。无论采用2005年WCG标准还是2019年CCC标准诊断的DD,均无法独立预测MACE或死亡/肝移植复合终点。这表明,在当前诊断框架下,术前常规进行复杂的DD分级对TIPS患者的预后分层价值有限。而肝病本身的严重程度(以MELD评分和术前门静脉压力梯度PPG为代表)是决定TIPS术后6个月内死亡或肝移植风险的唯一独立预测因子,其重要性高于心脏功能评估。
建议:对于拟行TIPS的肝硬化患者,临床决策应回归肝病本质,将评估重点放在肝功能储备和门脉高压严重程度上,而非过度依赖现有心脏超声参数进行风险分层。

翻译&解读
龚艳君
广州医科大学第一临床学院 本科生

专家简介
罗薛峰
四川大学华西医院消化内科
医学博士、副教授、博士研究生导师