如果问结直肠癌患者最怕什么?肝转移一定名列前茅,研究表明,肝转移是结直肠癌患者最主要的死亡原因[1-2]。今天我们通过一个真实案例来揭开结直肠癌的致命真相,请提前防范!

PART01 病情概述
2024年1月,李先生因为便血在北京某三甲医院做了肠镜检查,看到距肛门约12cm处存在肿物,等到活检结果出来,确诊是直肠中分化腺癌。
确诊后,李先生的家人赶紧跑医院、找医生,在2024年2月做了直肠癌根治术。
术后病理显示肿瘤最大直径2.5cm,侵及固有肌层,脉管侵犯阳性,淋巴结转移(2/13),分期为pT2N1bMx。免疫组化显示错配修复蛋白表达完整,Her-2阴性。
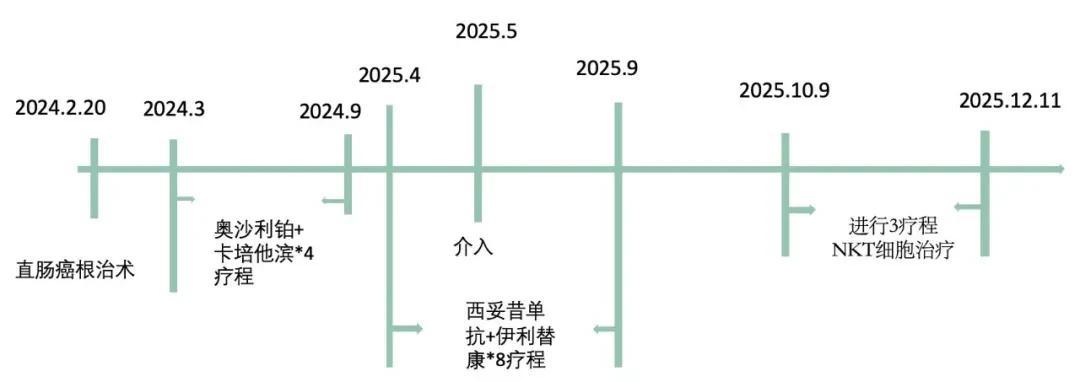
手术后2024年3月进入辅助化疗,先是做了4疗程奥沙利铂+卡培他滨,后续又做了4疗程单药卡培他滨,直到2024年9月底完成化疗。
手术切了肿瘤,又做了8个疗程全身化疗,术后CEA持续正常维持在1.7ng/ml左右,李先生觉得体内的癌细胞杀得很干净,应该没什么问题了。
但是反转来得猝不及防,2025年3月术后13个月复查竟然出现了肝转移。
肝转移,结直肠癌的致命真相肝脏可以说是结直肠癌血行转移最爱去的靶器官,由于结肠和直肠大部分的血液经门静脉直接流至肝脏,肝脏的肝窦结构会让血流速度减慢,就给了癌细胞容易在此滞留的机会,再加上肝脏微环境适宜癌细胞生存等因素,让肝脏被结直肠癌“偏爱”。
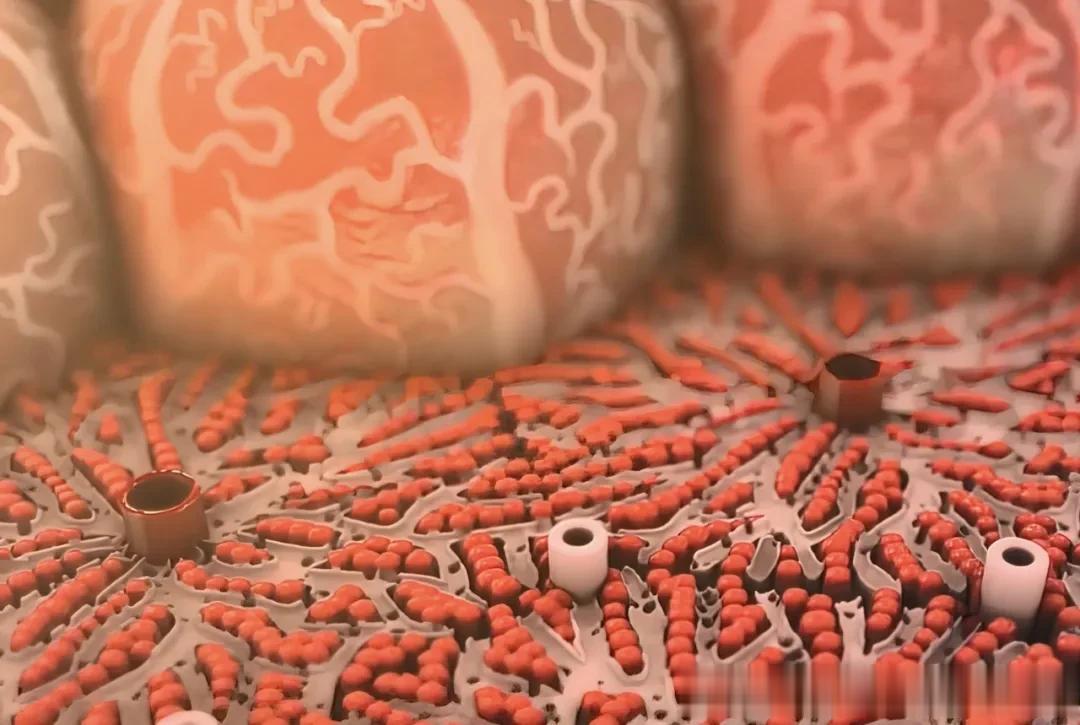
15%~25%结直肠癌患者在确诊时即合并有肝转移,而另15%~25%的患者在结直肠癌原发灶根治术后发生肝转移[3]。
肝转移对于结直肠癌患者意味着?很多人一听“肝转移”就以为癌症到了晚期没救了,先别紧张,对于结直肠癌来说,肝转移是一个特殊的存在。
80%~90%的肝转移灶初始无法获得根治性切除[3],李先生的情况也是如此。但研究表明,最初肝转移灶无法根除的患者经治疗后可以转化为可切除或消融。肝转移灶能完全切除或消融后,患者的中位生存期达35~60个月,5年总体生存率可达40%~57%[4-8]。
于是2025年4月李先生开始二线化疗,8疗程的西妥昔单抗+伊利替康。
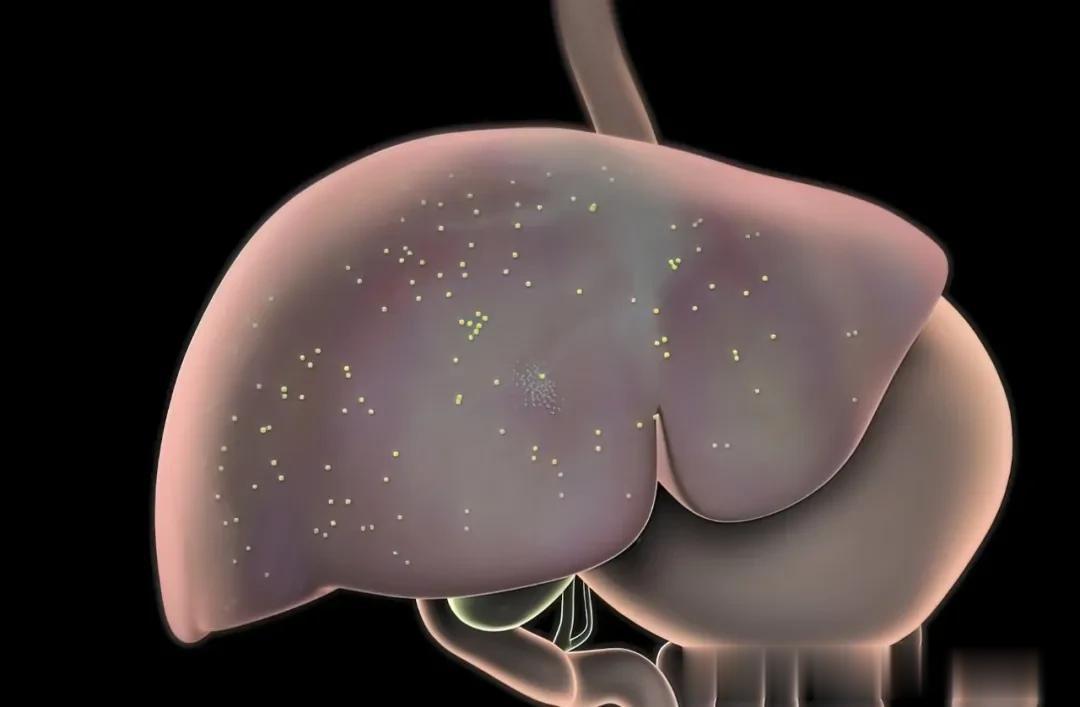
期间2025年5月还对肝转移病灶做了微波消融治疗。
经过一系列治疗,李先生的肿瘤标志物CEA基本稳定下来,影像学显示肝内病灶控制,无新发灶。但是CA19-9和细胞角蛋白19片段出现波动升高。
CA19-9的波动升高,由于肝脏是CA19-9代谢和清除的重要器官,有肝转移病史的患者出现这一指标的升高常被视为肝内病灶活动或进展的间接信号。
细胞角蛋白19片段波动升高,治疗后这一指标升高可能反映残留肿瘤细胞活跃或微转移灶存在,如果持续或进行性升高则提示疾病可能进展。
两者同时波动升高,要高度警惕是不是有隐匿性肿瘤残留或早期复发,虽然影像学上还没有看到,但标志物已经先一步有了变化。
肝转移后,有哪些“武器”可用?① 系统药物治疗:化疗+靶向药
② 局部根治手段:微创消融或手术
③ 后续巩固:监测+维持治疗
李先生①②步治疗已完成,影像检查上看起来“干净了”,但是肿瘤标志物CA19-9和细胞角蛋白19片段仍在提示微小残留病灶的高风险,依然让人没办法安心。
后续该如何维持现有的治疗成果,清除残留癌细胞,让无进展生存期延长?手术、化疗、放疗这些方式已经派不上用场,李先生在朋友的介绍下开始了解免疫治疗技术,并最终选择了清华大学免疫学张明徽教授团队研发的vNKT免疫细胞疗法。
PART02 第二诊疗建议
✔ 李先生系统化疗和局部治疗已完成,当前肿瘤负荷已降低,正是清除微小残留病灶的最佳窗口期。
✔ 李先生的肠癌类型对PD-1/PD-L1抑制剂几乎无效,传统免疫治疗获益有限。
✔ vNKT细胞是一类兼具NK细胞杀伤力与T细胞特异性的双重抗肿瘤效应免疫细胞,不仅能够直接杀伤癌细胞,还会调节肿瘤组织内部的免疫微环境。它在清除微小残留病灶、延缓复发方面具有很大潜力。

实验条件:有vNKT细胞存在的情况下,经过16个小时,近乎所有B16肿瘤细胞被杀死!
2025年10月李先生进入vNKT细胞治疗,目前已完成3疗程,肿瘤标志物趋于稳定,影像学报告未出现新发病灶,整体病情平稳。


PART03 结论与点评
在现代肿瘤治疗中,无瘤并不等于无风险,有时候看不见的敌人才是最难防的。vNKT免疫细胞治疗正在成为癌症患者长久治愈的一种重要巩固策略,它追求的不是让肿瘤缩小,而是在肿瘤尚未卷土重来之前,提前布防、清除残敌。这不仅是治疗的延续,更是对长期生存的主动管理。
参考文献:
[1]Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020[J].CA Cancer J Clin, 2020, 70(1): 7-30. DOI:10.3322/caac.21590.
[2]Cohen R, Raeisi M, Chibaudel B, et al. Prognostic value of liver metastases in colorectal cancer treated by systemic therapy: An ARCAD pooled analysis[J]. Eur J Cancer, 2024,207:114160. DOI: 10.1016/j.ejca.2024.114160.
[3]Vibert E, Canedo L, Adam R. Strategies to treat primary unresectable colorectal liver metastases[J]. Semin Oncol,2005, 32(6 Suppl 8): 33-39. DOI: 10.1053/j. seminoncol.2005.07.015.
[4]de Jong MC, Pulitano C, Ribero D, et al. Rates and patterns of recurrence following curative intent surgery for colorectal liver metastasis: an international multiinstitutional analysis of 1669 patients[J]. Ann Surg, 2009,250(3):440-448. DOI: 10.1097/SLA.0b013e3181b4539b.
[5]Margonis GA, Sergentanis TN, Ntanasis-Stathopoulos I, et al. Impact of Surgical Margin Width on Recurrence and Overall Survival Following R0 Hepatic Resection of Colorectal Metastases: A Systematic Review and Metaanalysis[J]. Ann Surg, 2018, 267(6): 1047-1055. DOI:10.1097/SLA.0000000000002552.
[6]Giuliante F, Ardito F, Vellone M, et al. Role of the surgeon as a variable in long-term survival after liver resection for colorectal metastases[J]. J Surg Oncol, 2009, 100(7):538-545. DOI: 10.1002/jso.21393.
[7]Padmanabhan C, Nussbaum DP, D'Angelica M. Surgical Management of Colorectal Cancer Liver Metastases[J].Surg Oncol Clin N Am, 2021,30(1):1-25. DOI: 10.1016/j.soc.2020.09.002.
[8]Morris VK, Kennedy EB, Baxter NN, et al. Treatment of Metastatic Colorectal Cancer: ASCO Guideline[J]. J Clin Oncol, 2023,41(3):678-700. DOI: 10.1200/JCO.22.01690.