

当80%的临床I期睾丸癌患者本可通过单纯手术治愈时,为何仍有20%的人被迫接受不必要的化疗毒性?
2026年2月,于美国旧金山举行的2026年泌尿生殖系统肿瘤研讨会(ASCO GU)上,澳大利亚彼得·麦克卡勒姆癌症中心的Ben Tran博士报告了CLIMATE研究(ANZUP 1906)的中期结果,该研究题为"Initial Results from CLIMATE (ANZUP 1906): A Prospective Cohort Study Assessing the Clinical Utility of miR-371a-3p as a Marker of Minimal Residual Disease in CS1 Testicular Germ Cell Tumor"。这一前瞻性队列研究将循环微小核糖核酸miR-371a-3p(microRNA-371a-3p)从实验室概念验证推向临床决策实用化验证。
现行监测策略疗效确切却毒性难避,分子标志物能否精准识别真正的高危复发人群?睾丸生殖细胞肿瘤(TGCT)作为15-39岁男性最常见的实体恶性肿瘤,其临床I期患者(CSⅠ)在接受睾丸切除术后的标准管理策略始终是肿瘤学界争论的焦点。当前国际指南推荐主动监测作为首选方案——约80%的CSⅠ患者通过单纯手术即可达到治愈,而辅助化疗虽能将复发风险从15%-50%降至3%-5%,却意味着对绝大多数本无复发风险的患者施加不必要的铂类化疗毒性,包括长期心血管风险、继发性白血病及肾功能损伤等。然而,现有基于肿瘤大小、淋巴血管侵犯(LVI)及组织学类型的风险分层模型预测准确性有限,导致临床决策常在过度治疗与治疗不足间艰难摇摆。
miR-371a-3p属于miR-371~373簇,在胚胎干细胞分化调控中具有关键作用,而在睾丸生殖细胞肿瘤中呈现高特异性表达。既往回顾性研究已证实其敏感性约90%、特异性超过90%,显著优于传统血清标志物甲胎蛋白(AFP)、β-人绒毛膜促性腺激素(β-hCG)及乳酸脱氢酶(LDH)——这些传统标志物在初诊时仅约60%患者升高,且在监测微小残留病(MRD)方面表现欠佳。
若能在睾丸切除术后早期通过血液检测识别出真正具有残留病灶的高危患者,便能精准筛选辅助化疗获益人群,同时让低危患者安心免于过度治疗,实现疗效与毒性的最优平衡。
前瞻性多中心队列设计保障证据等级,血浆血清双样本策略探索最优检测基质?本研究是一项前瞻性、多中心队列研究,旨在评估睾丸切除术后基线miR-371a-3p水平对CS1睾丸生殖细胞肿瘤患者复发风险的预测价值,并比较血浆与血清作为检测基质的性能差异。研究由澳大利亚与新西兰泌尿生殖与前列腺癌试验组(ANZUP)主导,联合沃尔特与伊丽莎·霍尔医学研究所(WEHI)共同开展,在澳大利亚与新西兰12个临床中心招募患者。
纳入标准设定为:年龄≥18岁,经组织学确诊为CS1睾丸生殖细胞肿瘤(无转移证据),计划接受主动监测,且在睾丸切除术后6周内入组。研究排除已接受辅助化疗或放疗的患者,以确保研究人群能真实反映单纯手术后的生物学状态。样本采集方案设计精细:在基线(术后≤6周)及此后每3个月一次、持续24个月的随访期内,同时采集血浆与血清样本,并在临床确诊复发时再次采集。所有临床与结局数据录入iTestis注册库——这是澳大利亚专门的睾丸生殖细胞肿瘤登记系统,保障了数据的标准化与完整性。miR-371a-3p检测采用基于定量PCR(Quantitative PCR)的技术平台,以已发表方法学为基础,设定检测阈值:当三次重复定量PCR的Ct均值≤40:1时判定为可检测。这一技术参数的选择体现了研究团队在灵敏度与特异度间的审慎平衡。
研究设置双重主要终点:首要目标是确定术后基线miR-371a-3p预测复发的阳性预测值(PPV);次要目标包括比较血浆与血清样本的检测性能,并与同期进行的国际协作研究AGCT1531(美国儿童肿瘤组)及SWOG1823(美国西南肿瘤组)进行数据验证。这种多中心协作设计不仅增强了样本代表性,更为后续跨研究验证奠定了基础。从2021年至2025年,研究共招募200例患者,其中196例在数据截止日前完成基线样本检测并被纳入本次中期分析,样本量计算充分考虑了预期20%的复发率及标志物检测的技术可变性。
血浆检测性能显著优于血清,基线标志物阳性者复发风险激增10倍且现有病理指标全面落败?CLIMATE研究的中期分析结果展现了miR-371a-3p作为微小残留病标志物的显著临床价值。在196例可评估患者中,中位年龄33岁(范围22-78岁),组织学类型分布为纯精原细胞瘤117例(60%)与非精原细胞瘤79例(40%)。中位随访18.9个月期间,共观察到40例(20%)复发,中位复发时间为4.2个月(范围1.1-17.7个月)。值得注意的是,实际复发时间较历史预期明显缩短:精原细胞瘤中位复发6.7个月(传统预期14-15个月),非精原细胞瘤中位复发4.0个月(传统预期5-6个月),这一发现可能反映了现代影像学早期检出能力的提升,也可能暗示了纳入人群的真实高危特征。
在样本基质比较方面,血浆检测展现出明确优势。基线血浆miR-371可检测率为21%(42/196),血清为17%(34/196)。受试者工作特征曲线(ROC)分析显示,血浆检测的曲线下面积(Area Under Curve, AUC)为0.77,显著优于血清的0.69,因此后续分析均基于血浆数据,报告如下:
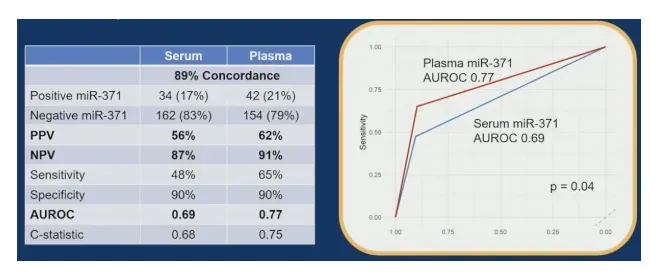
在复发预测效能上,基线血浆miR-371阳性表现出62%的阳性预测值与91%的阴性预测值。基线miR-371可检测组与不可检测组的24个月无复发生存率分别为32%与89%,风险比(HR)高达10.3(95%CI:5.3-19.8,p<0.001),意味着标志物阳性患者的复发风险是阴性者的10倍以上。
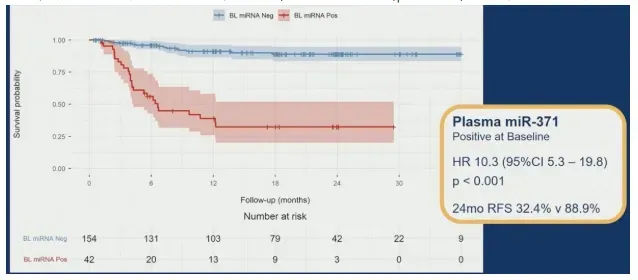
研究进一步揭示了标志物检测与临床结局的复杂关系。在40例复发患者中,14例(35%)基线血浆miR-371为阴性,中位复发时间6.9个月,提示存在标志物阴性的复发亚群,可能与肿瘤生物学异质性或检测灵敏度极限有关。
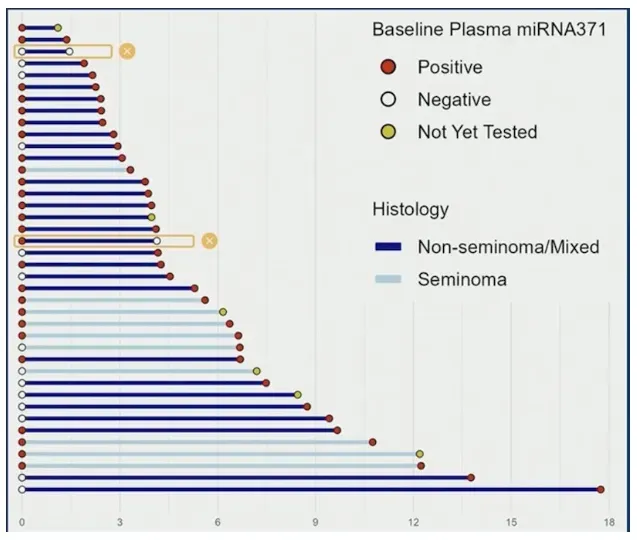
而在156例未复发患者中,16例(10%)基线标志物阳性但未出现复发,提示可能存在标志物阳性但无临床意义残留病灶的情况,或预示更长的随访期内可能出现迟发复发。
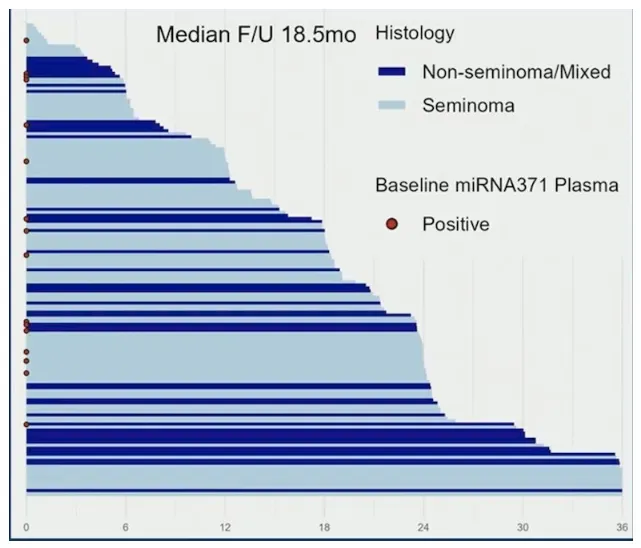
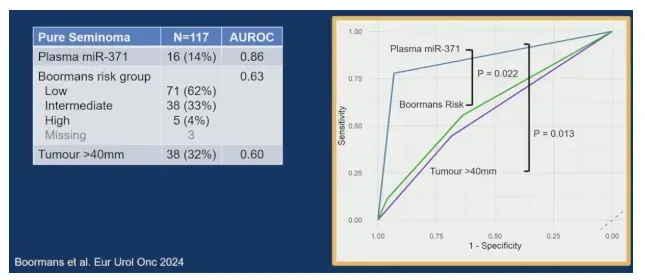
亚组分析展现了miR-371a-3p对传统风险分层的全面超越。在精原细胞瘤亚组(10例复发,中位随访18.4个月),miR-371的AUC达0.86,显著优于肿瘤大小>4cm(AUC 0.57,p=0.02)及Boorman风险分组(AUC 0.61,p=0.03)。
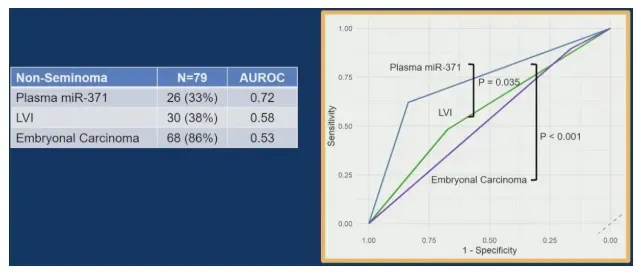
在非精原细胞瘤亚组(30例复发,中位随访20.8个月),miR-371的AUC为0.73,显著优于淋巴血管侵犯(AUC 0.58,p=0.035)及胚胎性癌成分(AUC 0.53,p<0.001)。
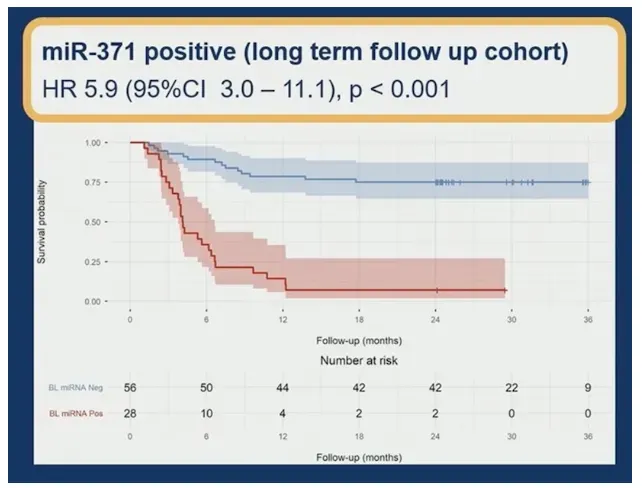
在对84例(43%)有复发或随访超过24个月的患者进行的敏感性分析中,miR-371展现出更高的判别准确性:AUC提升至0.80,阳性预测值达93%,阴性预测值为75%。无复发生存差异依然显著(HR5.9,95%CI:3.0-11.1,p<0.001),证实了标志物在更长随访期内的稳定预测价值。
Tran博士在报告中坦承研究的局限性:样本量相对较小(n=200),当前为中期分析且随访时间较短(中位18.9个月),且未纳入系列样本的动态变化分析。最终分析将整合完整随访数据及连续监测样本,并通过AGCT1531与SWOG1823研究进行外部验证。
总结该研究的核心贡献在于将分子标志物从诊断场景拓展至预后分层场景,为精准肿瘤学在睾丸癌领域的实践提供了关键证据。首先,血浆检测优于血清的技术发现为临床检测标准化提供了直接指导;其次,标志物对传统病理指标的全面超越挑战了现有风险分层体系,提示未来指南修订需纳入分子标志物;最后,91%的阴性预测值为临床豁免低危患者过度治疗提供了信心,而62%的阳性预测值(敏感性分析中达93%)则为高危患者早期干预指明了方向。尽管随访时间有限且存在标志物阴性复发的识别盲区,CLIMATE研究仍为个体化辅助化疗决策奠定了坚实基础,其最终分析结果及国际协作验证数据备受期待。
参考文献
Tran B, Grimison PS, Lewin JH, et al. Initial Results from CLIMATE (ANZUP 1906): A Prospective Cohort Study Assessing the Clinical Utility of miR-371a-3p as a Marker of Minimal Residual Disease in CS1 Testicular Germ Cell Tumor. Presented at: 2026 Genitourinary Cancers Symposium; February 26-28, 2026; San Francisco, CA.
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:白术
审核:梨九
封面图源:CMT