
导语:“治愈”二字说出口时,你曾否想过,放疗靶区外那几毫升下颌骨也在悄悄计数?五年后,张口受限、骨坏死、吸入性肺炎轮番登场,把无瘤生存变成二次战场。谁能提前锁定这群将被“迟来毒性”拖回医院的患者,并真正把治愈变成“活得久也活得好”?

图源:CMT
治愈数字节节高,迟来毒性却偷走生存,年轻口腔癌患者为何首当其冲?颌颈放疗后第三个月,患者张口度悄悄掉下1cm,你以为是术后疼痛未缓;第六个月纤维索条爬上咽缩肌,他才坦白吃流食也得配水冲。我们早已能把局晚喉癌的三年LC推到85%以上,却不得不看着40%的人在随访椅上因骨坏死或吸入性肺炎二次入院——治愈数字与致残曲线平行上扬,成为现代头颈放疗的“孪生耻辱”。更棘手的是,这些毒性多在无瘤窗口期出现,影像上既无复发证据,临床又缺乏统一编码,只能散落为“下颌疼痛”“吞咽困难”等碎片化主诉,真实发生率被系统性低估。现有干预为何失灵?首先,剂量学指南仍沿用10年前的OAR阈值,对口腔、下颌骨和舌下神经的“可接受剂量”停留在2D时代经验,IMRT的亚毫升级梯度优势未被重新标定。其次,毒性监测依赖RTOG量表,其主观等级与客观功能结局脱节,Grade 2的纤维化可能已意味着经口摄入热量<500 kcal/d,却仍被记录为“轻度”。再者,术后辅助放疗决策把“切缘阳性”视为唯一升级指征,却忽视口腔癌原发灶+双侧颈清扫带来的“手术+放疗”双轨打击——多模态治疗强度与迟发损伤之间缺少动态权衡模型,导致“治愈性剂量”在部分患者身上实质演变为“致残性剂量”。

2025年10月The Lancet Regional Health–Americas刊出的这项加拿大队列研究,把RLT从模糊主诉推向可量化终点:首次在>7000例连续病例中,用竞争风险模型把复发死亡与毒性死亡拆账,并区分“可改”与“不可改”因子,让“剂量-体积-手术-吸烟”四重交互作用首次有了真实世界权重。它把临床散点痛症拼成一张迟发毒性的“生存曲线”,提示若继续用旧阈值做计划,我们实际上在默许一条与肿瘤复发平行的死亡通道——头颈放疗的下一个技术拐点,不再是提高LC,而是把RLT发生率写进治愈率的定义里。
把复发和死亡设为竞争事件,用时间依赖Cox拆解毒性对寿命的暗箭,可行吗?本研究是一项回顾性队列研究,旨在量化≥50 Gy治愈性放疗后严重RLT(≥RTOG 3级)的累积发生率、危险因素及对总生存(OS)的独立影响。作者从2003-2020年加拿大Princess Margaret癌症中心7622例接受根治性放疗(含术前/术后)的HNC患者中,剔除再放疗、随访<2年、出现局部或远处复发者,最终锁定4650例“无瘤幸存者”进入精细化分析。暴露变量被事先二分为“可改变”与“不可改变”:前者包括放疗技术(IMRTvs2D/3D)、颈部照射体积、剂量>60 Gy、同步化疗、颈清扫及吸烟状态;后者涵盖年龄、性别、原发部位、TNM分期。主要终点为RLT累积发生率(competing risk:复发或死亡);次要终点是OS,并引入时间依赖协变量“RLT发生”校正immortal time bias。多变量分析采用Fine-Gray模型(RLT发生)与Cox比例风险模型(OS),同时探索成人迟发放射效应门诊(ARLEC)多学科管理是否稀释死亡风险。
五年毒性率16%且死亡风险翻倍,转去专科门诊可把HR降到1.7,为何仍不显著?五年累积毒性16%,死亡风险瞬时翻倍——图1曲线背后的数字警钟
整条队列7622例中位随访5.2年,958例出现≥3级RLT,竞争风险模型算出5年累积发生率16%(95%CI:15–16),并以每年≈1%的斜率继续爬升;其中骨坏死占34%(325/958),需管饲吞咽困难16%(157/958),外周神经病变16%(153/958),纤维化/淋巴水肿13%(122/958),四者合计>75%。作者强调,该曲线把“死亡或复发”设为竞争事件,因此16%是“在无瘤且存活”人群中真实可累积的毒性概率,远高于既往把毒性作为“随访副产物”报告的8–10%。
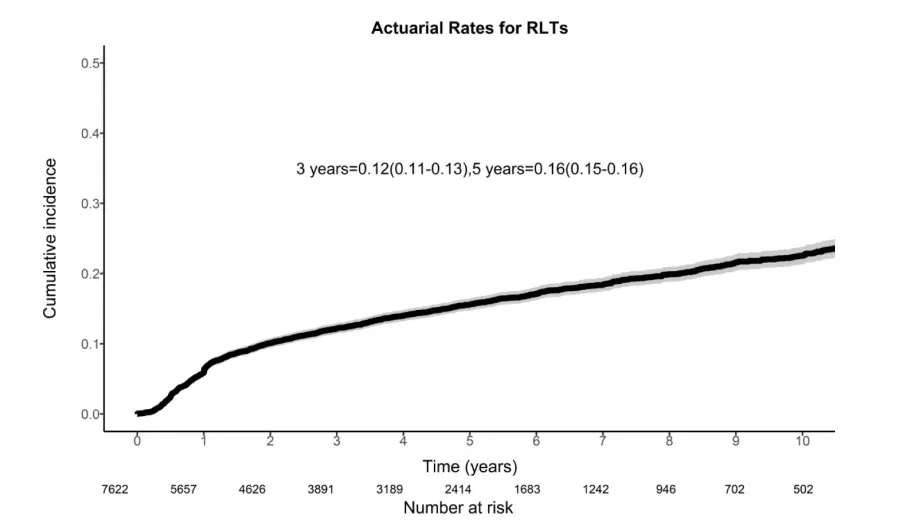
图1
注:整个队列(n=7622)严重(RTOG 3级和4级)迟发放射毒性(RLT)的实际发生率。采用累积发生率函数计算,以未发生RLT的死亡或复发为竞争风险。阴影区域表示实际发生率的95%CI。RTOG–放疗肿瘤学组。
非IMRT技术毒性风险+78%,口腔癌原发再追加48%——图2森林图左侧量化可改与不可改因子
多变量Fine-Gray模型显示,可改变阵营里,非IMRTvsIMRT的HR=1.78(p<0.001);双侧颈部照射vs不照颈部HR=2.42;剂量>60 Gyvs≤60 GyHR=1.35;同步化疗HR=1.28;颈清扫HR=1.54;诊断时仍吸烟HR=1.22(均p≤0.012)。不可改变阵营中,女性HR=1.33;口腔原发vs口咽HR=1.48;年龄<50岁HR=1.27。作者指出,口腔癌与双侧颈照叠加时,5年RLT概率跳升至28%,提示“原发部位+照射范围”可作为术前决策是否做颈清扫的实时权衡变量。
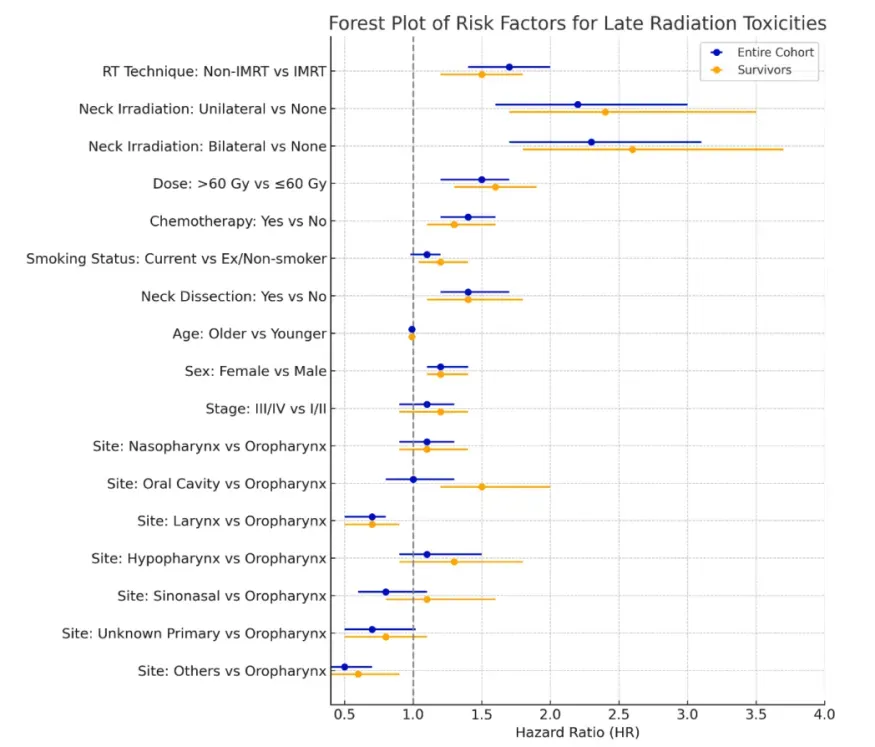
图2
注:森林图展示整个队列及幸存者发生严重迟发放射毒性的危险比(HR)及95%CI。危险比表示图中先列出变量相对于后列出变量发生结局的相对风险。RT–放疗;IMRT–调强放疗;Others–唾液腺、皮肤及肉瘤。
幸存者亚组危险谱几乎复制全队列——图2右侧验证风险模型在无瘤人群的外推性
4650例无复发且存活≥2年的幸存者中,上述HR点估计仅出现微小漂移:非IMRTHR=1.73,双侧颈照HR=2.38,口腔癌HR=1.44,女性HR=1.30,方向与显著性一致,P值仍≤0.003。作者认为,这排除了“毒性发生率被隐匿复发稀释”的可能性,证实危险因素一旦在诊断时锁定,其效应可持续至治愈后第五年,为后续“治愈后风险分层随访”提供时间窗口。
RLT出现即触发死亡陷阱,时间依赖Cox给出HR2.1——图3三曲线拉开生存差距
把RLT设置为时间依赖协变量,校正年龄、性别、分期、HPV、吸烟、化疗等混杂后,任何时点发生≥3级RLT的患者瞬时死亡风险升高2.1倍(95%CI:1.8–2.5,p<0.001)。作者拆解发现,吸入性肺炎与下颌骨坏死合并感染是最常见的毒性相关死因,占毒性组死亡的42%,而对照组主要死因为第二原发癌与心血管事件,提示RLT通过“局部功能崩溃→营养不良-感染”轴心缩短生存。
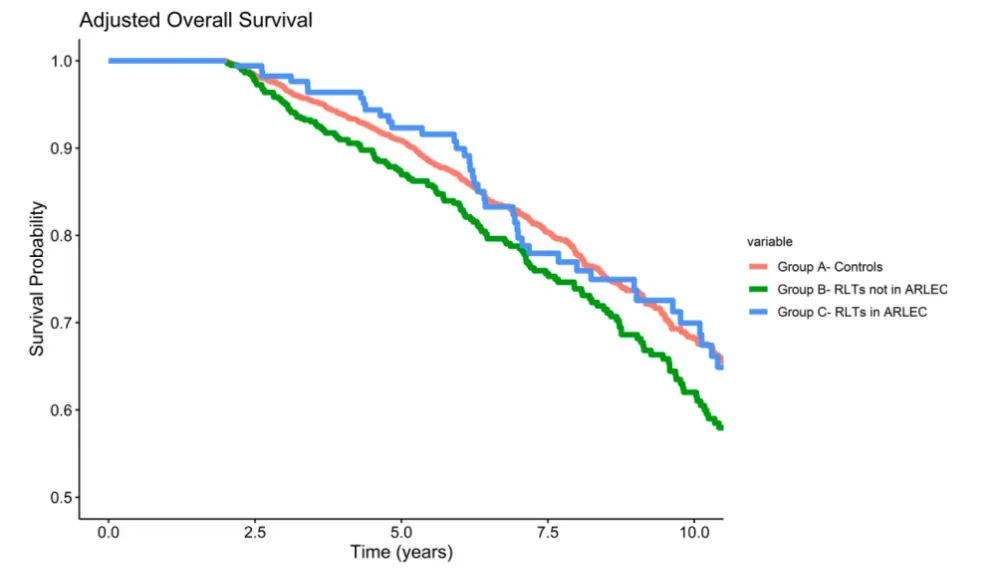
图3
注:使用多变量时间依赖Cox比例风险模型比较A、B、C三组的调整后总生存(OS)。模型以RLT发生为时间依赖协变量,并对性别、年龄、ECOG体能状态、分期、原发部位、HPV状态、吸烟状态、初始治疗及化疗进行调整。ECOG PS–东部肿瘤协作组体能状态;HPV–人乳头瘤病毒;RLT–迟发放射毒性;ARLEC–成人迟发放射效应门诊。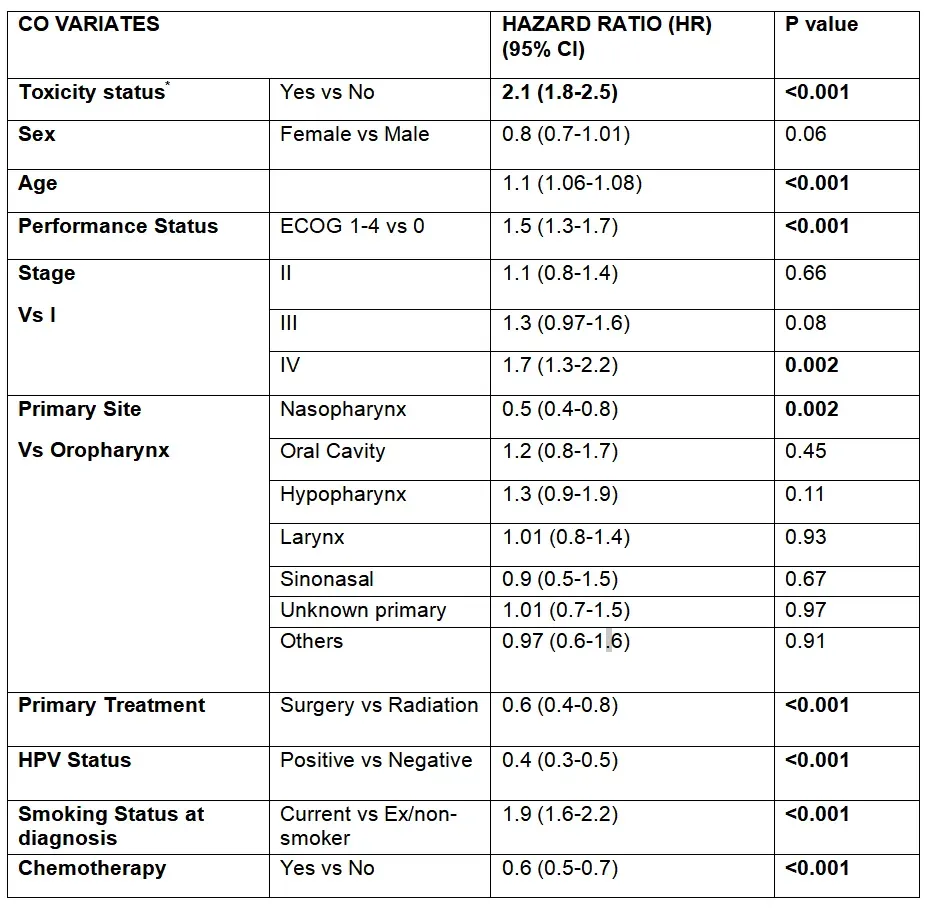
图4
注:幸存者中总生存多变量Cox模型结果(对应图4的主模型)。
专科门诊仅把HR从2.2降到1.7,差异未过α——图5Group CvsB段间距
进一步把毒性患者分为未转诊(Group B,n=659)与转ARLEC(Group C,n=299),时间依赖Cox显示Group Bvs对照Group AHR=2.2(1.9–2.7),Group CvsAHR=1.7(1.3–2.4),但Group CvsB直接比较HR=0.78(0.93–1.78,p=0.13)。作者讨论认为,选择偏倚(更重症状才转科)、干预时机晚(中位转科时间毒性发生后1.8年)、缺乏标准化康复协议,是“获益不显著”的三连坑;他们正在启动前瞻性“症状-触发-即刻转科”试验,以验证如果把介入窗口提前至毒性1级,能否把HR压到<1.3。
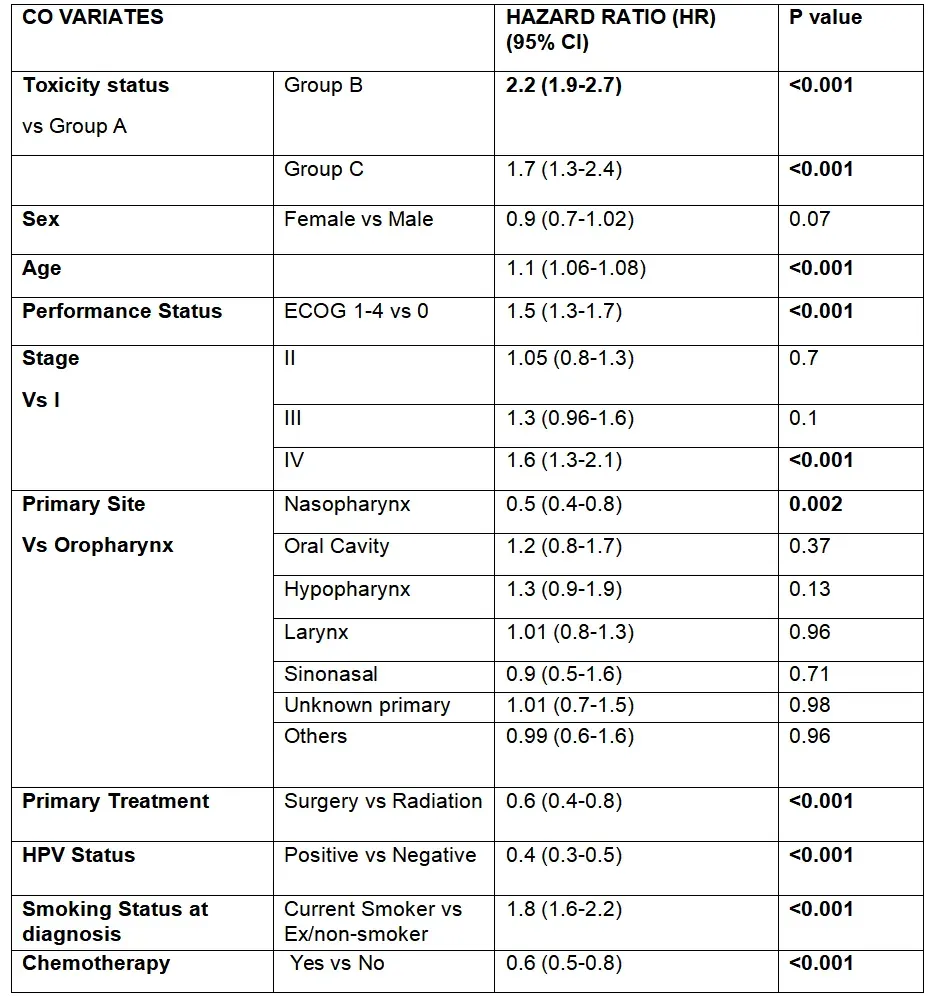
图5
注:A、B、C三组间总生存差异的多变量Cox模型结果(对应图4组间比较)。
吸烟毒性信号贯穿五年,戒烟窗口仍需前移
诊断时仍吸烟在幸存者亚组仍保持HR 1.22(p=0.012),且与口腔癌、颈清扫呈乘法交互(RERI=0.44)。作者引用中心前瞻性戒烟项目数据指出,若患者在放疗第一周内即停止吸烟,5年RLT绝对值可降6%,但样本仅218例;他们呼吁把“戒烟≤放疗第5次”写进质量指标,否则“剂量雕刻再精细,也抵不过一支烟的持续缺氧-微血管打击”。
总结本文用七千余例真实世界数据把RLT从“生活质量配角”推至“生存终点主角”:五年累积16%、死亡风险+110%,且年轻、女性、口腔癌、吸烟、颈清扫、高剂量放疗构成高危指纹。研究首次量化ARLEC多学科门诊的潜在“减损”幅度(HR2.2→1.7),虽未达显著,却为后续前瞻性干预试验划出样本量基准。作者把可改变因素明明白白摆在案头:推广IMRT、精准限制口腔与下颌骨剂量、慎行颈清扫、同步化疗权衡获益、诊断即刻戒烟,均可把RLT发生率往下拽;而对高危人群延长随访、早期专科转介,则有望把毒性对寿命的暗箭拔出来。对于每天把“治愈”挂在嘴边的临床团队,这份数据是一份迟到的提醒:放疗结束不是终点,而是第二战场的起点——只有把毒性筛查写进长期医嘱,才能真正让“活得久”与“活得好”并轨。
参考文献
Mathew JM, Ringash J, Su J, et al. Risk factors and survival impact of severe radiation-related late toxicities in head and neck cancer-a cohort study. [J/OL]Lancet Reg Health Am. 2025;50:101218. Published 2025 Sep 3. doi:10.1016/j.lana.2025.101218
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:一诺
审核:梨九
封面图源:CMT