
经历过试管移植失败的女性,对试管流程不陌生,一次次满怀希望的移植,又一次次失望地面对不着床或生化的结果。
在反复失败的迷茫中,查免疫往往成为一条被频繁提及的路径。
很多姐妹辗转于各大医院,抽了无数管血,尝试了各种免疫方案,身体承受着压力,内心却依旧充满疑问:
为什么我的身体就是留不住宝宝?难道问题真的全都出在免疫上吗?
事实上,生命的孕育如同一场精密的接力赛,移植只是其中一棒。
如果试管过程中卵子成熟或胚胎早期分裂时,就因为某种先天不足而微弱不堪,那么无论后续土壤(内膜)如何肥沃,园丁(免疫调节)如何努力,可能都无力回天。
上海九院匡延平教授领衔国内多个生殖团队正是将目光聚焦在了这个更为源头,却长期被临床忽视的关键环节上。
这项突破性科研成果刚刚被发表在了全球顶刊《细胞·基因组学》(Cell Genomics)上。
到底是怎么回事呢?赶紧跟着圈姐的解读一起来了解一下吧,也许就能帮你找到反复种植失败的原因呢!
01聚焦那些不明原因的种植失败我们想要成功怀孕,并最终生下一个健康的宝宝,首先需要有一颗优质的种子(卵子),这颗种子还要能顺利长成一个健康的幼苗(胚胎),这是最基本的前提。
但很多女性的种子或幼苗本身有质量问题,这会导致一系列悲剧,比如:
卵子长不大:种子还没成熟就停止发育了,有的甚至需要进行卵子体外培养;
受精失败:种子无法被成功激活,比如不受精,没有可用胚胎;
胚胎停止发育:主要体现在胚胎无法发育到八细胞。
以上这些情况,最终都会直接导致不孕。
更麻烦的是,在试管婴儿技术出现之前,医生很难提前知道卵子或胚胎好不好,相比之下,检查精子要方便得多。
只有当女性经历试管婴儿这个体外培养过程的时候,医生才能在试验室显微镜下亲眼看到,卵子到底有没有成熟?胚胎为什么长到一半不长了?
但是,这时发现问题已经为时已晚,患者已经承受了失败的经济和心理代价。
近年来,有了基因测序这种高科技工具(全外显子组测序,WES),科学家们才开始找到一些真正的罪魁祸首——也就是出问题的基因。
比如,之前研究发现TUBB8和PADI6这两个基因如果发生突变,就会直接导致卵子长不大或胚胎早期停育。
这个发现极其重要!它意味着,很多以前原因不明的卵子、胚胎质量问题,其实是一种遗传病,是会从父母那里遗传过来的,这彻底改变了对这类不孕症的认知。
虽然找到了一些嫌疑基因,但这只是冰山一角。
对于绝大多数不明原因反复种植失败患者(可能超过80%),医生仍然无法从基因层面解释她们失败的原因,这成了困扰医生和患者的巨大难题。
匡延平教授团队这篇研究想要回答一个非常关键的实际问题:
在我们遇到的所有因为卵子/胚胎问题而不孕的女性中,到底有多大比例的人,是能通过目前已知的这些基因检测找到明确原因的?还有哪些基因可能导致不明原因种植失败?
 02这项研究的设计?
02这项研究的设计?这项研究在全国多个生殖中心招募了三千多名原发不孕女性,她们至少经历了2次试管婴儿失败,并且失败的原因明确是卵子或胚胎问题,不是男方精子或子宫问题。
为了确保研究目的纯粹,他们排除了一些干扰因素,最终3627名患者组成了最终的研究队列。
研究人员将这些入组患者分为三组。
卵子缺陷组1554例,占比42.9%,主要包括卵子不成熟、透明带有问题、形态有问题;
受精异常组248例,占比6.8%,主要包括精卵结合后出问题,比如没有形成正常的双原核,而是形成了多个原核或者没有原核;
胚胎发育停滞组1825例,占比50.3%,指的是胚胎在早期就停止发育,无法长成8细胞胚胎或囊胚,或者看起来正常但反复种植失败。
之前研究知道有37个已知基因可能造成卵子出现问题,于是研究者首先对所有纳入研究患者进行已知卵子遗传基因缺陷进行检查。
03研究的主要成果在这37个已知卵子致病基因中,也有一个基因很关键,于是被列为重点排查头号嫌疑犯,那就是TUBB8基因。
于是,研究者首先对全部3627名患者进行TUBB8基因筛查,结果发现225个病例的病因是TUBB8突变。
研究者又对剩下的3402名(3627-225)患者筛查剩下的36个可疑基因,结果又查出了254个阳性病例。
也就是说,在已知的37个可能导致卵子出现缺陷的基因中,总共解释了479名患者的反复试管失败,占总人数3627的13.2%。
那么在这37个导致卵子缺陷的基因中,TUBB8是出问题最多的基因,单独揭示了225例患者的反复试管失败,占所有破案病例(479例)的47%;
PATL2是第二常见的,解释了45例,占所有破案病例(479例)的9.4%;
研究还发现一些基因变异会反复出现,比如PATL2基因的一个特定变异(c.223-14_223-2del)在45个病人中出现了20次,占比高达44.4%。
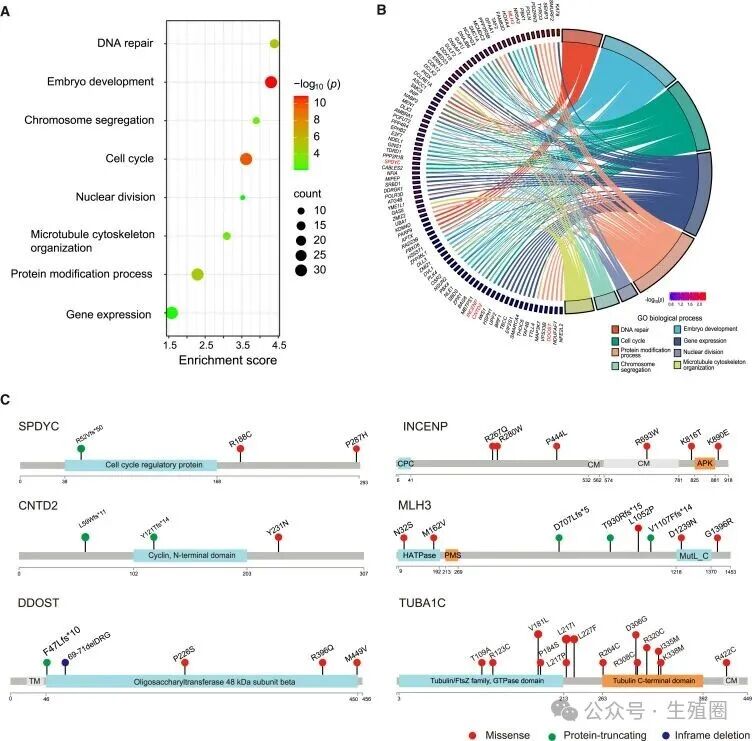
那么这37个可能导致卵子出现缺陷的基因在三个组中是如何分布的呢?
①
在卵子缺陷组1554例患者中,被明确诊断的占272例,诊断率占比17.5%;
其中TUBB8解释了155例,占该组的10.0%,它负责制造细胞骨架(像建筑的钢筋),它出问题,卵子成熟就会卡住。
其他骨架工比如TUBA4A等5个基因解释了14例(0.9%),说明骨架搭建是关键环节。
负责母源mRNA的基因指令传递员,比如PATL2,解释了52例,这些基因就像传递施工图纸的,它们出错,卵子发育就乱套。
质量检查员,细胞周期相关基因如CDC等,解释了13例。
特殊故障基因,比如PANX1 和COX15 基因故障会导致卵子“自杀”或退化,解释了14例。
特殊故障基因,比如透明带障碍相关基因ZP1/2/3,会导致卵子没有透明带或者透明带太厚,解释了 16例。
②
在受精异常组的248例中,诊断了38例,诊断率占比15.3%。
主要元凶为TUBB8和 WEE2这两个基因是主因,一起解释了 20例(8.0%)。
另外,细胞分裂基因(CDC20, CDC23)和防止多精入卵的基因(ASTL)故障,解释了5例(2.0%)。
③
胚胎停滞组1825例中,诊断了169例,诊断率占比9.3%。
TUBB8依然很关键,解释了57例,占比3.1%。
母体物资库故障,皮下母体复合物相关基因,如PADI6等7个基因,它们出问题解释了 41例,占比2.2%。
染色体修复不好,胚胎长不下去,DNA修复故障,如REC114等基因,解释了17例,占比0.9%。
第一次分裂故障,比如BTG4和CHEK1基因问题导致胚胎连第一次分裂都完成不了,解释了11例,占比0.6%。
总之,这个研究清晰描绘了目前已知的基因影响卵子的8条关键生理通路,比如骨架搭建、指令传递、质量检查等,为临床诊断提供了详细的卵子方面遗传缺陷诊断路径。
04本次研究新发现的致病基因通过上面的数据我们解释了13.2%的因卵子缺陷导致的反复种植失败病例,那剩下的86.8%的卵子缺陷元凶又是谁呢?
于是研究进入到了第二个步骤,寻找新的嫌疑犯。
研究者采用病例-对照关联分析法,把病人的基因数据和健康人的基因数据对比,看哪些基因变异在病人中出现的频率显著更高。
研究者从超过1万个基因中,优先筛选出与生殖相关的4903个基因,再结合基因在卵子和胚胎中的活跃程度(表达量FPKM>10),最终锁定122个高度可疑的新基因。
为了证实这些新基因的嫌疑,研究者挑了其中5个(CNTD2,SPDYC,DDOST,INCENP,MLH3)做了严格的功能试验。
比如研究者把人的突变CNTD2基因注入小鼠受精卵,发现胚胎果然停止发育了;降低小鼠卵子中DDOST基因的量,发现卵子成熟受阻。
另外研究发现,TUBA1C基因的杂合变异在病人中富集程度最高,涉及19例,占队列的 0.63%,它也是微管蛋白家族成员,和TUBB8是同伙,嫌疑极大。
总之,通过这套组合拳,研究最终找到了123个(122隐性+ 1显性)新的候选致病基因,为未来的研究和诊断提供了宝贵的线索库。
从整个研究结果来看,这项研究就像一份极其详细的遗传侦探报告,它精确量化了已知病因,目前技术下13.2%的这类患者能通过基因检测获得明确诊断。
同时,这个研究指明了卵子缺陷的主要方向,TUBB8是首要检测目标。
通过这个研究我们也知道了卵子和胚胎发育的多个关键环节都有遗传因素的参与,基因缺陷情况比我们想象的要更加复杂。
另外,最新发现的123个新的候选基因将极大地推动未来的诊断技术和潜在治疗方法的发展。
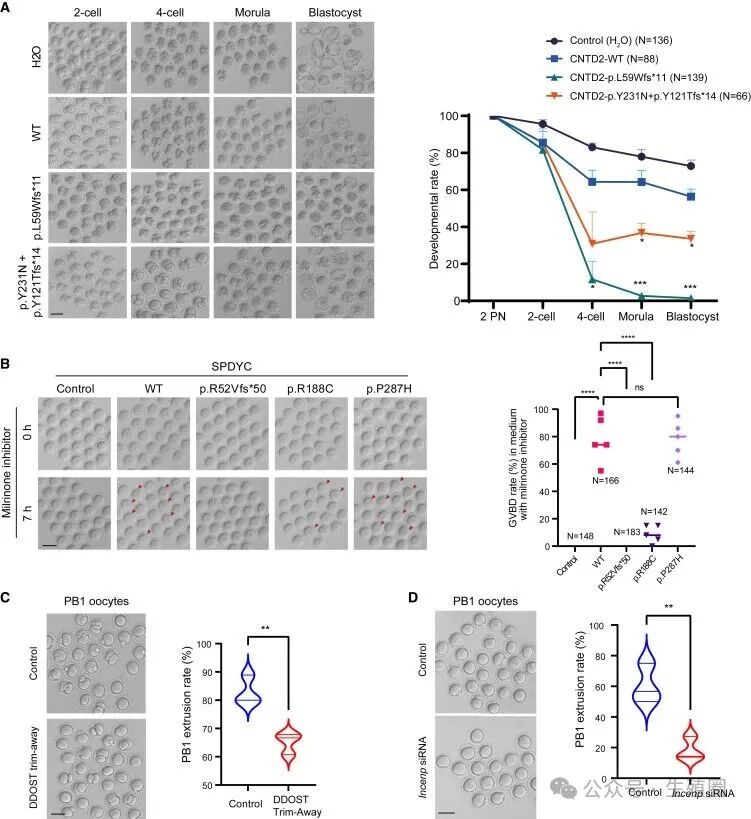 05这项研究的主要意义
05这项研究的主要意义在这项研究中明确显示,13.2%的病例能由已知基因解释,这远高于对照组1.2%,证明了进行基因诊断的必要性。
在研究涉及的3627个不孕患者中,研究者用已知的37个可能造成卵子缺陷的致病基因成功解释了479名患者的反复试管失败,占比13.2%;
但是在健康对照组的2868名女性中,携带这些致病基因的比例仅为1.2%,两者差距巨大,这强有力地证明了这些基因确实是不孕的元凶之一。
这项研究给出了一个明确的、量化的证据,对于因卵子/胚胎问题反复试管失败的患者,进行基因检测不是可选项,而是一个必要的诊断步骤。
过去面对反复失败的夫妻,医生常陷入试错循环——调整促排方案、更换培养条件,但收效有限。
通过这个研究,能帮助医生和患者避免盲目尝试,节省巨大的时间和经济成本。
有姐妹可能疑惑了,怀孕是夫妻双方的事,为什么这个研究把主要问题集中在妈妈身上?
这是因为无论卵子还是胚胎缺陷主要源于母体基因组,因为早期发育完全依赖卵子提供的养料,父源基因组至少要到囊胚才能启动。
未来通过精准的基因检测,可能可以明确患者导致反复种植失败的根本原因,而不是一直试错,比如目前能明确的就有:
携带TUBB8突变的患者,传统ICSI效果差,但采用卵母细胞激活技术或供卵可能更有效;
如果发现PADI6基因缺陷,需要警惕胚胎植入失败的风险,因为这个缺陷可能影响卵子透明带形成。
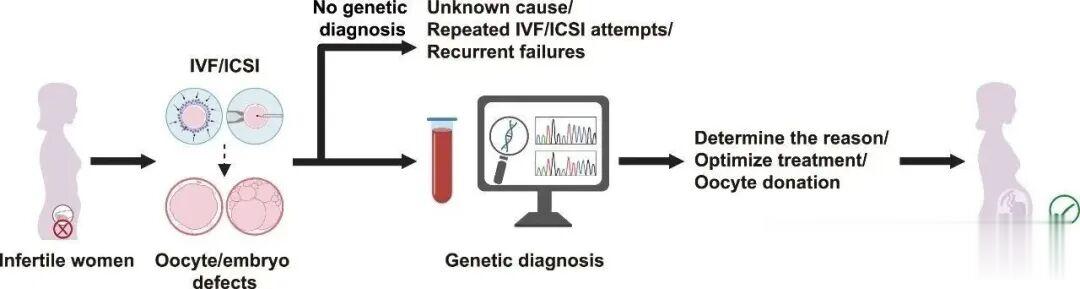
另外,对于新检出的123个基因缺陷,研究团队正在开发针对性的分子干预策略,未来的试管可能会针对卵子基因缺陷制定个性化方案。
长远来看,随着基因编辑等技术的发展,理论上存在未来纠正这些缺陷的可能性。
至少,它为针对特定基因问题的干预性药物或辅助生殖技术的研究打开了大门。

总的来说,这项研究的意义在于,它将一部分原因不明的反复移植失败,变成了病因明确的遗传性疾病。
它把一道无解的难题,变成了一个可以诊断、可以应对的医学问题,为无数在黑暗中摸索的家庭,点亮了一盏指路的灯。
当我们经历试管失败后,你可能已经听够了放宽心之类的苍白安慰,也受够了再试一次之类的隔靴搔痒式鼓励。
这项研究想告诉你的不是一个保证成功的魔法,而是一个确凿的答案,它想帮你结束那种为什么偏偏是我的追问。
当问题被定位到一个具体原因,才可能有相应的解决方案,你才能停止对自己身体的苛责,停止那些没有尽头的猜测。
总之,希望科学发展可以早一点造福反复试管失败姐妹,也许未来不再会有不明原因试管失败,期待这一天早日实现,加油!
全文完!现在流量为王的年代,围观也是一份力量,转发就是一份担当,希望动动您发财的小手,给我点个赞,如果您能转发到微信群或朋友圈,就会让更多孕育困难的小家庭受益,谢谢您!
郑重声明
本账号发表的内容仅作为科普分享,不对所引用文献的准确性和完整性作出任何承诺和保证,亦不承担因该内容已过时、所引用资料可能的不准确或不完整等情况引起的任何责任,请相关各方在采用或者以此作为决策依据时另行核查。本账号不做任何形式的营销推广,在采取任何预防或治疗措施前,请与你的医疗保健提供者沟通。
不传小道消息和谣言
不做只为转发量而存在的公众号
永远在意真实数据和文献论证
抱娃路上,我愿意陪你一起走过最无助的岁月
——THE END——
参考文献
Genetic landscape of human oocyte/embryo defects. Cell Genom. 2025 Sep 25:101012. doi: 10.1016/j.xgen.2025.101012. Epub ahead of print.