
免疫联合靶向或免疫治疗已经成为晚期肝癌一线标准治疗方案。近年来,研究者开始将免疫联合治疗前移至中期肝癌,即在TACE等介入治疗基础上联合应用此类新型药物,进一步展现了疗效提升的潜力。在万众瞩目的2024年ESMO大会首场主席研讨专场(Presidential Symposium I: Practice-changing trials)中,III期LEAP-012研究以重磅研究摘要(LAB3)口头报告的形式正式亮相,成为本次大会肝癌领域的吸睛焦点。《肿瘤瞭望》和《国际肝病》特邀该研究的中国PI之一、西安国际医学中心医院消化病医院执行院长韩国宏教授介绍和点评该研究。


△韩国宏教授在ESMO现场与Josep Llovet教授
研究简介经动脉化疗栓塞术联合或不联合仑伐替尼+帕博利珠单抗用于中期肝细胞癌的III期LEAP-012研究
背 景
经动脉化疗栓塞术(TACE)仍然是中期肝细胞癌(HCC)的标准治疗方法。LEAP-012研究是一项随机、多中心、双盲、III期试验,评估了仑伐替尼(Lenvatinib)+帕博利珠单抗(Pembrolizumab)+TACE对比双安慰剂+TACE在中期HCC中的疗效。
方 法
将无法根治且Child-Pugh A级、无门静脉侵犯、ECOG体能状态评分为0或1的HCC患者按1:1的比例随机分配至TACE联合仑伐替尼12 mg(体重≥60 kg)或8 mg(体重<60 kg)每日口服+帕博利珠单抗400 mg每6周静脉注射组,或TACE联合安慰剂口服+静脉注射组,治疗期最长为2年;仑伐替尼/口服安慰剂单独使用直至疾病进展或停药。首次TACE在全身治疗开始后2-4周内进行。随机分层因素包括:研究中心、甲胎蛋白 (≤400 ng/ml vs >400 ng/ml)、ECOG体能状态评分 (0 vs 1)、ALBI分级 (1 vs 2 或3)和肿瘤负荷 (6-and-12 评分,最大肿瘤直径+数目≤6 vs 6-12 vs >12)。主要终点是根据RECIST v1.1标准由独立盲态评审委员会(BICR)评估的无进展生存期(PFS)和总生存期(OS);使用分层Cox比例风险模型估计风险比(HR)和95%置信区间(CI)。
结 果
480例患者被随机分配至仑伐替尼+帕博利珠单抗组(n=237)或安慰剂口服+静脉注射组(n=243);两组患者均接受了TACE治疗。在本次首次中期分析中,从随机化到数据截止(2024年1月30日)的中位时间为25.6个月(范围:12.6-43.5)。仑伐替尼+帕博利珠单抗组的PFS显著优于安慰剂组(HR=0.66,95% CI:0.51-0.84;P=0.0002;显著性阈值:P=0.025);中位PFS分别为14.6个月(95% CI:12.6-16.7)和10.0个月(95% CI:8.1-12.2)。OS尚未达到显著性阈值(HR=0.80;95% CI:0.57-1.11;P=0.0867;显著性阈值:P=0.0012)。

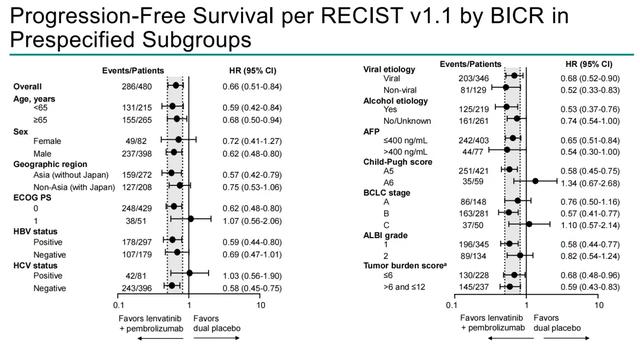

△该研究的PFS(BICR评估)K-M曲线、PFS亚组森林图、OS K-M曲线结果
两组患者根据RECIST评估的肿瘤客观反应率(ORR)分别为46.8%(95%CI:40.3-53.4)和33.3%(95%CI:27.4-39.6);根据mRECIST评估的ORR分别为71.3%(95%CI:65.1-77.0)和49.8%(95%CI:43.3-56.3)。仑伐替尼+帕博利珠单抗组中71.3%的患者发生了3-5级与治疗相关的不良事件(TRAEs),而安慰剂组为31.5%;TRAEs导致两组中分别有8.4%和1.2%的患者停用研究药物。
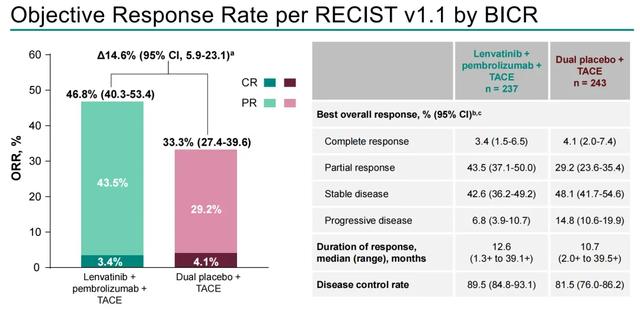


△该研究的ORR(根据RECIST和mRECIST标准)和常见不良事件结果
结 论
LEAP-012研究达到主要研究终点。仑伐替尼+帕博利珠单抗+TACE在中期HCC患者中显示出具有统计学意义和临床意义的PFS改善,并显示出OS改善的早期趋势。不良事件特征与已知的仑伐替尼、帕博利珠单抗和TACE的安全性特征一致。未来将进一步评估OS。
专家点评我国肝癌中晚期比例高,包括介入和药物的综合治疗探索积累了丰富的经验。能否介绍一下当前中晚期肝癌治疗现状或者您的临床实践经验?
韩国宏教授:中国是病毒性肝炎和肝细胞癌的高发国家,每年全球新增的肝癌患者中,有近一半病例发生在中国。尽管近年来,针对肝癌的治疗手段不断涌现并有所改进,包括一系列创新疗法的问世,但肝癌的治疗效果仍然远未达到临床的广泛需求,因此,肝癌依然是一个亟待深入研究和探索的肿瘤领域。
针对中晚期肝癌,尤其是那些因病情复杂而无法进行手术切除的患者,我们目前的治疗策略主要侧重于介入治疗和一系列局部治疗手段,如肝动脉化疗栓塞术(TACE)等,同时联合靶向疗法和免疫治疗,以期实现更全面的治疗效果。此外,随着医疗技术的进步,国内还引进了如钇-90微球放射栓塞治疗等前沿疗法,这些疗法在与靶向药物或免疫治疗联合使用时,已显示出能够延长患者的无进展生存期及总体生存期的潜力。
然而,我们必须认识到,尽管这些治疗实践为患者带来了一定的生存获益,但距离实现肝癌的彻底治愈或显著提高治疗效果的目标仍有较大差距。因此,我们急需开展更多深入的临床研究与实践,不断探索和优化治疗方案,以期在未来为肝癌患者带来更加显著和持久的生存改善。
本次大会报道了“可乐组合”联合TACE用于中期不可切除肝癌治疗的LEAP-012研究。您如何评价该研究所取得的结果?
韩国宏教授:LEAP-012是一项国际多中心、随机对照的III期临床试验,旨在探讨仑伐替尼和帕博利珠单抗(即“可乐组合”)联合TACE对比单独TACE,在不可切除中期肝癌治疗中的效果。我们知道“T+A”(阿替利珠单抗+贝伐珠单抗)或者“D+T”(度伐利尤单抗+曲美木单抗)等方案已经成为晚期肝癌一线标准治疗,研究者正试图将此类疗法前移至中期肝癌。尽管既往报道的LEAP-002研究没有取得阳性结果,但“可乐组合”一线治疗已经显示出无进展生存期(PFS)和总生存期(OS)延长的趋势。这促使研究者思考,是否能在TACE的基础上加入靶向与免疫疗法,以改善中期肝癌的治疗效果。因为过去20年,TACE一直是中期肝癌的标准治疗。
该研究从2020年5月开始入组,原计划入组960例患者,但因疫情等因素影响,至2023年下半年8月左右完成入组时,实际入组了480例患者。研究分为两组:一组接受仑伐替尼联合帕博利珠单抗加TACE治疗(n=237),另一组接受双安慰剂加TACE治疗(n=243)。今年1月30日进行的中期分析结果显示:联合治疗组的中位PFS从对照组的10.0个月显著延长至14.6个月,HR值为0.66,P值为0.0002,达到了统计学上的显著性差异。OS数据尚未达到统计学差异尚不成熟,需进一步观察。值得一提的是,该研究采用了我本人及其他学者提出来的“6 and 12”标准,即肿瘤数目加上最大肿瘤的直径之和超过6的患者,OS获益趋势更明显,这跟up-to-7标准也比较接近。此外,联合治疗的客观缓解率(ORR)也从对照组的33.3%提升至联合组46.8%。在安全性方面,联合治疗组的治疗相关不良反应较对照组有所增加,但主要集中在靶向治疗相关的高血压、蛋白尿等,且这些不良反应均为可控的。因此,该研究结果表明,联合治疗在疗效上展现出显著优势,同时其安全性也是可接受的。
综上所述,LEAP-012研究的结果可能改变临床实践,将中期肝癌的单独TACE治疗转变为TACE联合靶向与免疫疗法的综合治疗,以期为患者带来更长的生存获益,期待未来OS数据的进一步改善。同时,该治疗方案的安全性也经过验证,是可耐受和可管理的。
既往报道晚期一线治疗的LEAP-002研究没有取得阳性结果;而此次LEAP-12研究取得了阳性结果,您如何看待二者的差异?
韩国宏教授:LEAP-002研究探讨的是“可乐组合”对比单药仑伐替尼用于晚期肝癌一线治疗的疗效和安全性。虽然整体上得到阴性结果,但我们可以看到“可乐组合”相较于单药仑伐替尼的生存获益趋势。造成阴性结果的原因可能是研究选择的对照组仑伐替尼相较于索拉非尼等其他TKI的疗效更强,所以我们在该研究中可以看到,“可乐组合”的中位OS长达21.1个月,而仑伐替尼单药组的OS也达到了19.0个月。“可乐组合”所展现的治疗效果和生存获益趋势是有目共睹的,所以研究者进一步考虑到,如果应用在中期肝癌患者中,在TACE标准治疗基础上联合“可乐组合”的三联疗法,或可进一步增强治疗效果,而LEAP-012研究结果也进一步验证了这一设想。
中期肝癌的综合治疗涉及手术治疗、内科治疗、介入治疗等多学科,一些不良反应的处理还需要其他学科干预。您如何评价LEAP-012研究中的安全性结果?
韩国宏教授:该研究中,虽然联合治疗组的3-5级AE发生率有所升高(71.3% vs 31.1%),但总体上是可以管理和控制的,最终仅有少数患者因为不良事件导致停药(8.4% vs 1.2%)。联合治疗组较为常见的不良事件包括高血压、蛋白尿、肝酶升高、血小板计数增加,这些不良事件和LEAP-002研究结果总体保持一致。当然,在临床应用中,我们还是需要尝试给患者做减法。在不太影响疗效的同时,尽量减少药物的暴露引起的不良反应和经济学毒性。我们在临床实践中已经在探索靶免联合TACE治疗中期乃至晚期肝癌,无论是药物相关不良事件还是介入相关不良事件,临床预防和处理也将越来越成熟,积累了丰富的管理经验,尤其是在多学科团队(MDT)参与下,能够进一步提高我们对不良反应管理的信心。