前列腺导管内癌(IDC-P)是一种前列腺癌亚型,表现为预后较差。以往研究表明,IDC-P可能存在潜在的不稳定基因组。同源重组缺损(HRD)评分是一种以结果为导向的方法,用于描述基因组不稳定性状态。本文将探讨HRD评分与IDC-P及其他临床病理因素的关联,以及HRD评分在侵袭性前列腺癌队列中的预后影响。

基因组不稳定是癌症的标志。同源重组缺陷(HRD)显著影响基因组不稳定,并可被多元ADP核糖聚合酶抑制剂(PARPis)靶向。
PARPis在卵巢癌、乳腺癌、胰腺癌和前列腺癌(PCa)中的治疗效果已被认可。然而,目前的检测方法尚不足以识别所有对PARPi敏感的患者。HRD确实是一个正当的治疗目标,但在准确定义HRD方面仍有疑问。
约20%的PCa患者表现出DNA损伤修复(DDR)基因缺陷,且他们可能携带更具侵袭性的疾病特点[1]。
尽管生殖系DDR基因,尤其是BRCA突变,仍被公认为PARPi使用的临床预测因子,但DDR突变不足以全面描述患者的HRD状态。
此外,DDR突变的基因组检测存在一些固有的限制:回归突变、表观遗传调控以及其他基因的潜在预测性突变,尤其是在PCa中,双等位基因仅由体细胞基因缺失时较为显著[2]。
然而,PCa中详细的HRD分数分布尚未明确。目前的泛性研究显示关于PCa的结果存在矛盾[3]。对PCa中HRD评分的深入理解将有助于更好地对患者进行HRD靶向疗法的分层。此外,PCa在病理亚型方面具有异质性,而这些方面似乎研究不足。相关研究报告了不同PCa病理亚型之间的预后和分子差异[4]。值得注意的是,除了与阴性临床病理特征和预后不佳的关联外,前列腺导管内癌(IDC-P)在基因组和转录组特征上与腺窦腺癌(AC)并不相同。以往研究表明,IDC-P中基因组异常比例更高[5]。因此,推断可能含有IDC-P成分的肿瘤基因组疤痕增加,从而表现出较高的HRD评分。
华西医院研究人员对123名PCa患者,包括高风险局部性(M0)和新发转移性(M1)患者进行HRD评分与IDC-P及其他临床病理因素的关联,以及HRD评分在侵袭性前列腺癌队列中的预后影响的探讨。本次HRD评分基于分布在人类基因组中的超过10,000个单核苷酸多态性计算。研究人员通过秩和检验、卡方检验、Kaplan-Meier曲线和Cox比例风险法,探讨了HRD评分与临床病理特征、基因组变化及患者预后之间的关联。为了评估基因组瘢痕,使用基于分布在人类基因组中的超过10,000个单核苷酸多态性开发了3DMed-HRD算法[6],这些多态性也被纳入156和733基因NGS检测中。HRR通路基因的指定基于以往研究。本研究中的所有突变均指有害或疑似有害突变。
本队列的HRD中位数得分为21.0,其中65名(52.8%)患者表现出HRD评分≥21。IDC-P肿瘤的HRD评分高于腺癌;其他高HRD分数相关因素包括M1和ISUP高评分(4–5)。MYC突变与整体队列中高HRD得分相关。TP53突变和HRR通路突变分别对应IDC-P阳性和非IDC-P患者的高HRD分数,反之则不然。HRD得分高于21的表现为整体队列生存率显著较差。高HRD得分(≥21)与较短的CFS相关(22.6个月对32.8个月,P=0.004)。
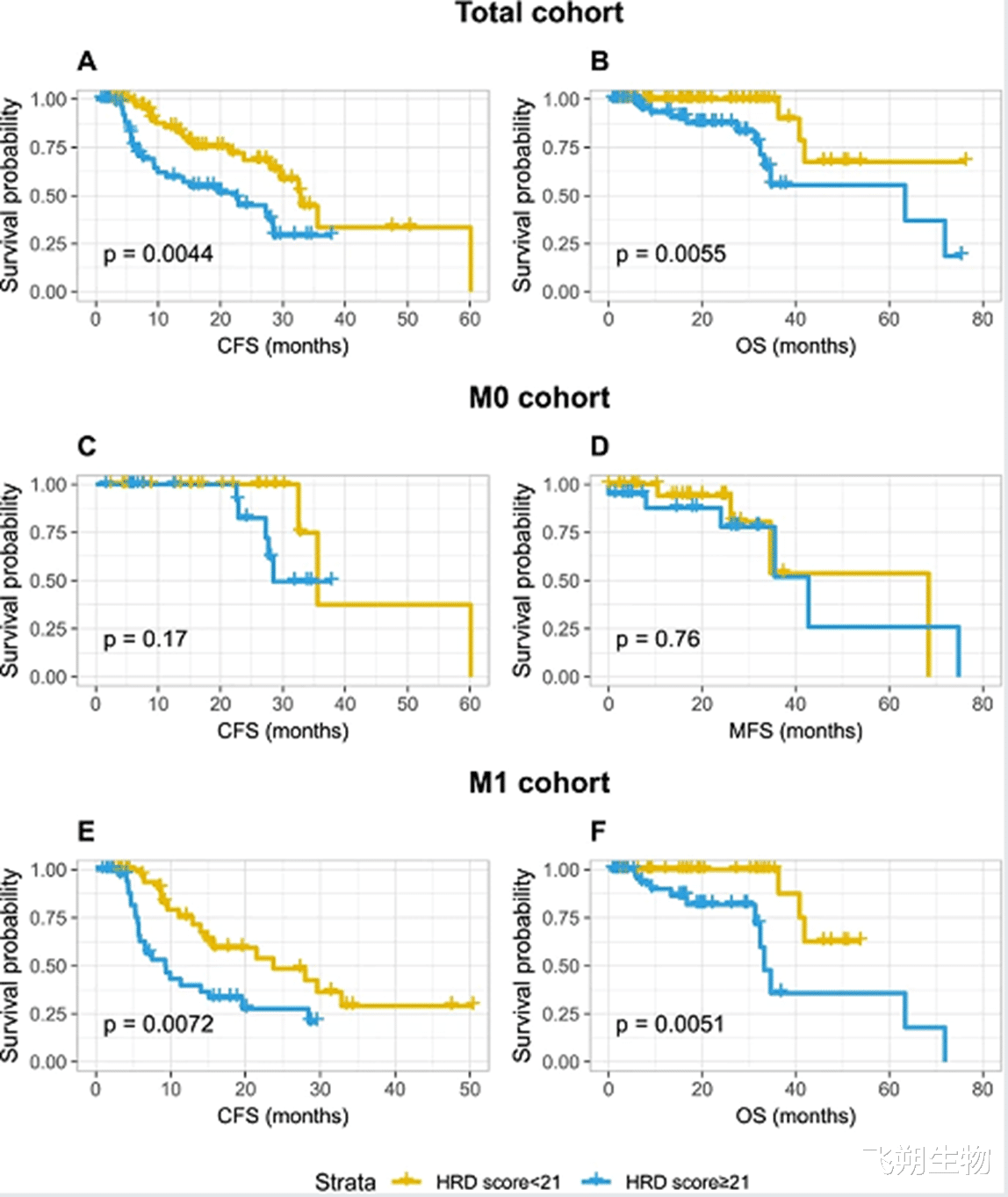
▲HRD评分的预后价值
Part2研究结果M1、ISUP高评分和IDC-P病理分型可能代表PCa中HRD评分较高。IDC-P的肿瘤患者可能具有与非IDC-P不同的高HRD评分的驱动机制。HRD评分在这一积极的前列腺癌队列中显示出预后价值。
Part3总结该研究首先报告指出,含有IDC-P成分的患者在HRD评分上显著高于AC。通过使用包含局限性和转移患者的队列,研究人员发现M1患者比M0患者更可能表现出更高的HRD评分。除HRR途径外的基因突变(MYC和TP53)也表现在PCa中的HRD评分较高。HRR通路基因改变主要驱动无IDC-P患者的高HRD评分表型,而TP53突变则仅指示IDC-P患者中的高HRD评分。这种差异此前未曾被观察到,可能具有重要的分子意义。此外,发现HRD高评分的患者在侵袭性前列腺癌中生存率更差。IDC-P患者中高HRD分数可能由TP53改变引起。这一发现进一步凸显了不同PCa病理亚型之间基因组维持机制可能存在的异质性。因此,IDC-P在染色体不稳定性的驱动突变上可能与AC存在差异。
即使HR功能恢复,已有的基因组疤痕也不太可能消失。因此,强烈建议高危患者在疾病早期阶段进行HRD检测,并在疾病进展时最好重复检测。新发转移性PCa患者及IDC-P或高ISUP评分患者HRD评分较高。IDC-P患者的HRD状态可由除HRR通路以外的异常因素引起。建议高风险前列腺癌患者进行HRD评分检测,因为该结果在侵袭性前列腺癌中可以作为有用的预测和预后标志。
参考文献
[1] Cell. 2019;176(4):831–43.e22.
[2] Prostate. 2018;78(5):401–7.
[3] Nucleic Acids Res. 2004;32(Database issue):D493–6.
[4] Ann Oncol. 2020;31(4_suppl);S790.
[6] Br J Cancer. 2012;107(10):1776–82.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!