上皮性卵巢癌(EOC)因确诊时多为晚期、复发率高且治疗选择有限,临床治疗面临诸多挑战。有80%的患者出现复发,其中位生存期仅为2年。患者5年总生存率仅约40%,预后极差,凸显出对创新疗法的迫切需求。
采用异基因自然杀伤(NK)细胞的过继性细胞治疗是极具潜力的方案,因NK细胞无需预先致敏即可介导对肿瘤细胞的细胞毒作用。NK细胞疗法可区分正常细胞与肿瘤细胞,并对肿瘤细胞发挥强效细胞毒作用,是一种极具前景且安全性良好的治疗选择。
2026年1月,来自荷兰拉德堡德大学医学中心(Radboud University Medical Center)的研究人员及其合作者在《Gynecologic Oncology》杂志上发表了题为《Intraperitoneal infusion of stem cell-derived natural killer cells in recurrent epithelial ovarian cancer patients: Results of the phase 1 INTRO-01 trial》的文章,这项1期试验(NCT03539406)评估了源自脐带血造血干细胞和祖细胞(HSPC)、经体外制备的NK细胞制剂RNK001的安全性。

研究设计
这项研究为首次人体试验,旨在探讨对第二次复发且CA125水平升高的上皮性卵巢癌患者,经腹腔(IP)输注RNK001的可行性、安全性及毒性。在研究中,6例患者在接受腹腔输注RNK001的同时联合腹腔给予了IL‑2。1例患者在输注RNK001前接受了环磷酰胺/氟达拉滨(Cy/Flu)进行淋巴清除化疗。
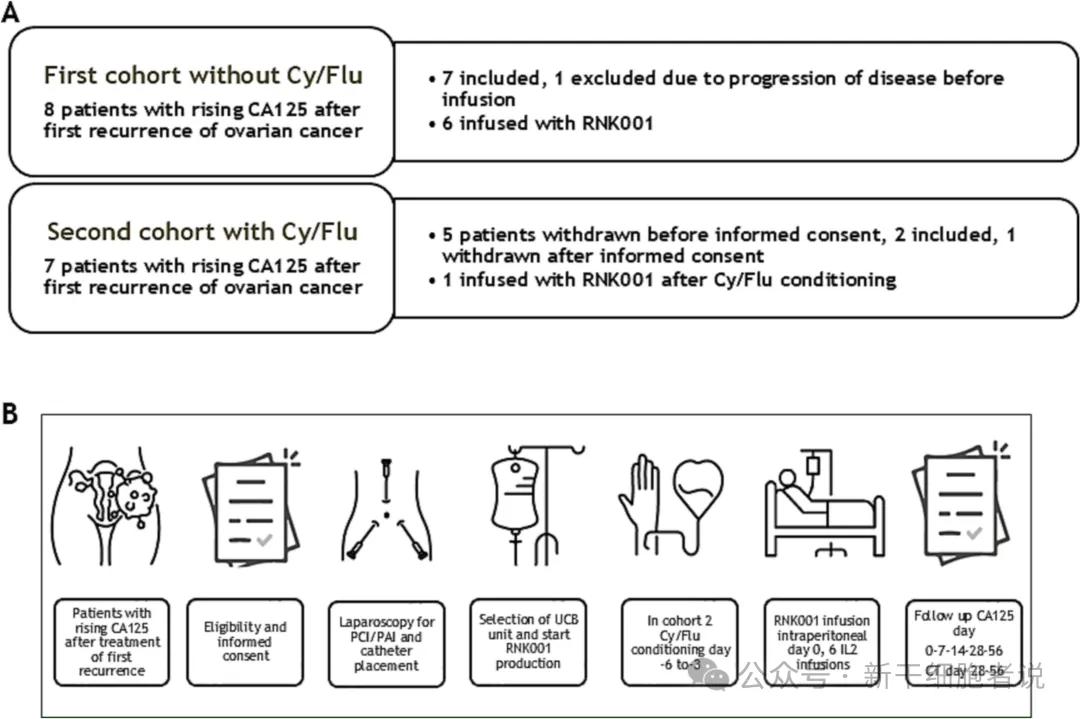
患者纳入及研究流程
1. 免疫与生化评估:于特定时间点采集外周血(PB)和腹腔液(PF),检测PB的血细胞计数、CA125、细胞因子及T/B/NK细胞组成,分析PF的NK和T细胞比例;2. HLA-KIR分型及HLA抗体检测:采用PCR-SSOP和Luminex技术完成分型与抗体筛查;
3. 嵌合状态分析:通过定量PCR检测,灵敏度达0.1%,所有检测均在ISO15189认证实验室进行。
结果分析
RNK001制剂含1.2×10⁹~3.0×10⁹个高度活化的CD56⁺CD3⁻NK细胞。

RNK001产品信息
患者整体耐受性良好,未出现NK细胞相关毒性、移植物抗宿主病或细胞因子释放综合征。6例患者输注IL‑2后出现发热、寒战,经对乙酰氨基酚治疗后缓解。1例患者出现3级一过性肝酶升高,另1例患者因疾病进展出现3级肠梗阻。
腹腔液获取困难,6例可采集样本,3例检测到供体NK细胞嵌合(0.24%,0.78%,1.02%),流式可见高活化NK细胞。IL‑2使外周血淋巴细胞亚群一过性升高,预处理化疗可致淋巴细胞减少后恢复。部分患者治疗后HLAⅠ类抗体升高。
值得关注的是,7例患者中有5例在输注后14天,血清CA125水平下降20%~53%。其中,1例患者获得临床及生化缓解,影像学评估为疾病稳定,无进展生存期达9个月。

RNK001细胞治疗对INTRO‑07号患者CA125及肿瘤病灶的影响
小结
这些结果表明,复发性上皮性卵巢癌患者可安全接受腹腔输注RNK001的免疫治疗,且未发生严重毒性反应。输注后第14天患者的CA125水平显著降低。1例患者获得临床及生化缓解,影像学评估为疾病稳定。其临床与生化缓解获益支持该疗法的进一步研发。
尽管NK细胞疗法在血液系统恶性肿瘤中的研究已较为充分,但在上皮性卵巢癌中的临床证据仍十分有限。已有多项试验评估了静脉输注NK细胞疗法在上皮性卵巢癌中的应用,其中APOLLO试验证实,腹腔输注该疗法对复发性上皮性卵巢癌患者具有潜在疗效。本研究进一步证实,无需环磷酰胺/氟达拉滨预处理,腹腔输注RNK001同样可带来临床获益。
卡铂-紫杉醇(CP)铂类化疗是上皮性卵巢癌的标准治疗方案,或可作为一种更安全的淋巴清除策略,为免疫治疗创造窗口期,同时还能降低调节性T细胞(Treg)及免疫抑制性髓系细胞的比例,潜在增强NK细胞的抗肿瘤效力。
此外,CP化疗可通过充分清除宿主B细胞和CD4+辅助性T细胞,抑制HLAⅠ类抗体水平升高。这一作用尤为重要,这项研究中观察到,未接受环磷酰胺/氟达拉滨预处理的异基因RNK001治疗患者出现了HLAⅠ类抗体升高,而该现象可能阻碍输注后NK细胞的存活与扩增。
总之,这种基于造血干细胞和祖细胞来源NK细胞的免疫治疗(RNK001),有望联合化疗用于铂敏感复发性上皮性卵巢癌患者,作为一种补充治疗方案。
— END —

新干细胞者说
- 科普 情怀 责任 -