56岁的张阿姨患糖尿病十年,没想到“拖”出了非酒精性脂肪肝(NAFLD)。B超显示肝脏弥漫性脂肪浸润,肝功能指标ALT飙升至正常值3倍,血糖也因脂肪肝引发的胰岛素抵抗居高不下。传统降糖药和保肝药效果有限,医生建议她做好“长期抗争”准备。然而,一次肠菌移植(FMT)治疗让她肝脏和血糖同时“转危为安”:3个月后,肝脏脂肪含量下降52%,ALT恢复正常,血糖波动幅度缩小40%。这一案例揭示了糖尿病合并脂肪肝的深层联系,也展现了FMT作为“肝脏清道夫”的独特价值。
糖尿病与脂肪肝:代谢灾难的双重暴击
NAFLD是糖尿病常见共病,二者互为因果,形成恶性循环。糖尿病加速脂肪肝,高血糖和胰岛素抵抗使脂肪分解增加,游离脂肪酸大量涌入肝脏,超出其代谢能力,形成脂肪堆积。脂肪肝恶化糖尿病,肝脏脂肪变性释放炎症因子,加剧胰岛素抵抗,让血糖更难控制。此外,糖尿病胃肠神经性病变引发的便秘或腹泻,会破坏肠道菌群平衡,增加内毒素入血,直接损伤肝脏。
张阿姨就是典型案例,她长期便秘,肠道菌群中产生内毒素的大肠杆菌比例高达40%,保护肝脏的双歧杆菌不足5%。内毒素通过“肠 - 肝轴”进入肝脏,激活炎症通路,加速脂肪沉积,最终形成“糖尿病 - 菌群紊乱 - 脂肪肝”的三重困境。
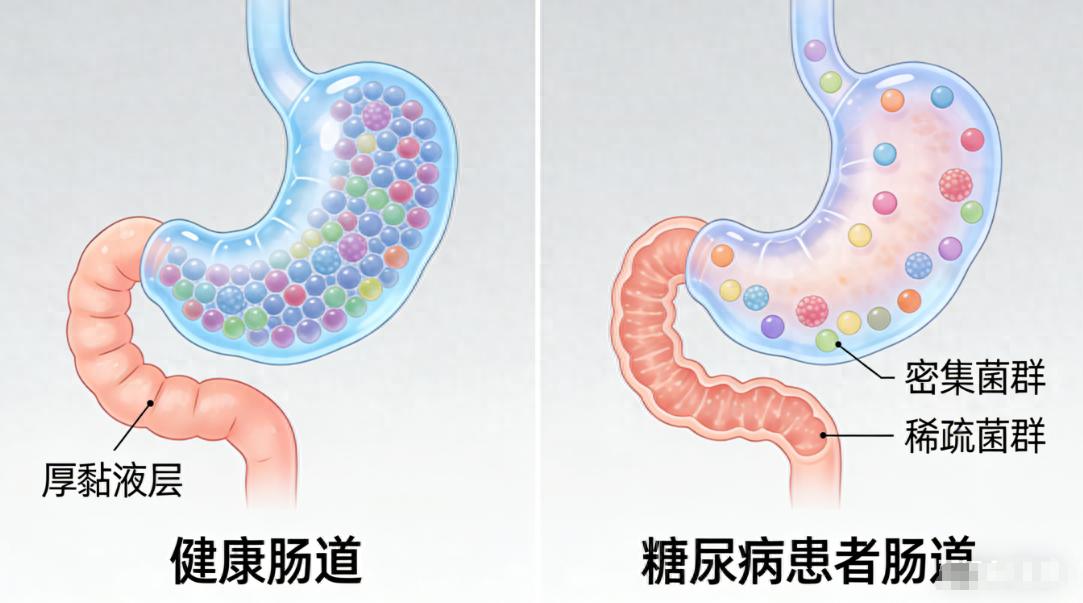
脂肪肝的“菌群密码”:肠道是肝脏第一防线
近年研究证实,肠道菌群是连接糖尿病与脂肪肝的关键枢纽,其“三重屏障”崩溃会导致脂肪肝。 一是物理屏障“溃堤”。健康肠道黏液层由产丁酸盐菌分泌的黏蛋白构成,可阻挡内毒素和细菌入血。但糖尿病患者这类菌群减少,黏液层变薄,形成“肠漏”。 二是化学屏障“断供”。丁酸盐等短链脂肪酸是肠道上皮细胞的“能量燃料”,能维持黏液层分泌并抑制炎症因子产生。糖尿病合并脂肪肝患者粪便中丁酸盐含量常低于健康人的30%,导致肠道和肝脏双重炎症。 三是免疫屏障“失职”。健康菌群可诱导肠道免疫系统产生调节性T细胞(Treg),抑制过度炎症反应。菌群紊乱时,促炎的Th17细胞占优,内毒素入血后激活肝脏库普弗细胞,释放大量炎症因子,加速脂肪肝进展。
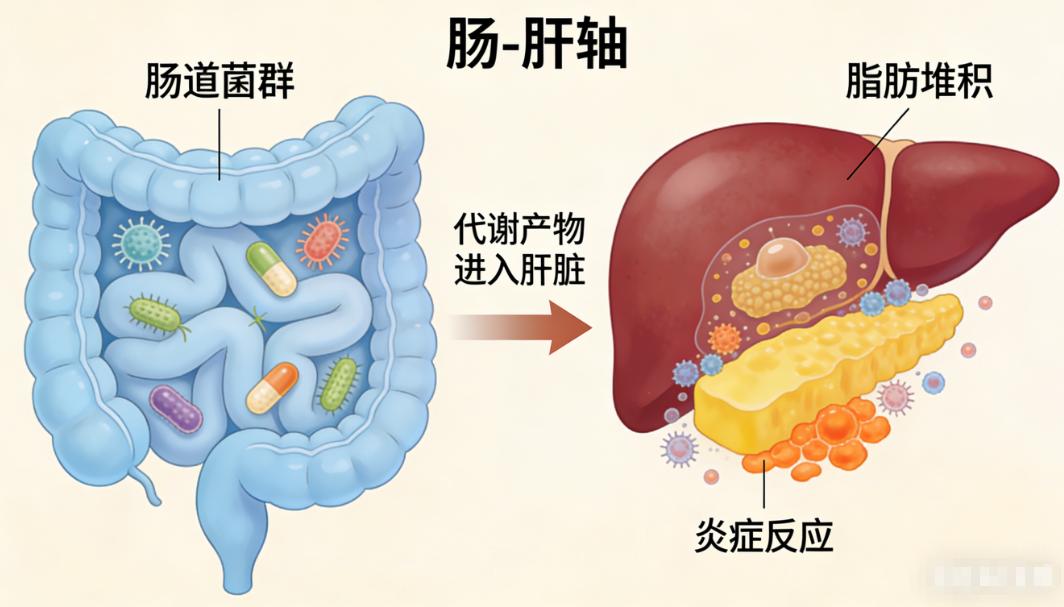
FMT:派遣“特种部队”修复肝脏生态
FMT通过移植健康供体肠道菌群,从三个层面“重建防线”,逆转脂肪肝。 一是补充产丁酸盐菌,厚植物理屏障。供体菌群中的罗斯氏菌、粪杆菌等迅速定植,分泌大量丁酸盐,修复受损肠道黏液层。研究显示,FMT后患者肠道黏液厚度增加2倍,内毒素入血减少60%。 二是提升SCFA水平,阻断炎症通路。丁酸盐能强化肠屏障,通过“肠 - 肝轴”直接作用于肝脏,抑制库普弗细胞活化,减少炎症因子释放,促进脂肪酸氧化,减少肝脏脂肪堆积。张阿姨治疗后,粪便丁酸盐含量大幅上升,肝脏脂肪含量随之下降。 三是调节免疫平衡,重建耐受环境。FMT可诱导肠道Treg细胞增殖,抑制Th17细胞过度活化,形成“抗炎微环境”,减少肝脏炎症,改善糖尿病患者全身免疫状态,降低感染风险。
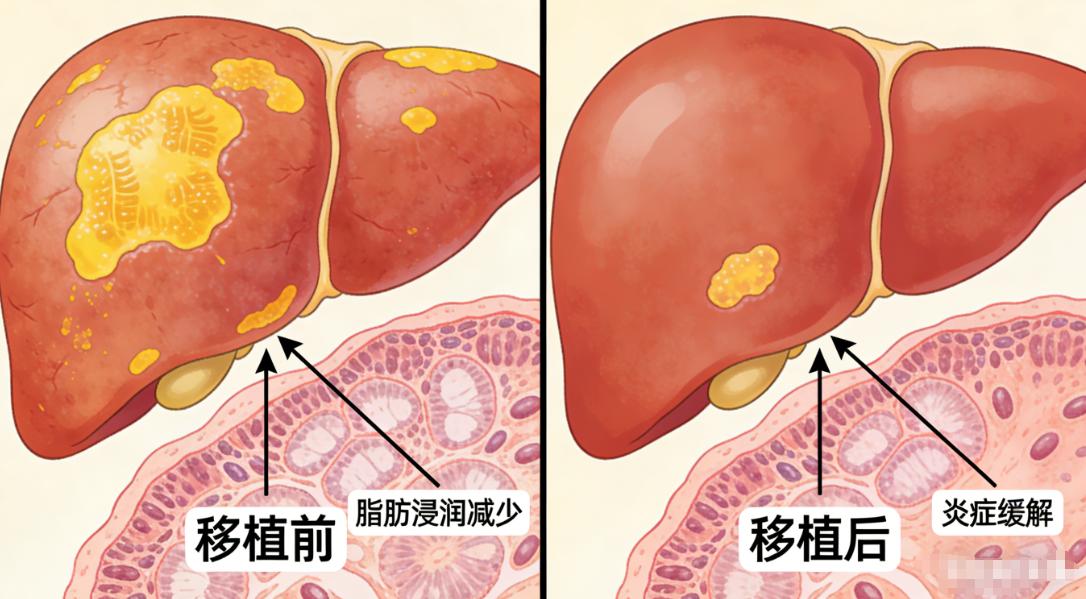
张阿姨的成功并非孤例。上海交通大学医学院附属瑞金医院团队追踪显示,FMT联合生活方式干预6个月后,82%患者肝脏脂肪含量下降≥30%,60%患者ALT恢复正常,胰岛素敏感性提升25%。不过,FMT普及仍需突破供体筛选、个性化方案、长期管理三大瓶颈。
专家预言,未来FMT可能与二甲双胍、GLP - 1受体激动剂形成“组合疗法”,从“控制血糖”转向“修复代谢生态”。对于糖尿病合并脂肪肝患者,这或许意味着无需再忍受“降糖药 + 保肝药”的双重负担,而是通过一剂“肝脏特种部队”,同步逆转血糖和肝脏损伤。
当医学从“对抗疾病”转向“调和菌群”,FMT正成为糖尿病共病治疗新范式。它让我们明白,脂肪肝是肠道菌群、代谢和免疫系统失衡的“交响曲”,重建肠道微生态,才能实现真正的“标本兼治”。