癌症免疫治疗包括一系列当前和具有前景的治疗策略,其目的是通过激活宿主的抗肿瘤免疫反应来根除肿瘤。美国食品药品监督管理局(FDA)已批准免疫检查点阻断(ICB)疗法和嵌合抗原受体(CAR)工程化T细胞免疫疗法,这些疗法显著改善了癌症治疗,但并非对所有癌症患者都有效。而癌症疫苗论是单独使用还是联合使用,都具有预防和治疗的潜力,有望成为未来联合免疫治疗的重要组成部分。
关于癌症疫苗
疫苗是一项至关重要的公共卫生干预措施,由于肿瘤细胞上某些抗原的异常高表达或独特表达,疫苗作为一种治疗手段展现出良好的应用前景。
与免疫系统很容易识别为入侵者的病毒不同,癌症是由自己的细胞产生的,发生突变和增殖。它已经进化出逃避我们免疫系统的复杂方法。因此,免疫系统很难区分癌细胞和健康细胞,经常无法产生足够大的反应,导致癌症在未被发现的情况下扩散。
而癌症疫苗的目的在于“教育”患者的免疫系统,使其能够识别并攻击恶性细胞。十年前,首个基于树突状细胞、用于治疗前列腺癌的治疗性癌症疫苗Provenge®(sipuleucel-T)的获批,为治疗性癌症疫苗领域带来了极大的鼓舞。这一成功证明了抗癌疫苗确实可以发挥作用。

分类
目前,科学家正在探索多种技术手段,包括肽疫苗、DNA疫苗、mRNA疫苗、树突状细胞(DC)疫苗和以修饰病毒为载体的疫苗。
肽类疫苗:这些疫苗由癌细胞中的特定蛋白质或这些蛋白质的小片段(称为肽)制成。目的是刺激免疫系统攻击携带这些蛋白质的癌细胞。
DNA/RNA疫苗:这种疫苗使用从癌细胞中提取的少量遗传物质,如DNA或RNA。当注射到体内时,这种遗传物质将“教会”人类细胞产生特定的蛋白质,从而激活免疫系统来识别和攻击癌细胞。简单地说,它们为人体产生能够引发免疫反应的蛋白质提供了“制造说明”。
mRNA代表“信使RNA”。它是我们细胞的天然部分,携带来自我们部分DNA(我们的基因)的一组临时指令。它告诉细胞如何制造某种蛋白质,然后将其分解。
新冠mRNA疫苗的成功,让研究人员的目光投向了更加复杂、难搞的“癌症”。与用于预防的新冠mRNA疫苗不同,用于癌症的mRNA疫苗旨在治疗,但是他们的原理是相同的:利用信使核糖核酸(mRNA)分子来促使机体产生蛋白质,这些蛋白质能够激活免疫系统,使其攻击外来入侵者(如新冠病毒)或异常细胞(如肿瘤细胞)。
当mRNA疫苗注射入体内后,会进入细胞,并向细胞发出临时指令,让细胞制造一种或多种存在于癌细胞表面的蛋白质。随后,免疫系统就能学会将这些蛋白质识别为“标志物”,并攻击携带这些标志物的癌细胞。
树突状细胞(DC)疫苗:树突状细胞(DC)是人体内功能最强的抗原提呈细胞,它能够高效地摄取、加工处理和递呈抗原,激活T细胞,从而启动、调控和维持机体的免疫应答。DC肿瘤疫苗利用DC细胞提呈抗原、激活免疫的功能,借助DC细胞来指挥T细胞。通过体外诱导或构建特异性识别肿瘤的DC细胞,并将其扩增后回输到肿瘤患者体内,激活T细胞,对癌细胞进行有效杀伤,从而达到治疗肿瘤的目的。
意外发现:新冠mRNA疫苗或能提升抗癌疗效
近日,《自然》杂志发表了德克萨斯大学MD安德森癌症中心研究人员领导的一项新研究,在开始接受免疫检查点治疗后的100天内接种了基于mRNA的新冠疫苗的癌症患者,在治疗开始三年后存活的可能性是未接种者的两倍。

这项研究纳入了多个癌种的多个队列,评估了在治疗开始后100天内接种mRNA疫苗的患者。在第一组中,180例接受疫苗的晚期非小细胞肺癌患者的中位生存期为37.33个月,而704例未接种疫苗的患者中位生存期为20.6个月。在转移性黑色素瘤患者队列中,未接种疫苗的167例患者中位生存期为26.67个月,而接种疫苗的43例患者中位生存期尚未达到,提示存在显著改善。
尤其值得注意的是,这些生存获益在免疫学上属于“冷肿瘤”的患者中最为显著,这类患者的肿瘤通常对免疫治疗反应不佳。这些肿瘤PD-L1表达极低的患者,在接种新冠疫苗后,其三年总生存率提高了近五倍。

新型癌症疫苗联合疗法公布积极数据
近日,2025年欧洲肿瘤内科学会(ESMO)年会即将在德国柏林召开。此次会议上公布了联合帕博利珠单抗用于不可切除或转移性(晚期)黑色素瘤患者的一线治疗的3 期试验 (IOB-013/KN-D18)结果。
Cylembio是一种现成的治疗性癌症候选疫苗。这项3期试验有407 名既往未经治疗的晚期黑色素瘤患者接受了Cylembio联合治疗方案(n=203)或单独帕博利珠单抗(n=204)治疗。结果显示:
联合治疗的客观缓解率(ORR)为44.8%,其中34例完全缓解(CR),57例部分缓解(PR),38例病情稳定(SD)。单独帕博利珠单抗客观缓解率(ORR)为41.2%,37例完全缓解(CR),47例部分缓解(PR),36例病情稳定(SD)。

联合治疗的中位无进展生存期为19.4个月,帕博利珠单抗的中位无进展生存期为11.0个月。

在几乎所有亚组中,无进展生存期(PFS)的结果均一致倾向于联合治疗方案,包括PD-L1阴性肿瘤患者(16.6个月 VS 3.0个月)、BRAF V600突变肿瘤患者以及乳酸脱氢酶(LDH)升高的患者。

该联合治疗方案耐受性良好,与帕博利珠单抗单药治疗相比,免疫介导的不良事件发生率(34.0%对比38.4%)或≥3级治疗相关不良事件(14.5%对比15.6%)均未增加。
该试验表明,IO102-IO103联合帕博利珠单抗在无进展生存期方面具有临床意义的改善。
临床新证:联合疗法在肺癌、头颈癌中显成效
此次会议上还公布了Cylembio联合帕博利珠单抗用于一线治疗非小细胞肺癌(NSCLC)及头颈部鳞状细胞癌(SCCHN)患者的II期IOB-022/KN-D38试验的最终数据。
在49例可评估患者中,31例为非小细胞肺癌患者,18例为头颈部鳞状细胞癌,结果显示:非小细胞肺癌患者中位无进展生存期为8.1个月,头颈部鳞状细胞癌患者为7.0个月,且缓解持久,中位总生存期(OS)分别为22.6个月和22.3个月,18个月的总生存率(OS)结果令人鼓舞,分别为64%和61%。
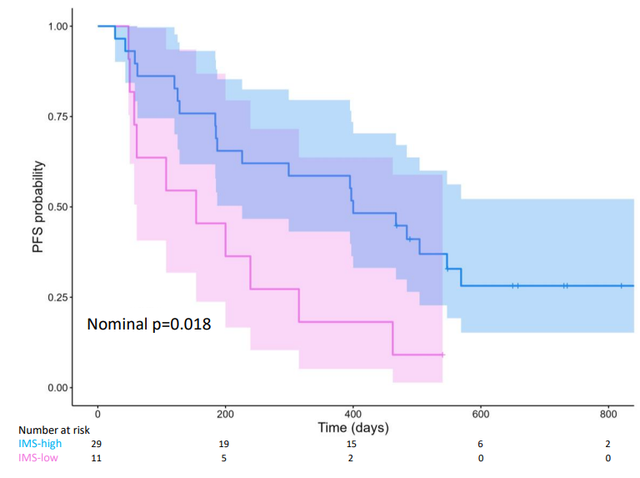
综上可见,Cylembio联合帕博利珠单抗在多癌种中具有治疗前景。
结语
癌症疫苗是一种具有吸引力的治疗方式,有大量证据表明癌症疫苗能够在部分患者中激活免疫系统并产生抗肿瘤活性,为癌症患者带来了新的希望。近期使用个性化癌症疫苗的临床试验数据令人备受鼓舞,但遗憾的是,并非所有患者都能从中受益。仍需开展更多临床试验来全面确认癌症疫苗的安全性和有效性。随着持续的研究和投入,癌症疫苗有望成为癌症患者的一种变革性治疗手段。