关键词: 阿尔茨海默病,仑卡奈单抗(lecanemab),真实世界研究,日本处方模式,轻度认知障碍,治疗中断率,LIFE研究,老年女性,医保与准入
Keywords: Alzheimer's disease, lecanemab, real-world evidence, Japan prescribing patterns, mild cognitive impairment, discontinuation rate, LIFE study, elderly women, insurance coverage
「期刊名: 《Alzheimer's & Dementia: Diagnosis, Assessment & Disease Monitoring》影响因子(IF): 4.4,分区(JCR): Q1
标题: 仑卡奈单抗处方规律的初步真实世界经验——日本LIFE研究(Initial real-world experience with lecanemab prescribing patterns in Japan: The Longevity Improvement Fair Evidence (LIFE) Study)
第一作者及单位: Takaaki Mori,日本国立长寿医疗研究中心(National Center for Geriatrics and Gerontology,NCGG),日本爱知县
发表时间: 2025年3月(在线发表)
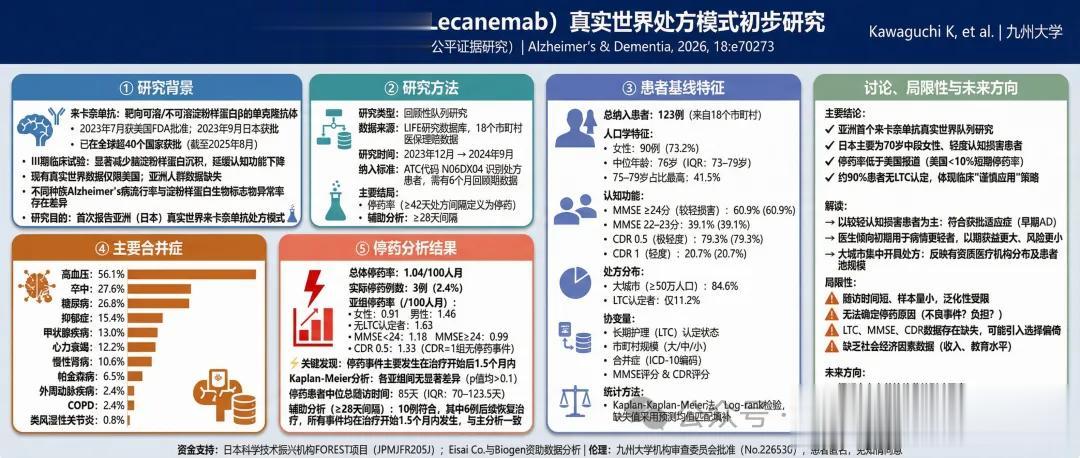
主要结论概要: 本研究基于日本18个市区町村的医疗保险理赔数据,纳入2023年12月至2024年9月间共123名接受仑卡奈单抗处方的患者(中位年龄76岁,女性占多数),发现处方群体以轻度认知障碍(MCI)及轻度AD为主(60.9%患者MMSE≥24,79.3%患者CDR为0.5)。这是首个来自亚洲的仑卡奈单抗真实世界应用数据,证实该药在日本临床实践中的患者选择高度符合适应症规范,体现了日本应用仑卡奈单抗治疗AD的出色效果。」

 研究背景:首个亚洲真实世界证据的来源与意义
研究背景:首个亚洲真实世界证据的来源与意义仑卡奈单抗(lecanemab,商品名LEQEMBI®)是全球首个被证明能够显著减缓AD进展的疾病修饰疗法(DMT),其于2023年1月获美国FDA加速批准、同年7月获美国FDA完全批准,2023年9月在日本获批——成为继美国之后全球第二个批准该药的国家,并于同年12月启动正式处方[1][2]。截至2026年初,仑卡奈单抗已在全球53个国家和地区获批上市[3],展现出迄今最广泛的AD疾病修饰疗法全球覆盖。
LIFE研究(Longevity Improvement Fair Evidence Study)依托日本多市区医保理赔数据库,填补了仑卡奈单抗真实世界证据在亚洲人群中的空白,也为理解该药在日本特殊医疗体系下的早期应用模式提供了第一手数据[1]。值得注意的是,日本AD患病人口庞大,而日本又是AD疾病修饰疗法商业化进程中最早的亚洲市场,其经验对中国、韩国等邻近市场的临床决策与准入政策均具有重要参考价值。
患者画像:仑卡奈单抗进入了"最该治疗"的患者群体研究从18个市区町村的医保数据库中识别出123名在研究期间首次被处方仑卡奈单抗的患者。人口学与临床特征分析揭示出清晰的患者画像:
年龄与性别: 中位年龄为76岁,女性占多数,这与日本AD流行病学特征(女性患者比例更高)高度吻合,也与Clarity AD三期临床试验的受试者构成相符。
疾病阶段: 这是本研究中最具意义的发现之一。60.9%的患者MMSE评分≥24分(认知功能相对保留),79.3%的患者CDR整体评分为0.5(即轻度认知障碍,MCI阶段)[1]。这意味着日本临床医生在实际处方中,精准地将仑卡奈单抗用于疾病早期阶段的患者,此人群经临床试验验证收益最明显。
早期管理及安全性是关键此处有必要强调仑卡奈单抗的安全性优势。在三期Clarity AD试验中,仑卡奈单抗的ARIA-E(脑水肿型)发生率为12.6%,ARIA-H(微出血型)为17.3%[4],安全性事件显著低于同类竞品多纳单抗(ARIA-E 24.4%,ARIA-H 31.3%)[5]。更低的ARIA发生率意味着更少的早期中断风险,这在真实世界处方场景中尤为重要——当药物在医院、诊所层面被更广泛地处方给非试验环境的患者时,安全性的边际差异会被显著放大。
长期治疗获益:而非简单斑块清除
斑块的清除从来不是治疗目标本身,持续抑制神经毒性、最大化延缓疾病进展才是长期用药的核心意义。2025年AAIC大会公布的长期随访数据数据明确回答了"斑块清除后是否仍需继续治疗"这一关键问题:持续治疗至4年时,CDR-SB获益扩大至-1.75分,较18个月时增加近三倍,51%的患者认知功能改善或零进展[10]。相比多奈单抗斑块清除后若停药,病理进程将重新启动,这正是仑卡奈单抗作为慢性病长期管理药物而非"疗程型"药物的本质所在。
LIFE研究背书仑卡奈单抗的核心优势LIFE研究不仅是一份"处方规律"调查,其背后隐含着仑卡奈单抗多维度优势的现实映射:
机制优势——优先靶向毒性最强的Aβ种类。 仑卡奈单抗对可溶性Aβ原纤维(protofibrils)的亲和力比单体Aβ高约1000倍,在清除可溶性毒性寡聚体的同时兼顾不溶性斑块,形成双重清除效应。这与LIFE研究中高比例MCI患者被优先处方的临床决策逻辑完全契合——越早干预,毒性可溶性Aβ种类的危害越容易被阻断[6]。相比多奈单抗清除Aβ斑块单一机制从原理上更胜一筹。
疗效优势——三期临床黄金数据夯实循证基础。 Clarity AD三期试验(n=1795)中,仑卡奈单抗使CDR-SB量表的疾病进展速度在18个月时减缓27%(p<0.001),同时在CDR整体评分、ADAS-Cog14、ADCS MCI-ADL等所有次要终点均达到统计学显著[4]。相比多奈单抗减缓17.4%[5],仑卡奈单抗在认知收益上优势明显。CTAD 2025最新数据进一步显示,持续长期治疗有望将疾病进展延迟最多8.3年[7],这为LIFE研究中患者坚持治疗提供了强有力的动机支撑。
给药优势——皮下注射制剂进一步降低治疗门槛。 2025年8月,FDA批准了皮下注射维持剂量LEQEMBI® IQLIK™,于同年10月6日正式上市[8]。这是同类抗Aβ单抗中首个获批皮下注射剂型,使患者可以在家中自行给药,无需每两周前往医院接受静脉输注——这一突破对于提升日本等亚洲市场患者的治疗持续性具有直接实际意义,有望从根本上改善LIFE研究中观察到的早期中断问题。
全球准入优势——保险覆盖与市场准入持续推进。 仑卡奈单抗已在全球53个国家和地区获批[3],并于2025年12月被纳入中国国家医保局推出的"商业保险创新药品目录"[9],标志着其在亚洲最大市场的准入正在加速落地,也进一步强化了该药的全球商业化竞争壁垒。
参考文献
[1] Mori, Takaaki et al. "Initial real-world experience with lecanemab prescribing patterns in Japan: The Longevity Improvement Fair Evidence (LIFE) Study." Alzheimer's & Dementia: Diagnosis, Assessment & Disease Monitoring vol. 18 (2025): e70273. doi:10.1002/dad2.70273. https://alz-journals.onlinelibrary.wiley.com/doi/10.1002/dad2.70273
[2] Biogen Inc. "LEQEMBI® Intravenous Infusion (Lecanemab) Approved for the Treatment of Alzheimer's Disease in Japan." Press Release, September 25, 2023. https://investors.biogen.com/news-releases/news-release-details/leqembir-intravenous-infusion-lecanemab-approved-treatment
[3] Eisai Co., Ltd. "Biologics License Application for Subcutaneous Formulation of LEQEMBI® Submitted to Japan PMDA." 2026. https://www.eisai.com/news/2026/news202608.html
[4] van Dyck, Christopher H. et al. "Lecanemab in Early Alzheimer's Disease." New England Journal of Medicine vol. 388, 1 (2023): 9–21. doi:10.1056/NEJMoa2212948. https://www.nejm.org/doi/full/10.1056/NEJMoa2212948
[5] Sims, John R. et al. "Donanemab in Early Symptomatic Alzheimer Disease: The TRAILBLAZER-ALZ 2 Randomized Clinical Trial." JAMA vol. 330, 6 (2023): 512–527. doi:10.1001/jama.2023.13239. https://jamanetwork.com/journals/jama/fullarticle/2807533
[6] Bao, Wufan et al. "Lecanemab preferentially binds to smaller aggregates present at early stages of amyloid formation." Alzheimer's & Dementia (2025). https://pmc.ncbi.nlm.nih.gov/articles/PMC12001052/
[7] Eisai Co., Ltd. "New LEQEMBI® data presented at CTAD 2025 suggests potential to delay disease progression by up to 8.3 years with continued treatment." PRNewswire, December 2025. https://www.prnewswire.com/news-releases/new-leqembi-data-presented-at-ctad-2025-suggests-potential-to-delay-disease-progression-by-up-to-8-3-years-with-continued-treatment-302632737.html
[8] Eisai Co., Ltd. "FDA Approves LEQEMBI® IQLIK™ (lecanemab-irmb) Subcutaneous Injection for Maintenance Dosing." August 2025. https://www.eisai.com/news/2025/news202559.html
[9] BioArctic AB. "Leqembi® Iqlik™ (lecanemab-irmb) supplemental Biologics License Application regarding subcutaneous starting dose granted Priority Review by the US FDA." 2026. https://www.bioarctic.com/en/leqembi-iqlik-lecanemab-irmb-supplemental-biologics-license-application-regarding-subcutaneous-starting-dose-granted-priority-review-by-the-us-fda/
[10]PRNewswire. "Early Alzheimer's Patients Continue to Benefit from Four Years of LEQEMBI Therapy." July 2025. https://www.prnewswire.com/news-releases/early-alzheimers-patients-continue-to-benefit-from-four-years-of-leqembi-lecanemab-irmb-therapy-new-clinical-data-presented-at-aaic-302516704.html
本文内容来自公开信息及研究文献,不代表临床建议。
如需投稿、转载、商务合作后台留言,回复有一定延迟敬请谅解。
辅助编辑:腾讯元宝or(GPT、Gemini、Claude等)