编者按:代谢相关脂肪性肝病(MASLD)已成为全球最常见的慢性肝病,其发病率持续攀升且临床异质性显著,不同患者在病理机制、疾病表型、自然病程及治疗反应上存在巨大差异,这成为了制约精准诊疗的关键瓶颈。在第五届肝病创新大会上,陆军军医大学第一附属医院(西南医院)消化内科柴进教授在主题报告中,系统阐述了其团队基于肝脏蛋白质组学等多组学技术,首次发现MASLD的三个临床精准亚型,并揭示了各亚型的分子机制、临床特征及潜在诊断标志物,为MASLD的个体化治疗开辟了新路径。
 MASLD的异质性是临床诊疗的核心挑战
MASLD的异质性是临床诊疗的核心挑战代谢相关脂肪性肝病是以代谢异常相关的肝脂肪变性为特征的慢性肝病,其发病率随着生活方式的改变而迅速上升,儿童和青少年的患病率亦呈增长趋势。MASLD不仅可进展为肝硬化、肝细胞癌,还与慢性肾病、2型糖尿病、心血管疾病以及多种肝外肿瘤密切相关。尽管2024年瑞美替罗和2025年司美格鲁肽相继获批,但二者对MASLD相关肝硬化和MASH的疗效仍十分有限,其根本原因在于MASLD存在高度的临床异质性。这种异质性体现在不同患者的病理机制、疾病表型、自然病程以及对治疗的反应差异显著。既往研究尝试依据病理特征分为MASH与非MASH、依据基因型分为PNPLA3突变型与非突变型、依据临床特征分为瘦型与肥胖型脂肪肝等,但这些分型均未能有效解决MASLD的异质性问题,且临床应用存在诸多不便。
表1.现有多种依据基因型、病理和临床特征的临床分型

(引自讲者会议幻灯)
近年来,基于多组学和空间多组学技术在肿瘤领域成功实现了异质性区分和精准分型,如食管鳞状细胞癌、肾透明细胞癌、肝细胞癌和黑色素瘤等,部分甚至实现了临床治愈。然而,国内外尚未有研究采用多组学技术对MASLD进行系统的临床精准分型。
表2. 基于多组学、空间多组学技术能有效区分肿瘤异质性,并实现临床精准分型、精准靶向治疗
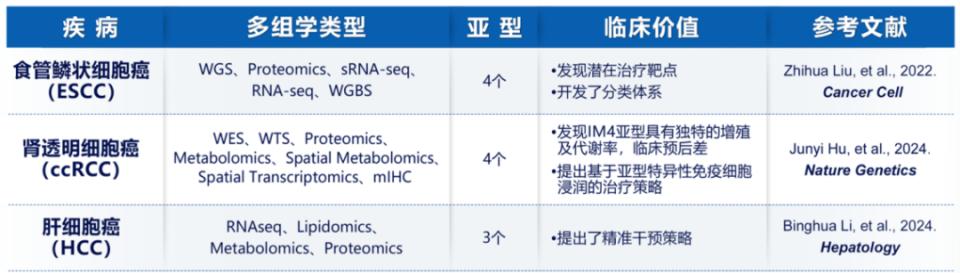
(引自讲者会议幻灯)
实验设计与分析流程为解决MASLD异质性这一领域瓶颈,研究团队联合国内多家中心,收集了肝穿刺样本、血液和尿液标本,开展了肝脏蛋白质组学、磷酸化组学、代谢组学及基因组学等多组学检测,旨在通过多维度数据整合发现新的临床亚型。团队利用机器学习等方法对数据进行聚类分析与特征筛选,并在内部队列中发现分型后,进一步在独立外部队列中进行验证,以确证分型的稳定性和普适性。
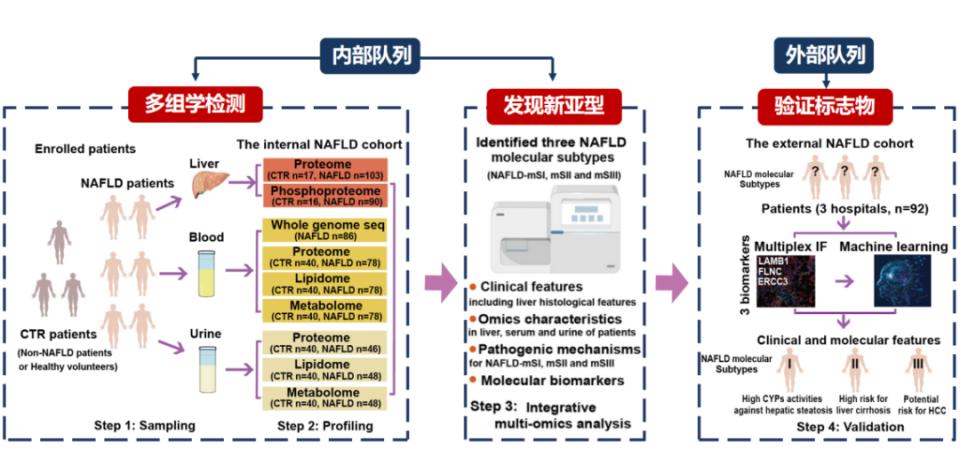
图1. 实验设计及分析流程
(引自讲者会议幻灯)
各亚型的临床特征与分子特征代谢活跃型患者的肝脏脂肪变性相对较轻,空腹胰岛素、C肽及HOMA-IR水平较低,其差异表达前五的分子主要参与代谢调节。肝硬化高风险型患者的肝脏炎症和纤维化最为严重,ALT、AST及BMI水平较高,其差异表达前五的分子主要参与炎症和纤维化调节。原发性肝癌高风险型患者的差异表达前五的分子则主要与肿瘤发生密切相关,多为转录因子。多组学联合分析显示,各亚型独特的分子之间具有显著相关性,提示不同亚型具有独立的分子网络调控特征。
MASLD的临床精准分型发现基于肝脏蛋白质组学分析,研究团队首先验证了样本的可靠性。结果显示,MASLD组与对照组相比,差异基因富集在铁死亡等信号通路,这与以往文献报道高度一致,证实了所用样本的质量符合要求。在此基础上,通过机器学习方法对蛋白质组学数据进行深度挖掘,团队首次发现MASLD可自然聚类为三个截然不同的临床亚型。根据其后续的临床特征和分子机制,这三个亚型被分别命名为代谢活跃型(mSI)、肝硬化高风险型(mSII)和原发性肝癌高风险型(mSIII)。进一步分析显示,这三个亚型与已知的MASLD易感基因多态性(如PNPLA3等)无显著相关性,且用于鉴定三个亚型的蛋白与易感基因亦无显著关联,提示基于蛋白质组学的分型独立于基因背景,更直接反映疾病的功能状态。
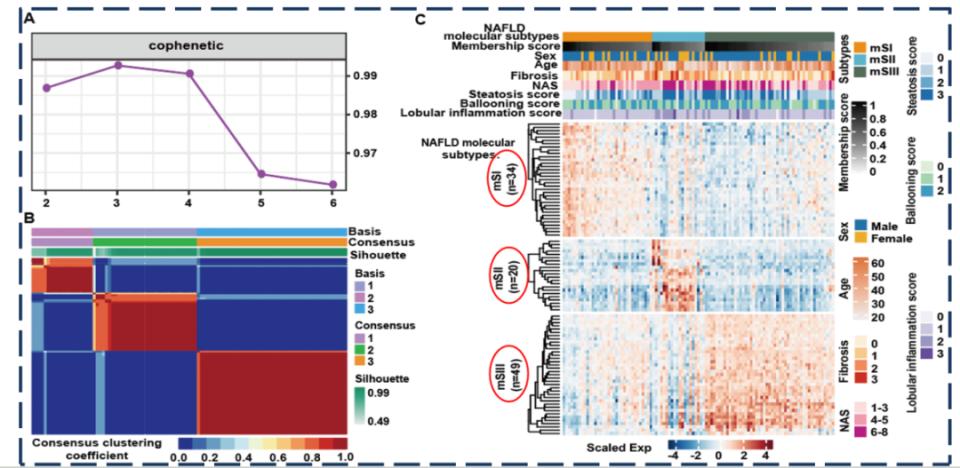
图2. 发现MASLD的三个临床精准亚型
(引自讲者会议幻灯)
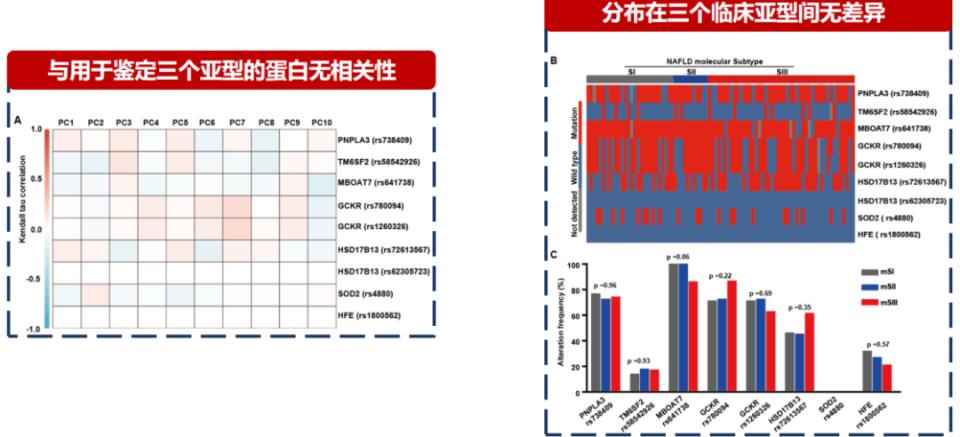
图3. MASLD的三个临床亚型与其易感基因多态性的关系
(引自讲者会议幻灯)
各亚型的临床特征与分子特征代谢活跃型患者的肝脏脂肪变性相对较轻,空腹胰岛素、C肽及HOMA-IR水平较低,其差异表达前五的分子主要参与代谢调节。肝硬化高风险型患者的肝脏炎症和纤维化最为严重,ALT、AST及BMI水平较高,其差异表达前五的分子主要参与炎症和纤维化调节。原发性肝癌高风险型患者的差异表达前五的分子则主要与肿瘤发生密切相关,多为转录因子。多组学联合分析显示,各亚型独特的分子之间具有显著相关性,提示不同亚型具有独立的分子网络调控特征。
各临床亚型的分子机制原发性肝癌高风险型的分子机制研究表明,该亚型与另外两个亚型相比,癌症相关信号通路被显著激活,关键蛋白GTF2F1、GTF2F2、TAF15、H3-3A、CEBPB和ERCC3呈高表达。其中,CEBPB和ERCC3与肝癌相关基因表达呈正相关,过表达这两个基因可促进Huh7细胞中癌基因的表达及细胞迁移和侵袭,小鼠原代肝细胞实验也得到一致结果。进一步研究发现,p-EGFR(Ser1037位点)通过激活PI3K-PDK1-AKT信号通路上调ERCC3和CEBPB表达。在肝癌患者样本中,EGF/p-EGFR/PI3K-PDK1-AKT信号通路活化,ERCC3、CEBPB及下游癌基因表达增高。这一机制提示部分MASLD患者可不经肝硬化阶段,在脂肪肝背景下直接向肝细胞癌(HCC)转化。
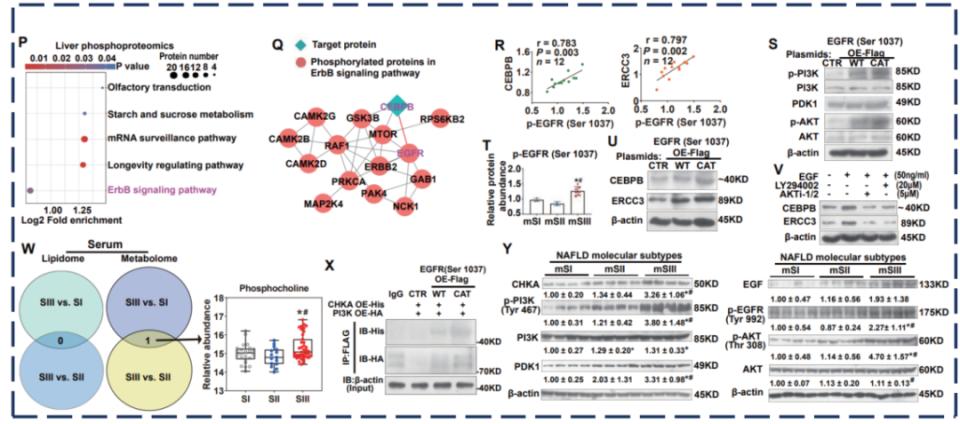
图4. 原发性肝癌高风险型中,p-EGFR(Ser 1037)通过激活PI3K-PDK1-AKT促进ERCC3/CEBPB表达
(引自讲者会议幻灯)
总之,初步机制探索显示,在MASLD-mSIII发病过程中,高水平的EGF通过p-EGFR,一方面激活PI3K-PDK1-AKT信号通路,进而促进CEBPB和ERCC3调控的癌基因表达;另一方面提高血清磷酸胆碱水平,最终增加HCC风险。
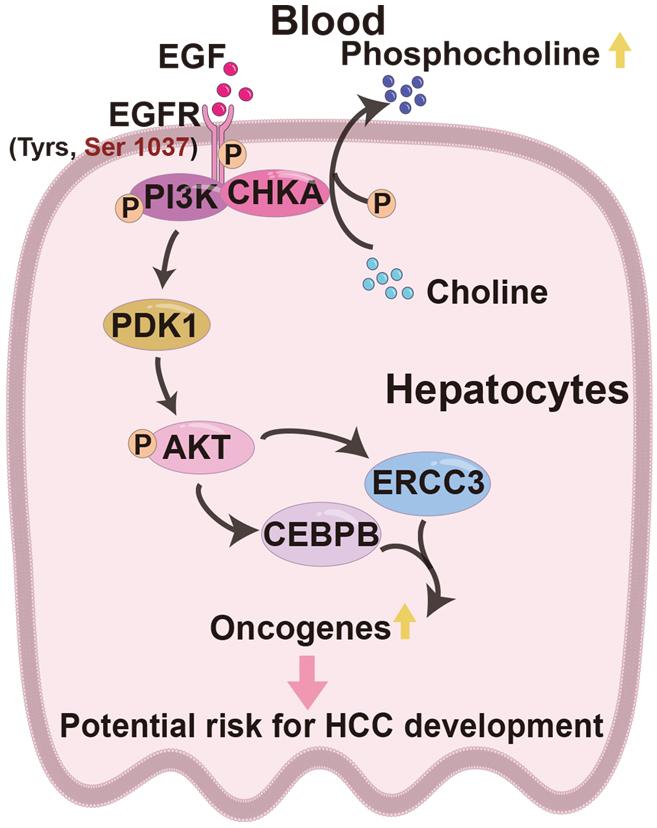
图5. 原发性肝癌高风险型(MASLD-mSIII)分子机制
(引自讲者会议幻灯)
肝硬化高风险型的分子机制显示,该亚型纤维化相关信号通路被激活,LAMA2、LAMA4、LAMB1、LAMC1、FLNA、FLNC、MYL2和MYLPF等细胞外基质蛋白是关键分子,且与纤维化程度及NAS评分呈正相关。TGFβ-SMAD2/3信号通路在该亚型中被激活,肝纤维化标志物α-SMA和COLs高表达。同时,肝脏炎症因子表达增加,白细胞跨内皮迁移被激活。免疫细胞浸润分析显示,M1型和M2型巨噬细胞浸润均显著高于其他亚型。机制上,CRP促使由CCL2招募的单核细胞分化为M1型巨噬细胞促进炎症,而脂肪酸可促进CCL2、CRP和PKM2的表达,并调节M1向M2型巨噬细胞的转化。
总之,初步机制探索表明,在MASLD-mSII发病过程中,肝脏内过高的血脂刺激CCL2和CRP分泌,引起单核细胞募集和M1型巨噬细胞极化,从而导致肝脏炎症。此外,脂质诱导PKM2高表达,促进M1向M2型巨噬细胞转化,并通过增加TGFβ1生成和HSC活化加重肝纤维化。
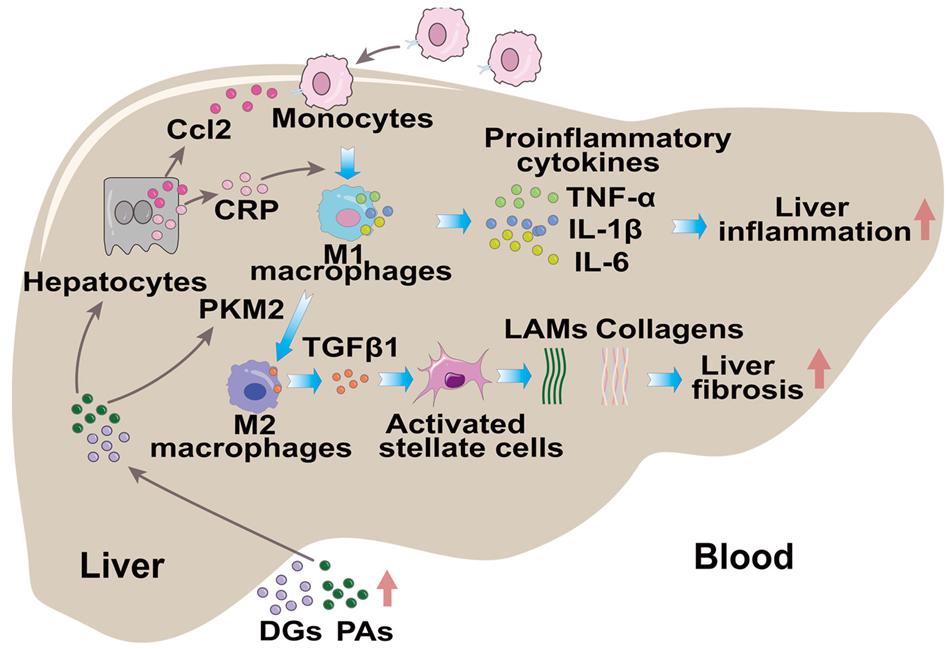
图6. 肝硬化高风险亚型(MASLD-mSII)分子机制
(引自讲者会议幻灯)
代谢活跃型的分子机制显示,该亚型代谢相关信号通路被激活,CYP1A2、CYP3A4、GSTA2、GSTT2B等代谢酶高表达。CYP1A2和CYP3A4与肝脏脂肪变性及NAS评分呈负相关,与血清胆汁酸和脂质水平亦呈负相关。抑制CYP1A2或CYP3A4可促进肝细胞内脂质积累。结合胆汁酸和游离脂肪酸分别通过NTCP和CD36被肝脏摄取,激活FXR和PPARα,进而抑制CYP1A2和CYP3A4表达,加重脂质积累。而在代谢活跃型中,mTOR信号通路被激活,抑制了FXR和PPARα,从而维持CYP1A2和CYP3A4的高表达,抵抗脂质沉积。
总之,初步机制探索表明,在代谢活跃亚型(MASLD-mSI)中,转运蛋白NTCP和CD36调节引起的肝内低浓度BAs和FFAs,激活mTOR信号,抑制FXR和PPARα活性来维持肝内高浓度的CYP1A2和CYP3A4,缓解肝内脂质积累。
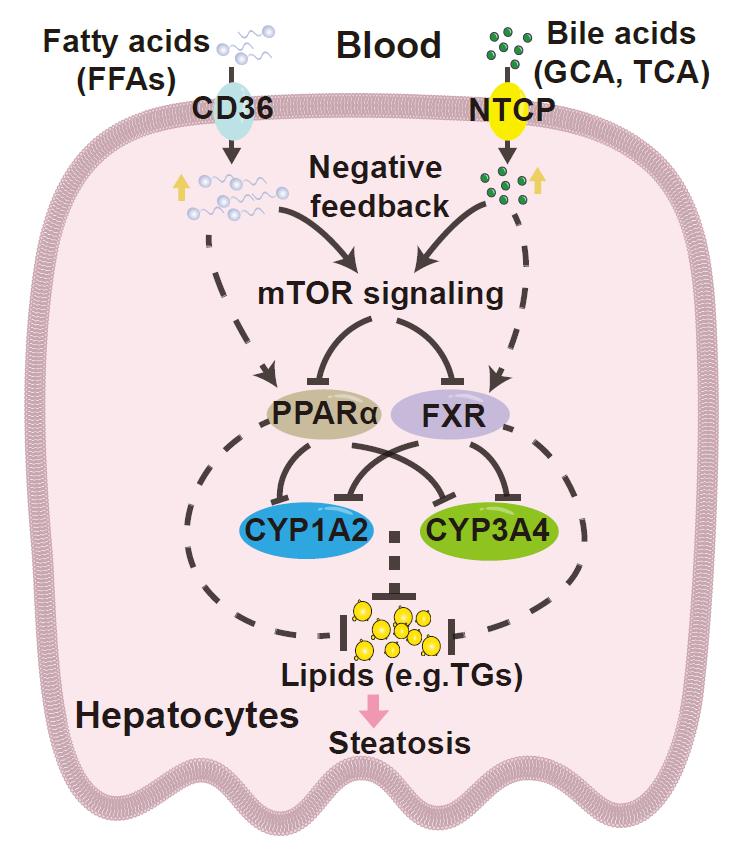
图7.代谢活跃亚型(MASLD-mSI)分子机制
(引自讲者会议幻灯)
MASLD三个临床精准亚型的诊断标志物探索通过机器学习筛选,研究团队发现LAMB1、FLNC和ERCC3三个肝脏蛋白联合可作为三个亚型的潜在诊断标志物。在内部MASLD队列中,采用多重免疫荧光技术检测肝穿刺切片中这三个蛋白的表达,诊断准确率高达93%。在包含三家医院90余例样本的外部验证队列中,该诊断模型同样能够准确区分三个亚型,且各亚型的病理特征、血清学生化指标及关键标志物表达均与内部队列一致。目前,团队正在开展血清学无创诊断标志物的筛选研究,以期实现无需肝穿刺的临床精准分型。
小结与展望本研究基于肝脏蛋白质组学首次发现MASLD的三个临床精准亚型,明确了各亚型的临床特征与分子特征,初步揭示了其独特的分子机制,并发现了可用于诊断的生物标志物。这一成果为MASLD的异质性难题提供了新的解决方案,为后续的个体化治疗和精准药物研发奠定了重要基础。