
精准医学的快速演进,正将两个曾经被视为"不可成药"靶点——KRAS G12C和TP53——推向临床实践的核心位置。2025年,KRAS G12C抑制剂的联合治疗策略取得多项关键进展;2026年2月,NEJM(The New England Journal of Medicine)正式发表了Rezatapopt(PC14586)的1期临床数据,首次在人体内验证了p53再激活的概念[1]。这两个靶点的突破性进展,正在改写肿瘤治疗的格局。
近日,国家药品监督管理局(NMPA)批准硫酸索西美雷塞片(商品名:济乐美)上市,该药适用于至少接受过一种系统性治疗的KRAS G12C突变型晚期NSCLC成人患者。在此之前,2025年KRAS G12C抑制剂进入"联合制胜"的新阶段:氟泽雷塞联合西妥昔单抗在一线展现出高缓解率与长PFS[2,3];戈来雷塞联合SHP2抑制剂在《The Lancet Respiratory Medicine》报道ORR达71%、mPFS 12.2个月,提示"KRAS+上游通路"双口服策略的竞争力[4,5]。这些进展表明,无论是"单药破局"还是"联合组合",KRAS G12C的适应症边界与获益人群持续扩宽。
2026年2月26日,TP53 Y220C再激活剂Rezatapopt(PC14586)的I期结果登上NEJM[1],为TP53这一传统"不可成药"靶点提供了概念验证。在既往多线治疗的实体瘤患者中,Rezatapopt在多种瘤种观察到客观缓解;当限定KRAS野生型且剂量≥1150mg QD时,ORR可达30%。机制上Rezatapopt通过非共价结合Y220C突变形成的"口袋",稳定野生型构象并恢复转录活性。安全性方面,最常见为恶心、呕吐与血肌酐升高,多属1–2级,可管理。
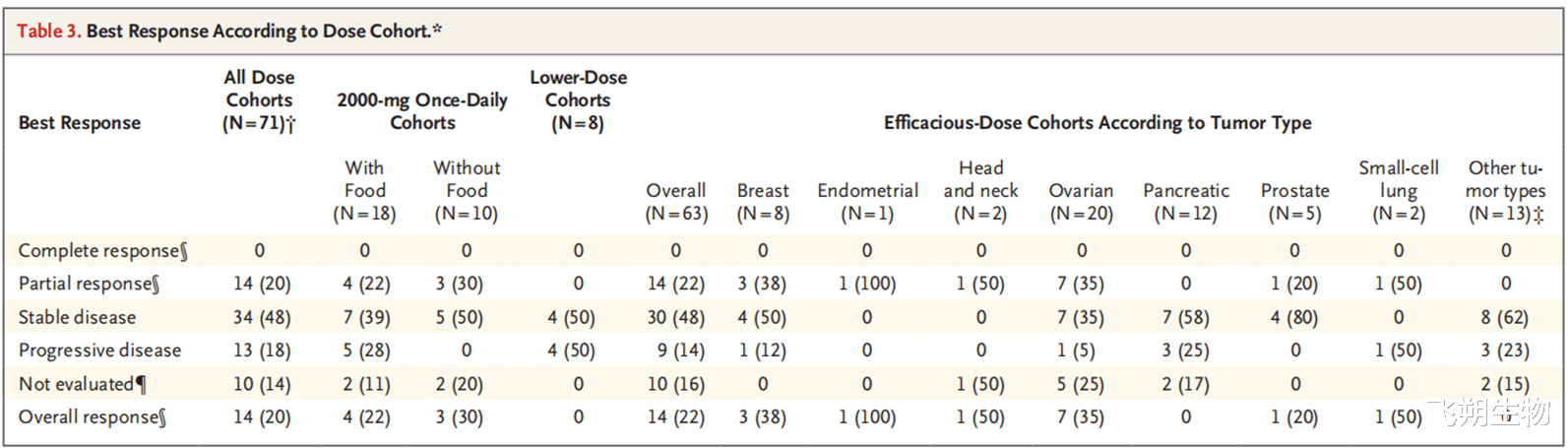
▲根据剂量队列的最佳反应
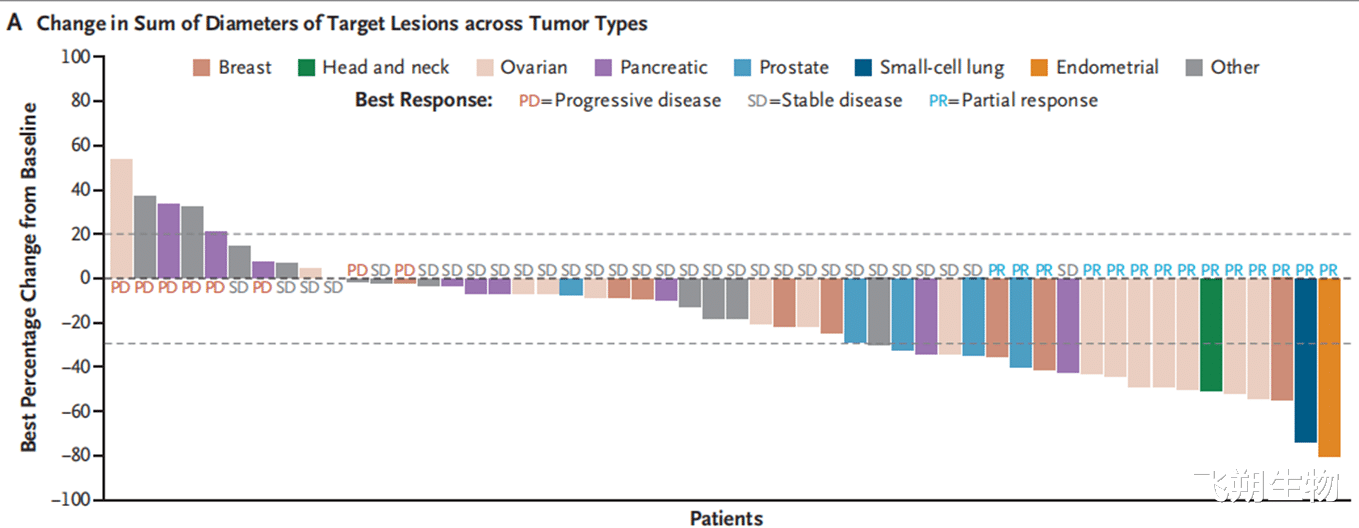
▲肿瘤类型靶病变直径总和的变化
注:从患者肿瘤病灶变化的图表中可以看到,大部分患者的靶病灶尺寸相比治疗前有所缩小(条形图大部分位于0%以下),但反应类型各异,包括疾病稳定、部分缓解以及疾病进展。
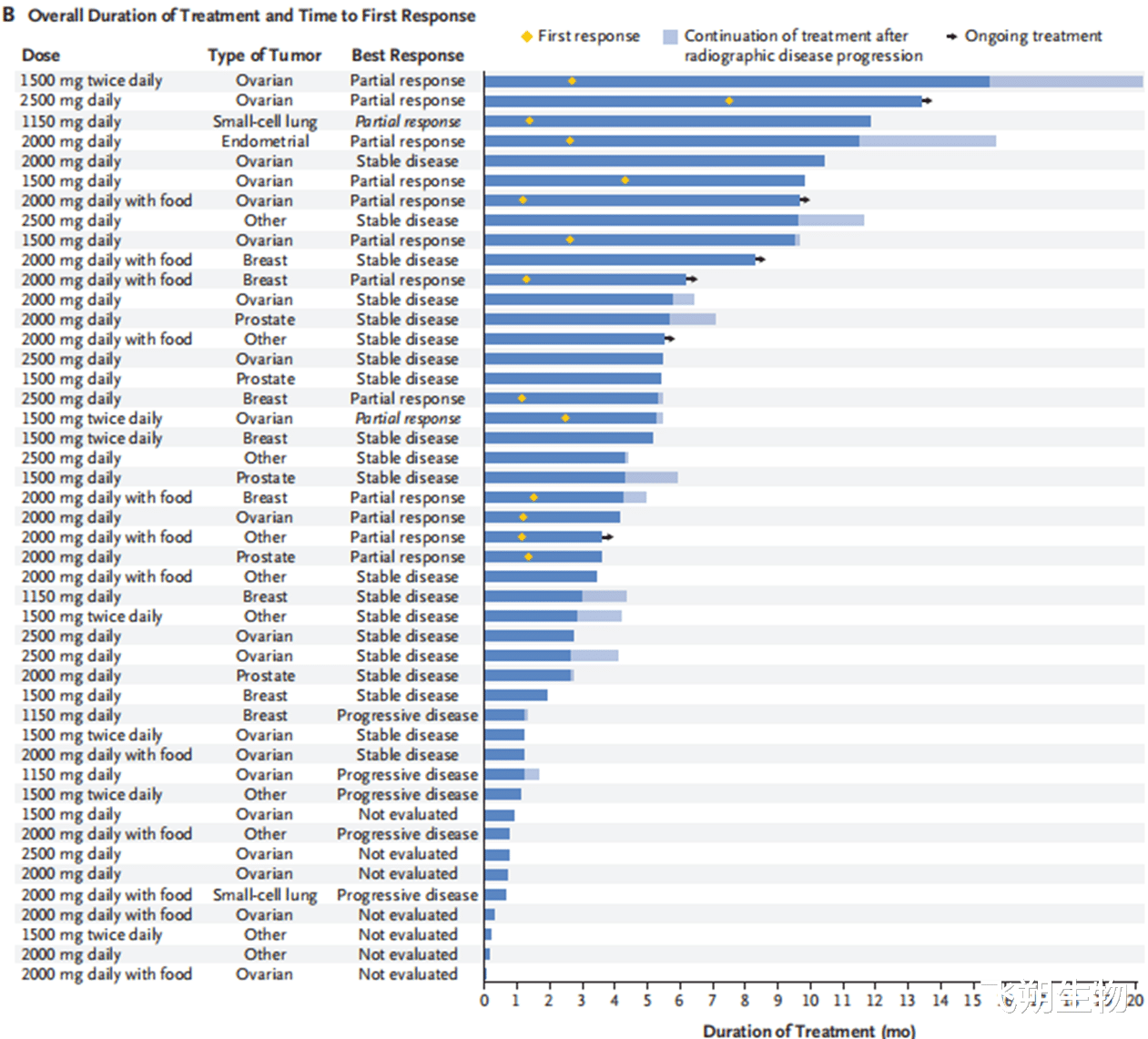
▲治疗的总持续时间和第一次反应的时间
注:关于治疗持续时间的图表显示,部分患者在治疗开始后1-3个月内就出现了首次疗效反应,并且能够持续治疗较长时间。
基于I期数据,PYNNACLE II期研究(NCT04585750)正在进行,以2000mg QD随餐作为RP2D,入组含卵巢、乳腺、子宫内膜等瘤种的TP53
Y220C突变且KRAS野生型患者。数据显示,Rezatapopt后线治疗卵巢癌的客观缓解率(ORR)达45.8%,肺癌的ORR为21.1%,乳腺癌的ORR为16.7%,子宫内膜癌的ORR为60%。总体患者的中位缓解持续时间为7.6个月。目前的数据提示Rezatapopt单药在妇科肿瘤中似乎疗效更好,而在肺癌、乳腺癌这些有比较明确驱动基因的肿瘤中,Rezatapopt可能更适合“打辅助”[6-8]。此外,响应快速且持续,ctDNA VAF早期下降与疗效相关。值得注意的是,TP53突变在卵巢癌与乳腺癌中高频出现,TNBC可达约60%,Y220C突变占约1%,为TNBC这类难治亚型提供了潜在"再激活"路径。
未来展望
KRAS已进入"组合时代",RAS(ON)与KRAS
G12C(OFF)的协同、以及SHP2/EGFR/免疫等不同层级的联合策略正加速推进,个体化选择可权衡疗效、安全性与经济性,临床选择需兼顾线数、基线特征与风险耐受度[9]。从中国KRAS G12C实践看,国产四药各具特色:氟泽雷塞在联合与二线PFS方面领先;戈来雷塞安全性更优(TRAE仅38.7%,停药率5.0%);格索雷塞价格更友好但肝毒性需谨慎;索西美雷塞的中位总生存期和治疗相关不良事件需持续关注。
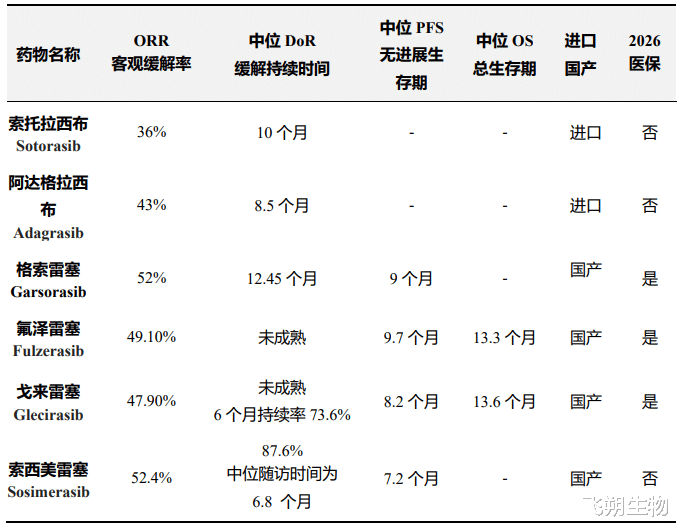
▲KRAS G12C抑制剂疗效对比表
注:除了上述已获批的产品以外,还有 42 款国产 KRAS G12C 抑制剂在研,进入临床阶段的有 15 款。其中华健未来 HJ891 进展最快,已启动 III 期临床。
TP53基因正迎来其"再激活时代"的重要发展节点,Rezatapopt等新型药物的临床推进,不仅验证了针对热点突变开发靶向药物的可行性,更提示了这种成药路径在肿瘤治疗中具有显著的可复制性和推广价值。随着研究的深入,针对TP53 Y220C等特定突变的再激活策略正在不断成熟,这一策略将在多个关键环节实现精细化升级,共同推动着精准医疗向更深层次发展,为携带TP53突变的癌症患者提供更加个体化的治疗选择[10,11]。
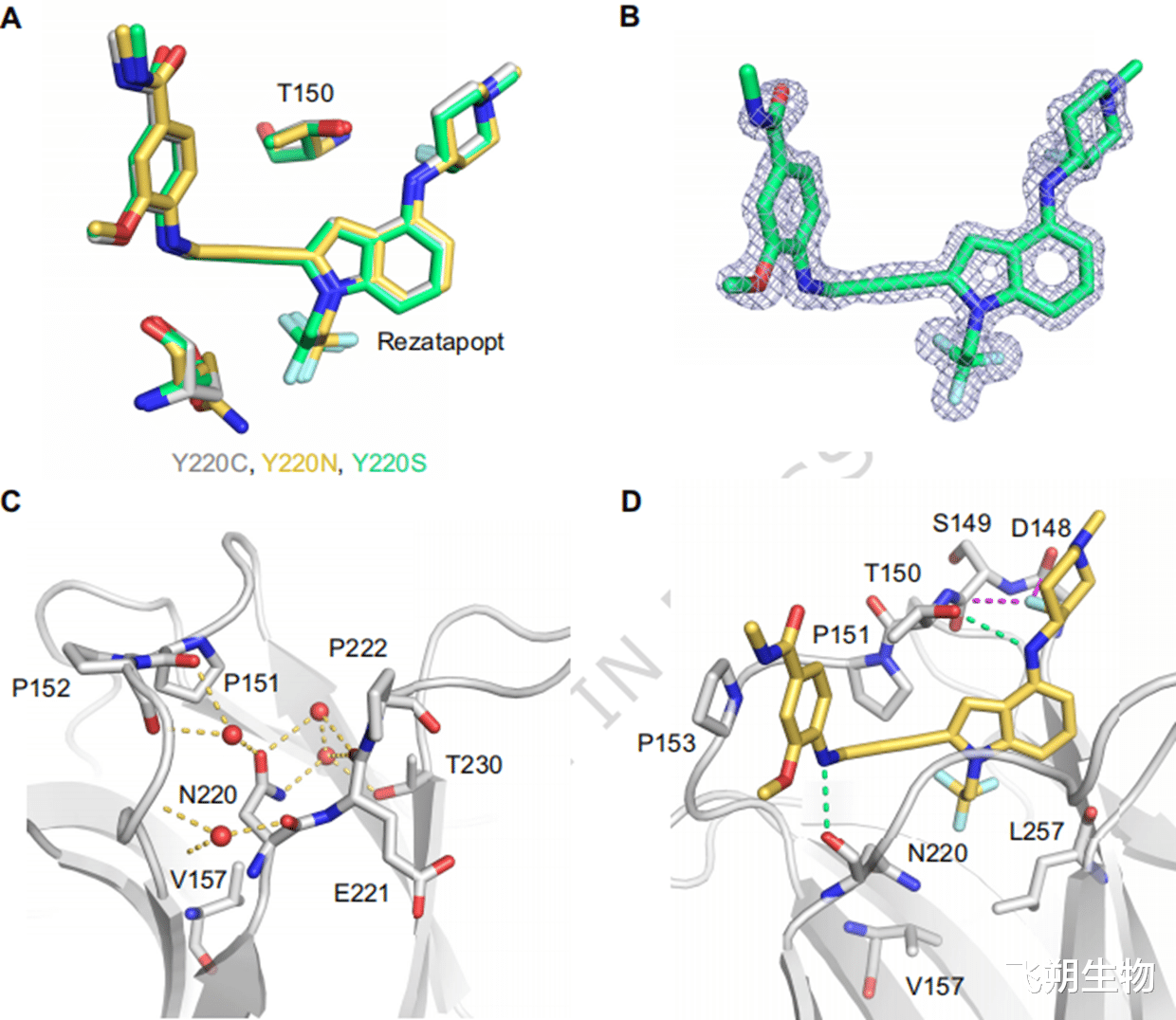
▲Y220S和 Y220N突变体与结合 rezatapopt 的复合物结构[11]
2025年的KRAS靶点临床实践积累了丰富经验,2026年TP53领域的研究取得了关键性突破,这两大里程碑事件共同揭示了一个重要趋势:精准医学正在经历从单一靶点向多靶点组合策略、从独立用药向协同治疗方案、从广谱普适向亚型分层诊疗的持续深化。这一演进路径清晰表明,未来精准医学的发展将更加注重以生物标志物为指导,推动个体化、多机制联合的精准治疗组合模式。
参考文献
[1] N Engl J Med. 2026 Feb 26;394(9):872-883.
[2] 2025 ELCC LBA1.
[3] KANDLELIT-001: MK-1084 in KRAS G12C CRC/NSCLC. 2025 ASCO.
[4] Nat Med. 2025 Mar;31(3):894-900.
[5] Lancet Respir Med. 2026 Feb;14(2):163-173.
[6] ACS Med Chem Lett. 2024 Nov 4;16(1):34-39..
[7] ESMO Asia Congress 2025 - LBA2
[8] ESMO Breast/ESMO Asia 2025.
[9] RAS(ON) strategies at AACR 2025: daraxonrasib, zoldonrasib.
[10] Blood. 2025 Nov 20;146(21):2574-2588.
[11] Cell Death Dis. 2026 Feb 26.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!