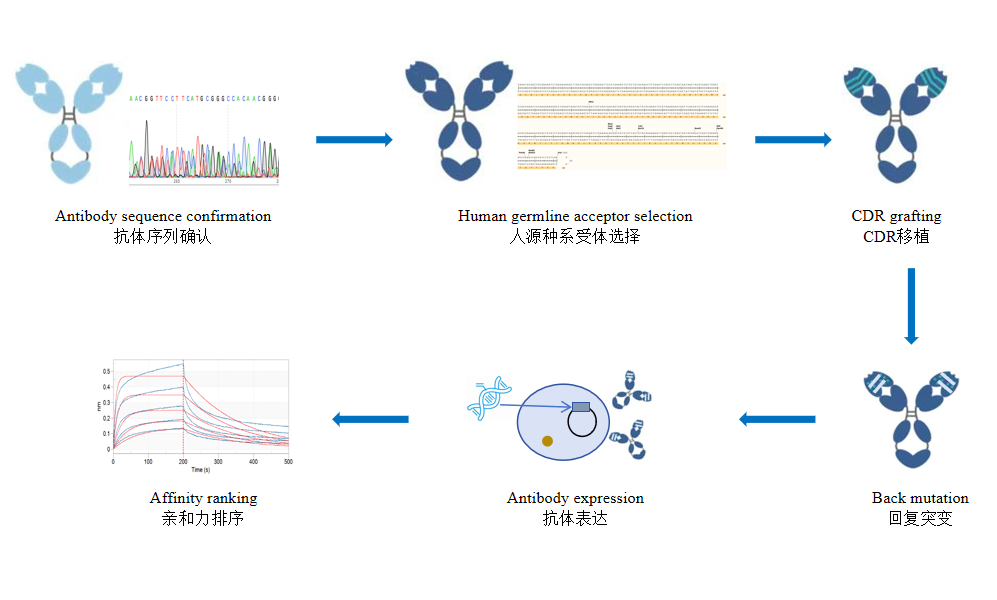
抗体人源化是治疗性抗体临床前开发的关键环节,其核心目标是在保留抗体特异性与亲和力的基础上,降低异种蛋白的免疫原性,为临床应用奠定基础。自 1975 年杂交瘤技术问世以来,单克隆抗体(单抗)凭借高特异性的靶向优势,在生物学研究与疾病治疗中展现出巨大潜力。然而,杂交瘤技术制备的鼠源性单抗作为异种蛋白,在人体应用中面临多重瓶颈,推动了抗体人源化改造技术的持续革新。
一、鼠源性抗体的临床应用局限与改造必要性杂交瘤技术制备的鼠源性单抗虽具备明确的抗原靶向性,但在人体中存在显著应用缺陷:其一,鼠抗体作为异种蛋白具有强免疫原性,重复给药后易引发人抗鼠抗体(HAMA)反应,不仅会中和抗体活性、削弱治疗效果,还可能导致过敏反应、炎症损伤等不良反应,甚至损害抗体清除相关器官;其二,鼠源性抗体的恒定区与人类补体、Fc 受体的相互作用较弱,难以有效激活抗体依赖的细胞毒性(ADCC)、补体依赖的细胞毒性(CDC)等效应功能,限制了其抗肿瘤、抗感染等治疗效能。
为突破上述局限,抗体人源化改造应运而生。其核心设计理念基于抗体结构与功能的关联性 —— 抗体的抗原结合特异性由可变区的互补决定区(CDR)决定,而免疫原性主要源于恒定区及可变区的骨架区(FR)。因此,改造需遵循两大基本原则:① 完整保留原抗体 CDR 区的序列与空间构象,确保抗原结合特异性与亲和力不受影响;② 最大限度替换鼠源性序列为人类抗体同源序列,降低或消除免疫原性。
二、抗体人源化改造的技术演进与核心策略抗体人源化改造历经半个多世纪的发展,形成了从嵌合抗体、改型抗体(CDR 移植抗体)到全人源化抗体的技术阶梯,每一代技术均针对前序方案的缺陷进行优化升级。
(一)嵌合抗体:免疫原性初步降低
嵌合抗体是第一代人源化改造产物,其设计核心是利用人类抗体恒定区替换鼠源性抗体的恒定区,保留鼠抗体的可变区(含 CDR 区与 FR 区)。这一策略的理论依据是:HAMA 反应的主要靶点为鼠抗体的恒定区,替换后可显著削弱免疫原性,同时人类恒定区能更高效地激活人体补体与 Fc 受体相关效应系统。
1. 嵌合 IgG 抗体
目前临床应用中最常见的嵌合抗体形式为鼠 - 人嵌合 IgG。其构建流程可概括为:① 从分泌目标抗体的杂交瘤细胞中克隆并鉴定鼠抗体轻链(VL)与重链(VH)可变区基因;② 分别与人抗体相应亚型(如 IgG1、IgG4)的恒定区基因(CL、CH1-CH3)进行重组;③ 将重组的嵌合轻链、重链基因克隆至真核表达载体;④ 转染宿主细胞(如 CHO 细胞、HEK293 细胞)进行表达,经纯化与活性筛选获得功能性嵌合抗体。该过程中,可变区基因的准确克隆与正确拼接是保障抗体活性的关键,任何序列突变或框架区损伤都可能导致抗原结合能力下降。
2. 嵌合 Fab 与 F (ab’)₂抗体
为解决完整 IgG 抗体分子量较大(约 150Kda)、组织渗透性差的问题,研究人员通过重组 DNA 技术开发了嵌合 Fab 与 F (ab’)₂片段抗体。嵌合 Fab 的构建原理是:将鼠抗体 VL、VH 基因分别与人抗体 κ 链恒定区(CL)、重链 CH1 区基因重组,表达后形成仅含抗原结合片段的单价抗体(分子量约 50Kda)。由于缺乏 Fc 段,Fab 抗体不仅降低了免疫原性,还避免了 ADCC、CDC 效应相关的非特异性损伤,适合作为靶向诊断探针或药物载体。
但 Fab 抗体存在固有缺陷:单价结合导致表观亲和力较低,且小分子易被肾小球滤过,血液半衰期短(通常仅数小时),单独应用于治疗时疗效有限。为优化药代动力学特性,可通过 PEG 化修饰增大分子量,延长体内滞留时间;或通过化学耦联、重组末端修饰等方法将两个 Fab 片段连接形成二价 F (ab’)₂抗体(分子量约 100Kda),其抗原结合亲和力与体内稳定性显著提升,同时保留了组织渗透性优势,在肿瘤靶向治疗、免疫毒素偶联等领域具有独特应用价值。
(二)改型抗体(CDR 移植抗体):免疫原性深度降低
嵌合抗体的可变区仍保留约 30% 的鼠源性序列(主要为 FR 区),部分患者仍可能产生 HAMA 反应,尤其在长期治疗中。为进一步降低免疫原性,改型抗体(又称 CDR 移植抗体)技术应运而生,其核心创新是仅保留鼠抗体中直接参与抗原结合的 CDR 区,将其移植至人类抗体的 FR 区框架中,构建 “人类骨架 - 鼠源 CDR” 的嵌合可变区,再与人抗体恒定区重组形成全人源化程度更高的抗体。
CDR 移植的关键在于选择合适的人类抗体骨架区。理想的骨架区需满足两个条件:① 与鼠抗体可变区框架区序列同源性较高,以维持 CDR 区的正确空间构象;② 无自身免疫原性风险。常用策略是从人类抗体数据库中筛选与鼠抗体可变区同源性最高的天然抗体序列作为骨架,或采用通用骨架区(如 EU 框架)进行改造。然而,单纯 CDR 移植常导致抗体亲和力下降,这是因为鼠抗体 FR 区的部分氨基酸残基可能通过氢键、疏水作用等稳定 CDR 区构象,或直接参与抗原结合(即 “框架区贡献”)。因此,需通过 “亲和力成熟” 技术对框架区关键位点进行定点突变,恢复或提升抗体的抗原结合活性。
(三)全人源化抗体:免疫原性最小化
尽管 CDR 移植抗体的鼠源性序列占比已降至 5%-10%,但仍可能存在潜在免疫原性。随着基因工程技术的发展,全人源化抗体技术逐渐成熟,彻底摆脱了鼠源性序列的依赖,主要包括噬菌体展示技术、转基因小鼠技术两大核心路径。
噬菌体展示技术通过构建大容量人类抗体基因文库(含 VL、VH 基因组合),利用噬菌体表面展示系统筛选与目标抗原特异性结合的抗体序列,经重组表达获得全人源抗体;转基因小鼠技术则通过基因编辑将人类抗体基因簇导入小鼠基因组,使其在免疫后产生全人源抗体,再通过杂交瘤技术或单细胞测序筛选目标抗体。全人源化抗体的免疫原性降至最低,HAMA 反应发生率显著低于嵌合抗体与 CDR 移植抗体,且能更高效地激活人体免疫效应系统,是目前治疗性抗体开发的主流方向。
三、人源化改造的关键技术要点与应用展望(一)核心技术考量
抗体人源化改造需在 “免疫原性降低” 与 “抗原结合活性保留” 之间实现精准平衡。除了选择合适的改造策略,还需关注以下关键点:① 抗体亚型选择:不同人抗体亚型(如 IgG1 具有强 ADCC/CDC 活性,IgG4 无补体激活能力)需根据治疗需求匹配;② 糖基化修饰:宿主细胞的糖基化模式会影响抗体稳定性与效应功能,需通过细胞工程优化;③ 稳定性优化:部分 CDR 移植抗体可能存在热稳定性下降问题,需通过定点突变或二硫键工程增强结构稳定性。
(二)临床应用价值与发展趋势
经过人源化改造的治疗性抗体已在肿瘤、自身免疫病、感染性疾病等领域取得显著突破。例如,抗 HER2 嵌合抗体曲妥珠单抗、CDR 移植抗体帕妥珠单抗已成为乳腺癌治疗的核心药物;全人源 PD-1 抗体帕博利珠单抗、纳武利尤单抗引领了肿瘤免疫治疗的革命。未来,抗体人源化技术将向更精准、高效的方向发展,结合人工智能辅助设计、结构生物学指导的亲和力成熟、双特异性 / 多特异性抗体构建等技术,进一步提升抗体的治疗效能,降低不良反应,为更多疾病提供个性化治疗方案。
总结抗体人源化改造是治疗性抗体从实验室走向临床的关键桥梁,其技术演进体现了 “降低免疫原性” 与 “保留生物活性” 的核心诉求。从嵌合抗体的初步探索,到 CDR 移植抗体的精准优化,再到全人源化抗体的成熟应用,每一代技术的革新都推动了治疗性抗体的临床转化效率。随着基因工程与结构生物学技术的持续进步,抗体人源化改造将更加高效、精准,为开发更安全、有效的生物药物提供坚实基础。