嵌合抗原受体(CAR-T)细胞能够在自身免疫性疾病患者体内重塑免疫系统,属于一种强效的治疗手段。开展临床研究时,需要采用创新的试验设计,才能切实可行地评估CAR-T细胞的安全性与有效性。
2026年1月,来自欧洲多个国家的研究者在《Nature Medicine》上发表了题为《CD19 CAR-T cells for treatment-refractory autoimmune diseases: the phase 1/2 CASTLE basket trial》的文章,报告了一项1/2a期、两阶段优化设计的篮子试验(CASTLE研究)。
CASTLE研究旨在探究自体CD19 CAR-T细胞产品zorpocabtagene autoleucel(Zorpo-cel,亦称MB-CART19.1),在治疗难治性系统性红斑狼疮(SLE)、系统性硬化症(SSc)及特发性炎症性肌病(IIM)患者中的安全性与有效性。
研究设计
CASTLE表示“CAR-T细胞治疗系统性B细胞介导自身免疫病”,其临床试验注册编号为NCT06347718,欧洲临床试验数据库(EudraCT)编号为2022-001366-35。
研究共入组了24例患者(10例SLE、9例SSc、5例IIM),所有患者均在停用免疫抑制治疗,并接受环磷酰胺联合氟达拉滨标准淋巴清除预处理后,按每公斤体重1×10⁶个CAR-T细胞单次输注Zorpo-cel。
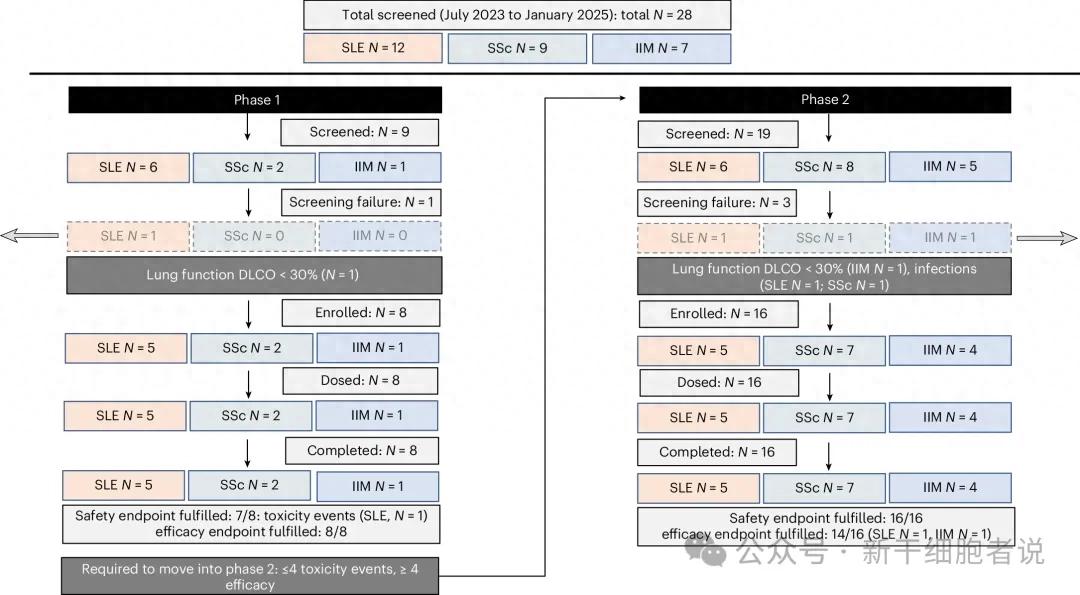
流程图展示了CASTLE研究中筛选并入组的患者总数及各疾病对应的患者数量(所有患者均接受了Zorpo-cel治疗)
主要安全性终点为细胞因子释放综合征(CRS)与免疫效应细胞相关神经毒性综合征(ICANS)的发生率。
次要临床疗效终点为治疗24周后,依据系统性红斑狼疮缓解定义(DORIS)标准评估的SLE缓解情况、SSc患者间质性肺病无进展情况,以及IIM患者达到美国风湿病学会(ACR)显著/中度应答的情况。
结果分析
CASTLE研究的主要及次要终点均已达成。
安全性方面,未出现2级以上细胞因子释放综合征,亦无免疫效应细胞相关神经毒性综合征发生。

SLE患者的DORIS缓解情况(患者例数N=10;绿色方框代表达到DORIS缓解)
疗效方面,24例患者中有22例达到预设疗效终点:10例SLE患者中有9例实现DORIS缓解,9例SSc患者均未出现疾病进展,5例IIM患者中有4例达到ACR显著/中度应答。此外,在24周的整个观察期内,所有患者均停用糖皮质激素及其他各类免疫抑制治疗。
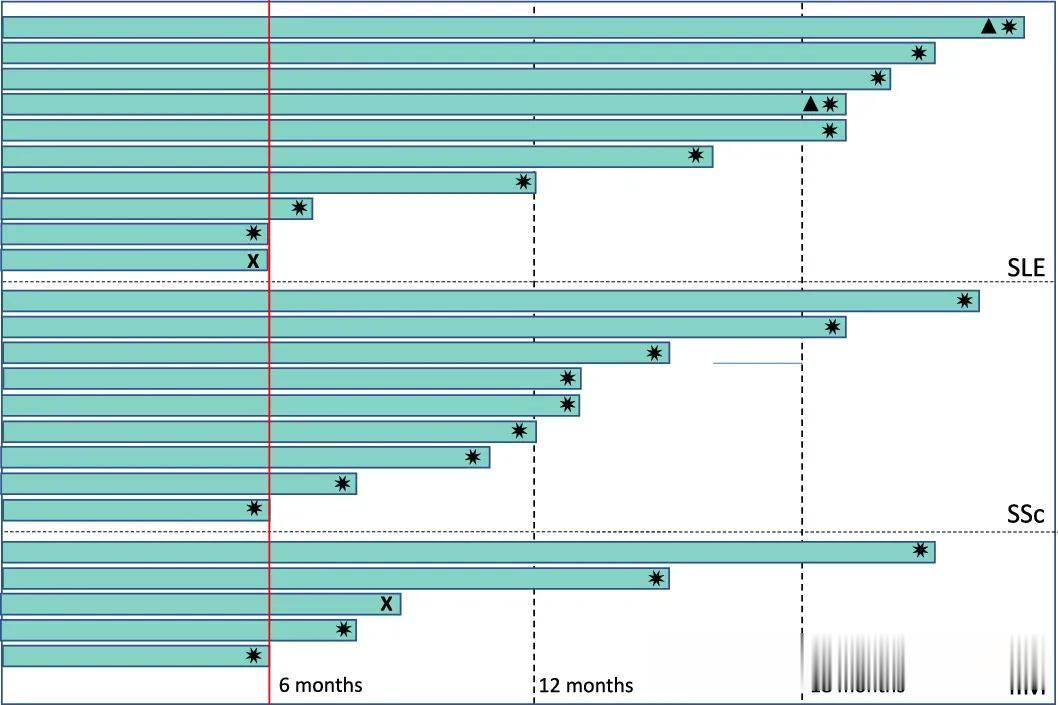
无药物缓解/无进展状态持续时间
CASTLE研究证实了Zorpo-cel在三种不同自身免疫性疾病中应用的可行性、安全性与有效性,为后续开展关键临床试验奠定了基础。
讨论
CASTLE研究纳入的患者均患有高度活动、病情危重且难治的自身免疫病,其病情进展急需得到快速控制。受试人群相对年轻(中位年龄39岁),病程较短(中位4年),但在此期间既往接受过无效免疫抑制治疗方案的中位数达4种,这反映出疾病的侵袭性以及对有效治疗手段的迫切需求。
尽管这类病情危重且呈进展性的患者仅占SLE、SSc、IIM患者中的一小部分,但在发生不可逆脏器损伤前,他们能从CD19 CAR-T细胞疗法这类深度免疫干预治疗中获益最大。尤为值得关注的是,全部24例患者均实现了稳定的无免疫抑制剂、无糖皮质激素状态,该状态不仅维持至6个月研究终点,最长随访时长更是达到23个月。
CASTLE研究还验证了此前的发现:CD19 CAR‑T细胞治疗并不会清除疫苗免疫记忆,患者既有的疫苗诱导IgG免疫应答基本保持完整,同时可清除大部分(但并非全部)自身抗体。部分自身抗体显著下降,但尚未发生血清学转阴,提示随着随访时间延长仍可能进一步下降。部分自身抗体在治疗后仅有中度降低,提示其产生至少部分依赖浆细胞。由于浆细胞通常不表达CD19,因此可逃逸CD19 CAR‑T细胞介导的细胞毒性作用。
总之,CASTLE研究为自身免疫病的CD19 CAR-T细胞治疗提供了大量新的研究依据,也将助力Zorpo-cel在自身免疫病领域关键临床试验的设计与开展。
— END —

新干细胞者说
- 科普 情怀 责任 -