糖尿病周围神经性病变(DSPN)是2型糖尿病最常见的慢性并发症,超过一半的糖尿病患者迟早要面对它。
手脚麻木、针刺样疼痛、烧灼感,走路像踩在棉花上,夜里疼得睡不着——这些症状不是暂时的,而是会持续进展。最终,足部溃疡、感染、截肢的风险会一步步逼近。
长期以来,临床治疗只能“治标”:营养神经、止痛,症状可能暂时缓解,但受损的神经组织无法修复,病变仍在悄悄加重。
2025年,《Cell Metabolism》刊发的中山大学杨志刚团队研究,第一次给出了不同的答案:粪便菌群移植(FMT)可以通过重建肠道微生态、减轻全身炎症、激活神经再生,实现糖尿病周围神经性病变的实质性逆转。
研究纳入了63例2型糖尿病合并DSPN的患者。所有人病程≥1年,疼痛视觉模拟评分(VAS)≥6/10,并且经神经电生理检查确认存在神经传导速度减慢。
他们被随机分为两组:一组接受健康供体的肠道菌群移植,另一组接受自体菌群移植(作为对照)。两组都维持统一的基础降糖和生活方式管理。
84天随访后,差异清晰显现。
FMT组的肢体神经传导速度比基线提升了27%,腓肠神经纤维密度增加了31%。疼痛VAS评分平均下降了3.2分。更重要的是,35%的患者足底浅感觉、深感觉完全恢复正常,肢体不适症状基本消失。
而对照组的各项指标均无明显改善。这说明,真正起作用的不是移植过程本身,而是健康异体菌群带来的生态重建。
研究团队通过机制研究,理清了DSPN的发病逻辑。
DSPN患者普遍存在一个共同问题:肠道菌群多样性显著降低。产短链脂肪酸的有益菌大量减少,肠道屏障随之受损。
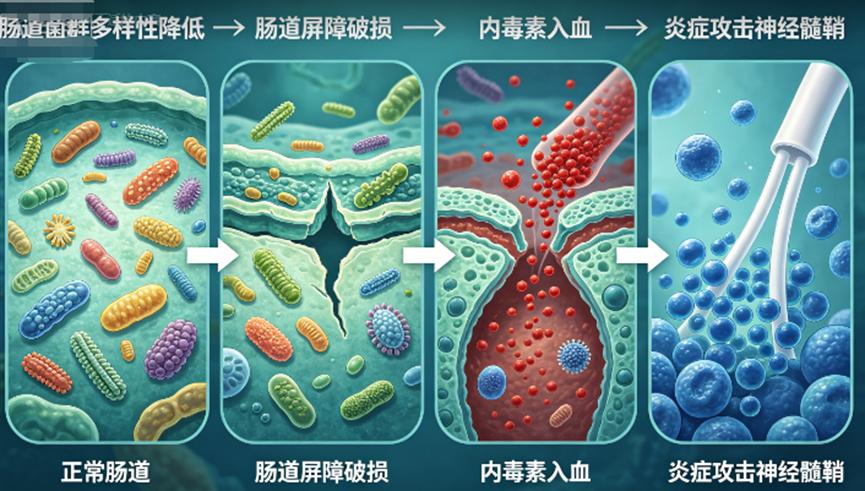
破损的肠道屏障像一扇关不上的门。内毒素从肠道渗漏入血,诱发全身持续性低度炎症。肿瘤坏死因子(TNF-α)、白介素-6(IL-6)等促炎因子水平异常升高。
这些促炎因子直接攻击周围神经的髓鞘结构,损伤神经轴索。神经信号传导出现障碍——这就是DSPN发病的核心上游驱动因素。
而FMT的干预逻辑完全不同。
健康供体中的有益菌群在患者肠道内快速定植。产丁酸菌等优势菌群的占比显著提升。它们修复受损的肠道屏障,阻断内毒素渗漏入血,从源头抑制全身炎症反应。
与此同时,这些有益菌还能上调神经生长因子(NGF)的表达,启动神经髓鞘修复和轴索再生程序。
整个过程形成了一条完整的链条:重建肠道微生态 → 阻断炎症损伤 → 促进神经再生。不是压制症状,而是修复病因。
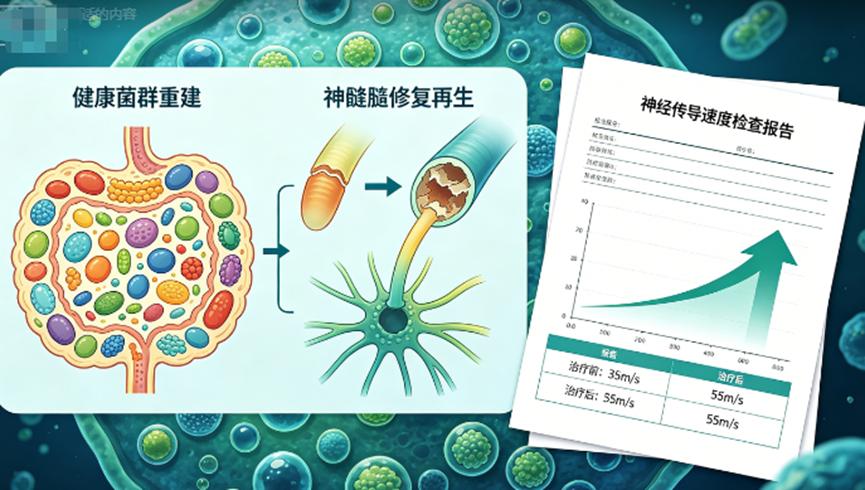
这项研究的突破在于,它重新定义了DSPN的发病本质。
糖尿病周围神经性病变不是单纯的局部神经损伤。它是“肠—神经轴”调控失衡引发的全身性代谢微生态疾病。肠道菌群紊乱,是重要的始动因素。
传统药物只能对症止痛、营养神经,无法打断上游的炎症驱动。而FMT从上游纠正肠道菌群失衡,切断炎症损伤通路,帮助受损神经结构真正修复。
当然,这项技术仍在临床研究阶段。长期安全性、菌株适配性、个体差异等问题还需要更多数据。但对于那些被神经性病变折磨多年、常规治疗无效的患者来说,肠菌移植提供了一条全新的出路——从“缓解症状”到“逆转病变”,这个转身本身,就是治疗理念的一次深刻进化。