前言
“慢加急性肝衰竭(ACLF)主题月评”是中国慢(加急)性肝衰竭联盟受《国际肝病》编辑部邀请,制作的ACLF相关学术月评专栏。本专栏每月以ACLF某一特定领域为主题展开,旨在普及ACLF的概念及意义、帮助读者快速了解有关领域的进展。希望本专栏对无论是需要了解相关领域热点的肝病专家及研究人员,或是需要实用知识、活跃于临床一线的医务工作者,均能有所裨益。
本期月评阐述了“四步动态分诊”实现肝硬化急性加重患者分层管理。最后对本月(2026.02.21-2026.03.20)PubMed上更新的ACLF相关重要文献进行简评。

关于作者:
中国慢(加急)性肝衰竭联盟(Chinese Acute-on-chronic liver failure Consortium,Ch-CLIF-C)是由上海交通大学附属仁济医院消化内科李海教授牵头,由全国15家三甲医院感染科/肝病中心共同参与成立的肝病科研合作团队,致力于探索慢加急性肝衰竭(ACLF)的发病机制、制定基于高询证等级的乙肝高流行区ACLF诊断标准。目前团队开展了全球已报道入组数最多的ACLF前瞻性多中心队列研究“CATCH LIFE”(Chinese AcuTe-on-CHronic LIver FailurE),包含2个大型队列(入组2600例的探索队列与入组1370例的验证队列)。
本期责任编辑

李海教授
上海交通大学医学院附属仁济医院消化内科主任医师,卫生部消化重点实验室副主任,目前担任上海医学会临床流行病学与循证医学分会主任委员。研究方向为慢加急性肝衰竭。牵头组织全国14家三甲医院肝病中心开展慢加急性肝衰竭前瞻性研究(CATCH-LIFE Study),该研究入组3970余例患者,成为全球入组数量最多之一的慢加急肝衰竭领域临床研究。该多中心临床研究目前已发表30余篇原创性论著。
本期责任副编辑

张艳
上海交通大学医学院附属仁济医院消化内科住院医师,研究方向为慢加急性肝衰竭。主持国自然青年、上海市扬帆等项目,以第一作者在Journal of Hepatology、Clinical Gastroenterology & Hepatology等杂志发表论文4篇,参与发表论文10余篇。
主题述评肝硬化急性加重(Acute exacerbation of cirrhosis)是肝病领域的常见问题。面对汹涌而来的失代偿患者,急诊和病房医生每时每刻都在面临艰难抉择:谁必须进ICU抢救?谁可以留在普通病房?谁又能够安全地下放到基层医院随访?李海教授团队基于肝硬化急性加重患者的全病程自然史,创新性地提出“四步动态分诊”,为打通三甲医院与基层医疗的双向转诊、实现医疗资源精准下沉提供了极具价值的“实战路线图”。
01
研究背景与临床需求
肝硬化急性加重患者从发病到随访,需要跨越四个生死攸关的决策节点:①门/急首诊(门/急诊)→②入院分诊→③院内演变→④出院后监测。而传统预后研究往往只关注患者某一横断面的病情,忽略了该疾病在院内及出院后的动态演变,缺乏涵盖全流程的连续性分级标准,造成临床上普遍存在专科医疗资源过度消耗与高危患者早期识别不足并存的认知空白。
02
核心发现:四步动态追踪,精准揭示显著生存差异
本研究对CATCH-LIFE队列肝硬化急性事件住院患者完成了全病程动态追踪,精准切分了不同临床阶段患者流向与死亡风险。
肝硬化急性加重患者首诊时可以根据有无合并急性失代偿(AD)事件(包括肝性脑病、食管胃底静脉曲张破裂出血、显性腹水、明确部位感染和/或黄疸)分成转归截然不同的两组患者。肝硬化AD患者的90天死亡率为12.7%,而肝硬化非AD患者的死亡率仅为1.8%。
以AD为临床表现的患者入院后,住院期间进展为ACLF患者90天死亡率高达28.7%。而入院后仅以肝硬化并发症为临床表现的患者90天死亡率仅为3.9%
肝硬化并发症治疗好转出院患者,根据出院3月内是否再次出现AD需要住院可分为不稳定性肝硬化(UDC)与稳定性肝硬化(SDC)两群患者,UDC患者1年死亡率高达30.4%,而SDC患者1年死亡率仅为3.8%。
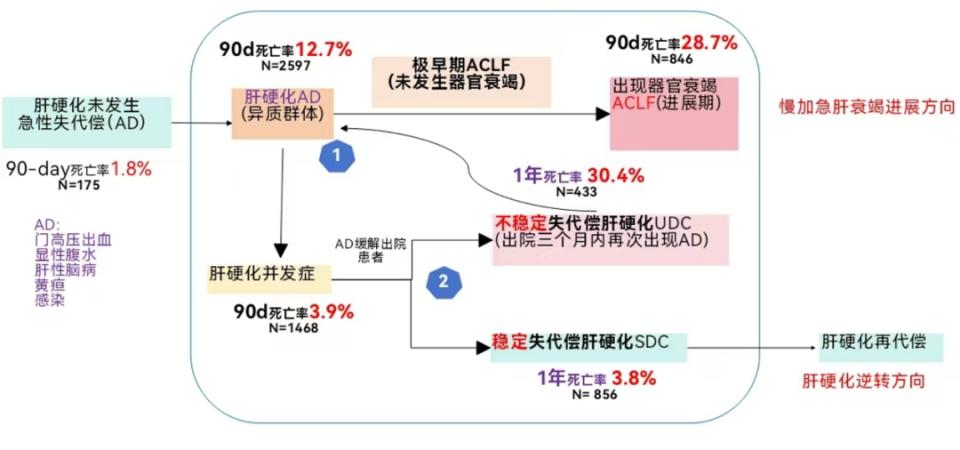
图1.CATCH-LIFE队列肝硬化急性事件住院患者全病程数据
03
临床启示:建立临床管理路径,让医疗资源真正用在刀刃上
基于肝硬化急性加重患者的全病程动态追踪结果,本研究提出了一项分级诊疗与管理路径(图2):
①首诊决断(肝硬化AD vs. 非AD)
肝硬化患者就诊时,首诊需明确是否发生急性失代偿(AD),包括肝性脑病、静脉曲张破裂出血、显性腹水、感染和/或黄疸。AD患者短期死亡风险高,应收治于三级医院或肝病专科;非AD患者病情稳定,可分流至基层或非专科病房。此分流策略有助于释放重症医疗资源,同时需建立双向转诊机制,以便非AD患者恶化时及时转入专科。
②入院分诊(肝硬化ACLF vs. 非ACLF)
确诊AD的住院患者,入院时应评估是否存在器官衰竭。若为ACLF,其死亡风险极高,需强化治疗与器官支持;若无,则可收治于普通专科病房,但仍需密切监测病情变化。
③院内演变(早期ACLF vs. 稳定非ACLF)
入院时非ACLF的肝硬化患者中,约25%可在28天内进展为早期ACLF。传统经验性观察存在滞后,亟需在器官衰竭前识别高危人群并提前干预。团队前期开发的ACLF预警试剂盒正处于真实世界研究阶段,未来有望在入院48小时内提供预警信息,为阻断病情恶化争取黄金窗口期。
④出院后监测(UDC vs. SDC)
病情好转出院的患者预后差异显著,出院后3个月内是否因急性事件再入院直接影响长期生存率。出院时精准预测患者转归,有助于优化院外管理:高危(UDC)患者需在三甲医院密切随访,低危(SDC)患者可下放至基层机构进行常规慢病随访。
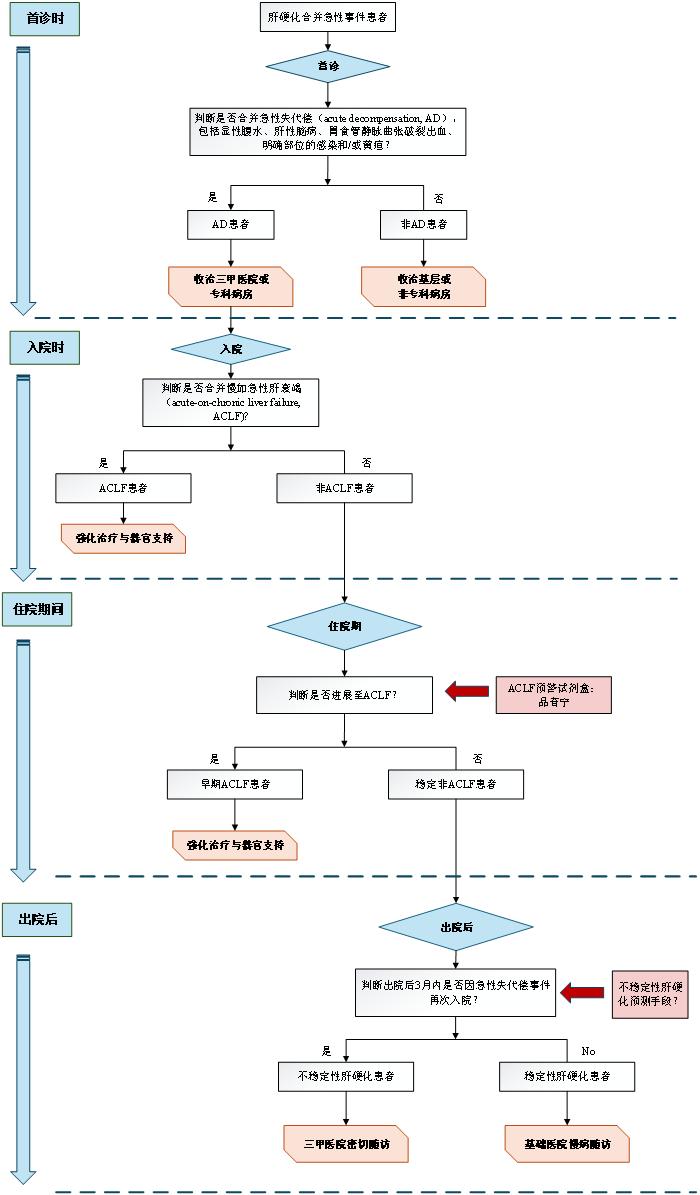
图2.肝硬化急性加重患者“四步动态分诊”
04
总结与展望
我们建立的“四步动态分诊”临床管理路径不仅可以加强对危重患者的管理,还可以缓解沉重的医疗压力,可以优化临床资源分配。此外,我们期望在未来随着新型IVD诊断工具的介入,能够在每一个生死的十字路口为患者指明最安全的方向。
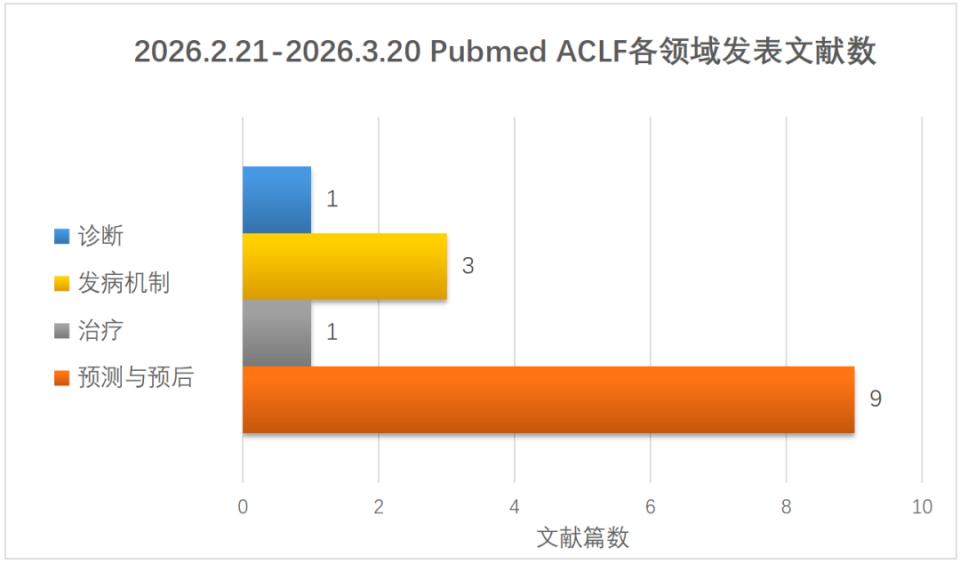
近一月ACLF研究优秀论文简评2026.02.21-2026.03.20在PubMed上在线发表关于ACLF相关文献共14篇,涉及诊断及预后、治疗与发病机制,具体分布见下图。
01
Xiang X, Zhu J, Jiang J, et al. Unique gut microbiota and metabolomic profiling as biomarker of post-transplant recovery in acute-on-chronic liver failure after liver transplantation. Appl Microbiol Biotechnol. 2026;110:89. doi:10.1007/s00253-026-13774-5(IF=4.3)
简述:该研究是一项回顾性观察研究,旨在分析慢加急性肝衰竭(ACLF)患者在肝移植(LT)术后早期肠道菌群和代谢谱特征,并探讨其与术后移植物功能不全的关系。研究纳入了2022年10月至2024年6月间接受肝移植的69例患者(包括24例ACLF、32例肝硬化和13例肝细胞癌患者),并采集患者术后1个月内的粪便样本进行16S rRNA和非靶向代谢组学测序。
研究结果显示,ACLF患者在肝移植术后表现出独特的肠道菌群和代谢谱特征。与肝硬化和肝细胞癌患者相比,ACLF组患者的肠道菌群Beta多样性显著改变,且g_Anaerostipes(厌氧棒状菌属)显著减少。非靶向代谢组学数据分析显示,ACLF组中橘皮素(tangeritin)富集而坎地沙坦(candesartan)显著减少。网络分析进一步明确g_Anaerostipes是连接差异菌属和代谢物的核心节点。此外,研究发现肠道菌群与早期移植物功能不全密切相关,其中,g_Lachnoclostridium(毛螺菌属)被认为是预测肝移植术后恢复的潜在指标 。
简评:肠道微生态失调被认为是驱动ACLF系统性炎症的关键因素。该研究揭示了ACLF患者即便在肝移植后仍具有独特的肠道菌群和代谢特征,ACLF患者g_Anaerostipes显著减少,可能是肠道菌群和代谢特征改变的核心环节。此外,g_Lachnoclostridium被发现可预测肝移植术后恢复情况,可为评估术后移植物功能恢复提供新维度。这些发现为优化ACLF患者移植后的精准医疗和预后监测提供了重要依据。
02
Splith K, Berndt N, Haber PK, et al. Immune biomarkers predicting response to G-CSF in acute-on-chronic liver failure: results from a GRAFT trial sub-study. Hepatol Int. Published online March 7, 2026. doi:10.1007/s12072-026-11069-5(IF=6.1)
简述:粒细胞集落刺激因子(G-CSF)治疗ACLF的效果在亚洲和欧洲研究中存在着争议。该研究是针对德国GRAFT试验(NCT02669680)进行二次分析,旨在寻找能够预测ACLF预后以及对G-CSF治疗产生反应的免疫标志物。研究分析了79例随机分配至G-CSF组(n=40)和标准治疗组(n=39)的患者的血样,检测血标本细胞因子、免疫细胞表型及功能、细胞游离DNA(cfDNA)等指标。
结果显示,基线血浆VEGF-A水平是ACLF无移植生存(TFS)的显著预测因子(AUC:0.70,95%CI:0.56-0.84)。通过对基线循环免疫细胞进行非监督层次聚类分析,研究者在G-CSF治疗组中识别出一个特定的亚群,该亚群患者的生存期显著优于对照组(中位生存期102天 vs 16天,P=0.002)。此外,淋巴细胞中CD39+比例的升高被证实是G-CSF治疗后预后不良的独立危险因素(HR:1.05,95%CI:1.01-1.09,P=0.008),提示高CD39表达的患者较难从G-CSF治疗中获益。
简评:虽然GRAFT试验结果为阴性,但本项亚组研究证明了ACLF患者的异质性。VEGF-A可用于患者整体预后评估,而基于免疫细胞簇(特别是CD39+淋巴细胞比例)的分析则提供了一种筛选G-CSF治疗受益人群的手段。这强调了在未来针对ACLF的免疫调节治疗中,基于生物标志物进行患者精准分层的重要性。
03
Thiyagarajah K, Sonnenberg J, Görgülü E, et al. Higher prevalence of cytomegalovirus and Epstein-Barr virus in acute-on-chronic liver failure. JHEP Rep. 2026;8:101627. doi:10.1016/j.jhepr.2025.101627(IF=7.5)
简述:在约40-60%的ACLF病例中,常规临床检查无法明确ACLF的诱发因素。该研究利用探索队列(n=211)和外部验证队列(n=153)探索巨细胞病毒(CMV)和EB病毒(EBV)在ACLF患者中的流行特征及其与疾病进展的关系。研究通过高灵敏度多重qPCR检测血清巨细胞和EBV病毒DNA,并结合细胞因子分析评估系统性炎症状态。研究结果显示,ACLF患者的巨细胞病毒血症(25.6% vs 8.9%,P<0.01)和EBV病毒血症(16.3% vs 6.6%,P<0.05)发生率显著高于非ACLF患者。在ACLF患者中,病毒血症患者未发现ACLF诱因的比例显著高于无病毒血症患者(54.8% vs 26.5%,P<0.05)。此外,CMV DNA血症与肝衰竭(P<0.001)及90天病死率(P<0.001)密切相关,且此类患者呈现出独特的促炎细胞因子特征。血清学证据表明,绝大多数病例属于病毒再激活而非原发感染。
简评:该研究首次明确指出,既往被忽视的CMV和EBV再激活可能是诱发或加重ACLF的重要诱因。CMV和EBV病毒可能通过加剧肝脏炎症和损害肝细胞功能促进ACLF病程进展。研究建议对失代偿期肝硬化患者进行常规CMV和EBV DNA筛查,这为ACLF早期干预和预防提供了一个全新的、可干预的临床靶点。
各研究中心PI