近日,深圳默赛尔生物医学科技发展有限公司自主研发和自主申报的无血清细胞冻存液(金装版),已顺利获得国家药品监督管理局药用辅料(高风险)登记资质。
查询网址:https://zwfw.nmpa.gov.cn/web/index

为什么要进行药用辅料登记?
药用辅料作为药品研发与生产的关键组成部分,直接影响制剂性能、药品安全性与有效性,更是推动医药产业实现高质量发展的重要支撑。
药用辅料登记要求辅料生产企业提交详细的生产工艺、质量控制、杂质研究、稳定性研究等资料。通过登记,表明细胞冻存液的质量标准、生产过程符合药品监管要求,能更好地保证质量的一致性和安全性,为下游制剂企业使用提供信心。
细胞治疗产品等生物制品通常需要使用高质量、合规的辅料。根据药品监管要求,药品制剂生产企业在进行药品注册时,必须使用已登记或符合要求的药用辅料。细胞冻存液获得登记后,可以与制剂产品进行关联审评审批。这大大简化了下游制剂企业的注册申报流程,因为它能直接引用已备案辅料的资料,避免了制剂企业需要独立提供辅料全部详细资料的繁琐。
NO.1[ 产品介绍 ]
无血清细胞冻存液(金装版)
预混式即用型细胞保护剂,使用临床级渗透性和非渗透性冷冻保护剂、 以及细胞膜保护剂;细胞毒性低,细胞复苏活率高,无动物源组分,成分明确,无需程序降温,集安全、有效、便捷、可靠于一身,适用于申报细胞药物的企业,极大降低细胞药物申报的验证工作与申报难度。
适用于:造血干细胞、间充质干细胞等干细胞的储存;PBMC、DC、T细胞、NK细胞等免疫细胞的储存及其他各种类型哺乳动物细胞的储存。
已取得中国医疗器械I类备案:粤深械备20220337
已取得美国FDA DMF备案:041841


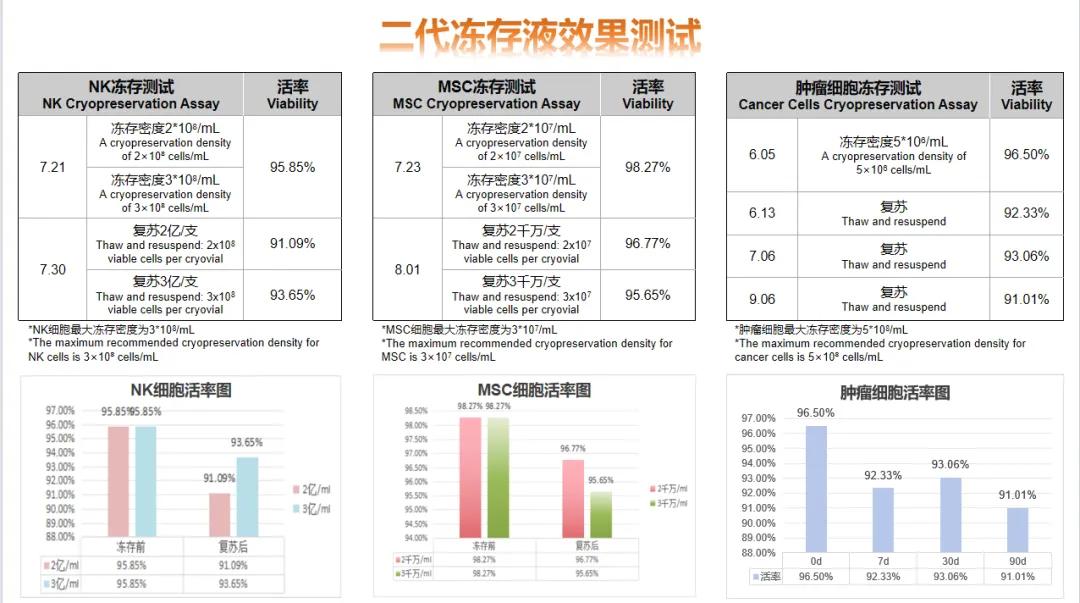
利用细胞冻存液金装版冻存复苏的最大密度细胞数据
默赛尔生物人NK杀伤细胞无血清培养基
现已取得中国医疗器械II类注册
为国内首家
NO.2[ 产品介绍 ]人NK细胞无血清培养基

默赛尔自主研发的人NK细胞无血清培养基不含任何动物血清、外源生长因子或不明成分的添加剂,与自然杀伤细胞培养试剂盒联合使用可高效地将人外周血单个核细胞诱导分化成NK细胞,并在短时间内大规模扩增,获得大量高纯度、高活性的可供临床使用的NK细胞。
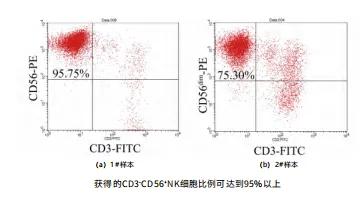
采集血液30ml-50ml,联合使用自然杀伤细胞培养试剂盒和自然杀伤细胞无血清培养基进行培养,17天内可使NK细胞绝对数扩增1000倍以上,细胞终数量>50亿;获得的CD3-CD56+NK细胞比例可达95%以上,其中发挥主要杀伤作用的CD3-CD56dimNK细胞比例超过75%,活细胞比例>95%。
NK细胞纯度
NK细胞杀伤活性

备案查询
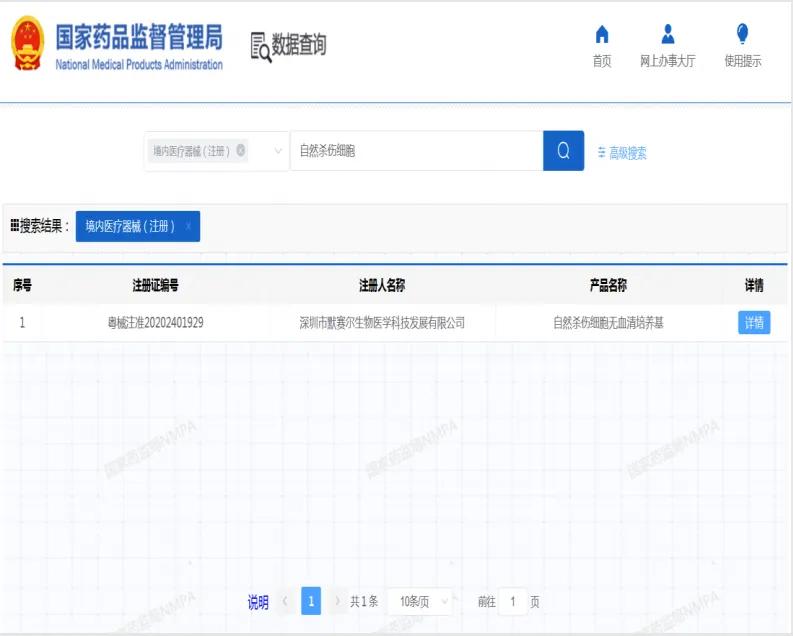

至此,默赛尔生物成为全国首家在免疫细胞/自然杀伤细胞领域获得国际权威及国内认证双备案的企业,为接下来CAR-NK细胞药物申报及抗肿瘤靶向细胞药的研发迈出重要一步。
默赛尔生物现有国内医疗器械备案、药用辅料登记及DMF备案产品一览:
产品名称
产品批号
规格
资质
1
免疫细胞无血清培养基
MCM-001
1L/瓶
DMF备案号:040823
2
人NK细胞无血清培养基
MCM-002
1L/瓶
II类注册:粤械注准20202401929
3
细胞冻存液
(无血清非程序)
MCL-001
100ml/瓶
I类备案:粤深械备20160265号
4
无血清细胞冻存液(金装版)
MCL-002
100ml/瓶
I类备案:粤深械备20220337
DMF备案号:041841
CDE高风险药用辅料登记号:F20250000495

— END —

新干细胞者说
- 科普 情怀 责任 -