
导语:BRAF突变晚期结直肠癌患者接受标准化疗联合抗VEGF治疗后,中位生存期仍不足一年。当靶向BRAF的单药屡屡因EGFR介导的反馈激活而落败,临床是否只能接受这种注定耐药的结局?
图源:CMT
BRAF突变肠癌靶向治疗困局待解,EGFR/BRAF双抑制策略能否成为一线优选?BRAFV600E突变在结直肠癌中约占8-15%,这类肿瘤侵袭性强、对常规化疗反应差,中位总生存期显著短于野生型患者。传统一线治疗多采用双药或三药化疗联合抗血管内皮生长因子(VEGF)抗体,但客观缓解率不足45%,且极易继发耐药。单用BRAF抑制剂虽能阻断MAPK通路,却会因EGFR(表皮生长因子受体)快速再激活导致疗效昙花一现,这一反馈机制在2012年后被反复证实,却始终缺乏有效破解方案。
转机出现在EGFR/BRAF双重抑制概念的提出。BEACON研究率先在二线治疗中确立西妥昔单抗联合康奈非尼的疗效,BREAKWATER试验更进一步,将该组合推至一线并加入化疗。然而,由于BRAF突变肠癌发病率低,随机对照试验样本量受限,各靶向方案间始终缺乏头对头比较。更棘手的是,临床实践中医生面临多重抉择困境:抗VEGF与抗EGFR孰优?化疗强度如何把握?单用靶向药是否足够?这些问题因证据碎片化而悬而未决。
2025年9月,BMJ在线发表了一篇题为"Targeted therapy in advanced BRAF-mutated colorectal cancer: systematic review and network meta-analysis"的文章,通过网络荟萃分析整合直接和间接证据,在大样本人群中量化比较12种一线方案与14种后线方案的疗效与安全性,明确将化疗联合抗EGFR/BRAF双抑制推至一线治疗的首选地位,为这一小众却凶悍的肿瘤亚型提供了基于证据等级的精准治疗层级图。

本研究是一项系统综述与贝叶斯网络荟萃分析,旨在通过直接和间接比较,明确晚期BRAF突变结直肠癌各线治疗的最优靶向策略。研究团队遵循PRISMA网络荟萃分析扩展声明,预先在PROSPERO注册方案,检索PubMed、Embase、Cochrane图书馆和ClinicalTrials.gov从建库至2025年5月31日的所有文献,并补充美国临床肿瘤学会、欧洲肿瘤内科学会等国际会议摘要,最终纳入60项研究共4633例患者。
研究仅纳入组织学确诊的晚期BRAF突变结直肠癌患者,优先提取BRAFV600E亚组数据,要求各臂样本量≥10例以确保统计稳定性。治疗方案按药物类别而非具体品种分类,将12种一线策略归为抗EGFR基础组合、抗VEGF基础组合、抗EGFR/BRAF双抑制联合化疗与否、以及化疗单药等类别。这种分类法既维持了网络连通性,又避免了因药物细微差异导致网络碎片化。统计设计上,研究采用三层次分析方法:单臂荟萃分析汇总各方案客观缓解率、疾病控制率和≥3级不良事件发生率;配对荟萃分析处理有直接对照的研究;网络荟萃分析则通过马尔可夫链蒙特卡洛模拟,整合直接和间接证据,计算各方案生存获益的累积排序概率(SUCRA),以0-1的连续尺度量化疗效优劣。主要终点为总生存期(OS)和无进展生存期(PFS),次要终点包括客观缓解率(ORR)、疾病控制率(DCR)和≥3级不良事件,所有时间事件数据采用风险比(HR)及95%CI表示。
化疗联合双靶方案一线生存获益登顶,二线及后线治疗排序揭示精准选择逻辑研究共纳入60项研究4633例患者,其中一线治疗分析涵盖32项研究2460例患者。单臂荟萃分析显示,所有一线方案汇总客观缓解率为44.2%,但抗EGFR/BRAF双抑制联合双药化疗方案(DCT-anti-EGFR/BRAF)以67.0%的客观缓解率居首,显著高于抗EGFR基础方案的39.7%和抗VEGF基础方案的42.7%。网络荟萃分析进一步证实,DCT-anti-EGFR/BRAF在总生存期上表现最优,相较于传统DCT-anti-VEGF方案,死亡风险降低51%(HR0.49, 95%CI0.36-0.66),这一优势在统计学和临床意义上均显著。
更令人瞩目的是贝叶斯排序结果(图1),DCT-anti-EGFR/BRAF在总生存(SUCRA=0.94)和无进展生存(SUCRA=0.93)两项关键指标上均排名第一,而单药化疗联合抗EGFR/BRAF(SCT-anti-EGFR/BRAF)紧随其后(OS SUCRA=0.90),表明在耐受性较差的患者中单药化疗联合双靶也是合理选择。二线及后线治疗分析纳入30项研究2173例患者,网络荟萃分析显示抗EGFR/BRAF±MEK抑制剂(丝裂原活化蛋白激酶激酶抑制剂)方案优势明显,其中抗EGFR/BRAF/MEK三靶方案总生存SUCRA值达0.82,客观缓解率SUCRA值0.89,均位列第一,但≥3级不良事件风险较单纯抗EGFR/BRAF增加51%(OR1.51, 95%CI1.10-2.07),提示需权衡疗效与毒性。
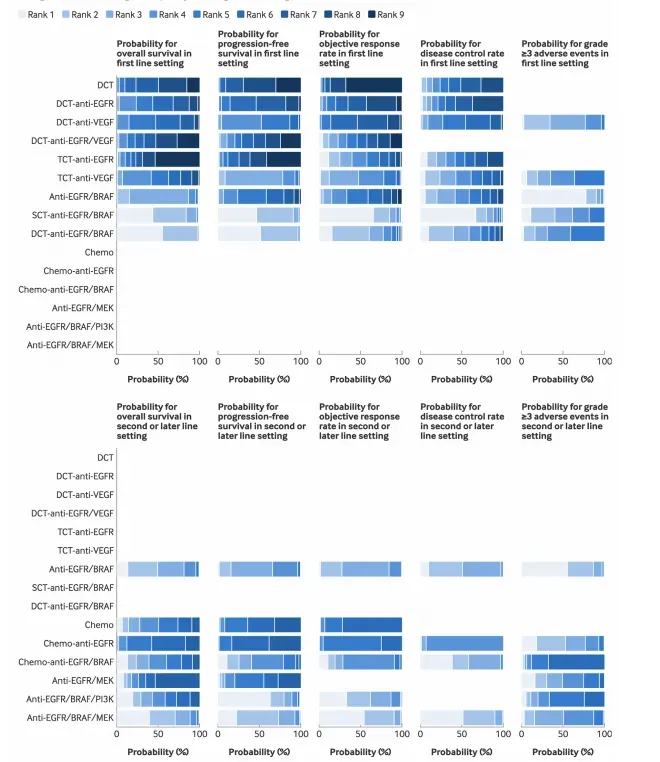
图1 贝叶斯排序分析的一线治疗方案疗效和安全性结果
注:图中呈现了从第一到最后一的排序概率,以及累积排名曲线(SUCRA)值。SUCRA值越高,表示治疗方案在比较中的优先级越高。Chemo:化疗;DCT:双药化疗;EGFR:表皮生长因子受体;MEK:丝裂原活化蛋白激酶激酶;PI3K:磷脂酰肌醇3激酶;SCT:单药化疗。
安全性分析揭示重要权衡:DCT-anti-EGFR/BRAF在一线治疗中≥3级不良事件发生率最高,但其风险与DCT-anti-VEGF无统计学差异,而化疗-free的抗EGFR/BRAF方案安全性最优,不良事件发生率较化疗组合降低近50%。这一发现为临床决策提供清晰路径:体能状态良好者一线应接受DCT-anti-EGFR/BRAF以最大化生存获益,而虚弱患者可选择SCT-anti-EGFR/BRAF,后线治疗则优先考虑化疗-free方案。
总结本研究通过创新性地整合网络荟萃分析技术,在缺乏头对头试验的BRAF突变晚期结直肠癌领域,建立了基于证据等级的治疗方案优选体系。明确了抗EGFR/BRAF双抑制联合化疗在一线治疗中的金标准地位,使死亡风险较传统抗VEGF方案降低50%以上,同时揭示了治疗线数对化疗必要性的调控作用——后线治疗中靶向治疗单用或联合MEK抑制剂即可维持疗效,无需化疗增毒。研究还创新性地运用SUCRA排序将复杂比较转化为直观概率,为临床医生在12种一线和14种后线方案中快速决策提供可视化工具。尽管受限于试验水平数据而非个体病例数据,且部分亚组样本量较小,但其通过严格异质性检验和敏感性分析确保了结论稳健性,填补了NCCN和ESMO指南中方案排序证据的空白,直接推动精准治疗从有选择迈向最优选。
参考文献
Qin BD, Jiao XD, Wang Z,et al. Targeted therapy in advanced BRAF-mutated colorectal cancer: systematic review and network meta-analysis[J]. BMJ. 2025 Nov 19;391:e086026. doi: 10.1136/bmj-2025-086026.
“医学论坛网”发布医学领域研究成果和解读,供专业人员科研参考,不作为诊疗标准,使用需根据具体情况评估。
编辑:白术
审核:薄荷
封面图源:CMT