近年来,以司美格鲁肽(Semaglutide)和替尔泊肽(Tirzepatide)为代表的新型减重药物在临床上大放异彩,研究中帮助患者实现了10%至21%的显著减重。然而,临床数据表明,这类药物在一年内的停药率高达47%至65%。
但在真实的临床诊疗中,情况是否真的如此悲观?
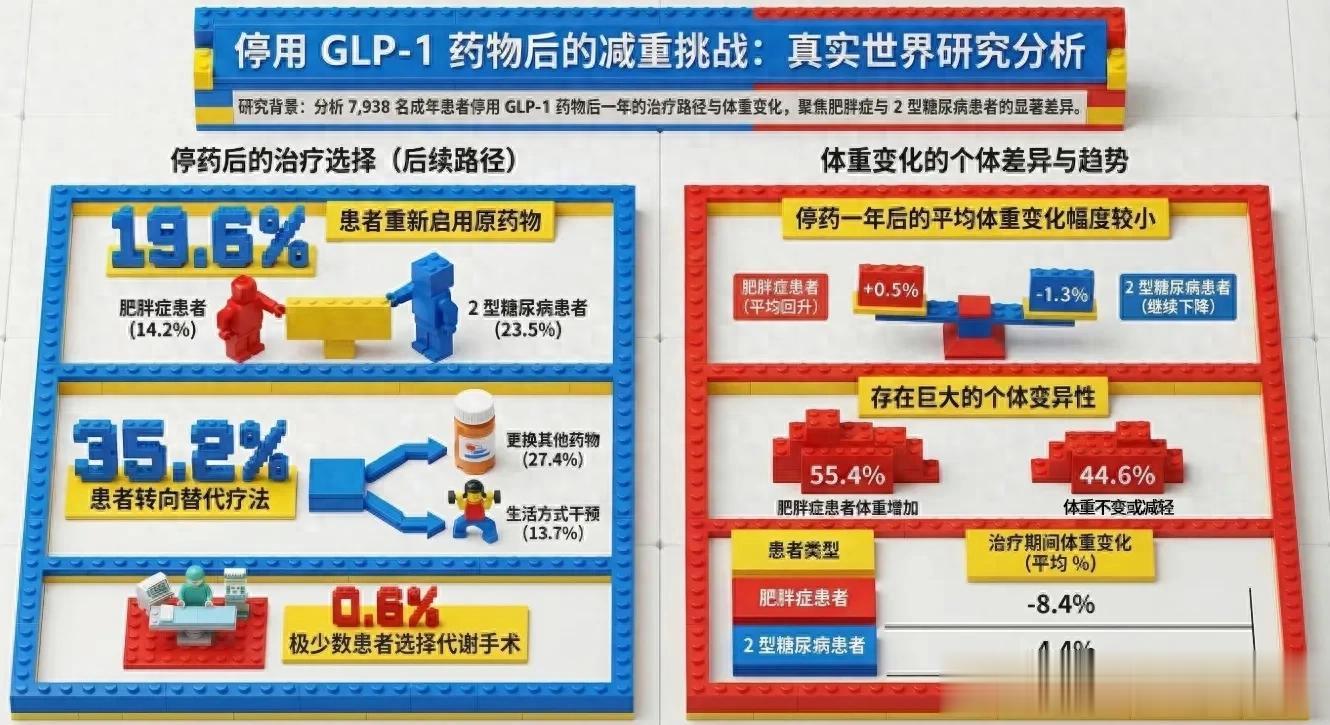
2026年3月12日发表于《糖尿病、肥胖与代谢》(Diabetes, Obesity and Metabolism)的研究,基于近8000例患者数据揭示了停药后的真实图景:一年内,19.6%的患者重启原药,35.2%转用替代方案;而肥胖症患者停药一年后的平均体重反弹仅0.5%。虽然温和的平均值背后是显著的个体差异,但研究给出了重要提示:停药并非治疗的真空期,而是启动新干预的关键窗口。
 PART 01真实世界的后续干预:停药不等于“放弃治疗”
PART 01真实世界的后续干预:停药不等于“放弃治疗”该研究依托美国克利夫兰诊所的电子病历系统,纳入了7938名在2021年至2023年间启动司美格鲁肽或替尔泊肽治疗,并于用药3至12个月后停药的成年患者。数据表明,在真实的医疗环境中,患者在停用初始药物后并未停止对体重的管理,而是积极采取了后续干预措施:
1.重新启用原药物
在停药一年内,19.6%的患者重新恢复了原药物的注射。
其中,因2型糖尿病(T2D)用药的患者复用率(23.5%)明显高于单纯为治疗肥胖的患者(14.2%),这可能与当前医保对糖尿病适应症的覆盖更为广泛有关。
2.寻求替代治疗方案
高达35.2%的患者在停药后接受了其他的肥胖替代治疗。具体而言:
27.4% 的患者开始使用其他药物(例如在司美格鲁肽与替尔泊肽之间相互转换,或使用芬特明、托吡酯等传统减重药物)。13.7% 的患者接受了专业的“生活方式干预”(如营养咨询、运动生理学家指导等)。0.6% 的患者最终接受了代谢与减重手术。
PART 02体重变化轨迹:整体反弹幅度微小在用药期间(从基线到停药),患者获得了切实的减重成效:肥胖症治疗患者平均减重8.4%,2型糖尿病治疗患者平均减重4.4%。
令人欣慰的是,与既往临床试验中观察到的普遍性剧烈反弹不同,本研究发现,在真实世界中停药一年后的平均体重变化幅度非常小:
肥胖症患者:停药一年后,平均体重仅微幅回升了 0.5%。2型糖尿病患者:停药一年后,平均体重甚至进一步下降了1.3%。
研究指出,正是由于患者在停药后广泛采取了重新用药、更换其他药物或强化生活方式等替代干预,才在很大程度上缓冲了预期的体重反弹。

图3 治疗期间至停药后长期的整体体重变化趋势
PART 03 个体差异不容忽视:平均值背后的“两极分化”尽管从“平均值”来看体重维持得相当平稳,但研究团队特意强调了背后巨大的个体差异。在临床实践中,停药后的走向呈现出明显的两极分化:
在最初因肥胖接受治疗的患者中,有44.6%的人在停药一年内体重继续下降或保持不变,但仍有55.4%的人出现了体重增加。在最初因2型糖尿病接受治疗的患者中,有56.4%的人体重下降或无变化,43.6%的人出现了体重反弹。
糖尿病患者之所以在停药后表现出更好的体重维持率,很大程度上得益于他们拥有更稳固的医疗保障,从而更容易获得其他降糖及减重药物的替代治疗。
PART 04临床启示:构建“停药后”的长期干预策略这项大规模真实世界研究释放了一个重要的医学信号:停用新型减重药物并不等同于减重干预的失败。
在实际临床中,患者可能因费用、耐受性等多种原因中断用药。但只要医患双方保持沟通,及时引入替代性体重管理方案(如更换药物、强化行为干预或考虑减重手术),依然有很大机会维持初期的减重成果。
目前,医疗界尚未针对这类新型减重药物的停用制定标准的循证临床指南。未来,亟需开展关于“不同替代疗法相对疗效”的进一步研究,从而为面临停药的患者量身定制科学、长效的体重管理策略。
参考文献
Gasoyan, H., Schulte, R., Boyer, C. B., Casacchia, N. J., Butsch, W. S., Le, P., Aminian, A., Griebeler, M. L., Burguera, B., & Rothberg, M. B. (2026). Obesity treatments and weight changes in clinical practice after discontinuation of semaglutide or tirzepatide. Diabetes, Obesity and Metabolism.