子宫内膜癌的分子分型已成为全球共识,其中TCGA分型体系将其分为四类:POLE突变型、MSI-H(dMMR)型、p53突变型(多伴TP53异常)、无特异性分子改变组。在临床实践中,大多数肿瘤仅符合一种分子特征,但约3%-11%的患者会同时携带两种及以上分子特征,这类肿瘤被定义为"多重分子特征子宫内膜癌"[1,3]。

在所有多重分类肿瘤中,dMMR合并TP53变异(MMRd-p53abn)是最常见的类型,占比约6.6%,远高于其他组合类型 [1]。
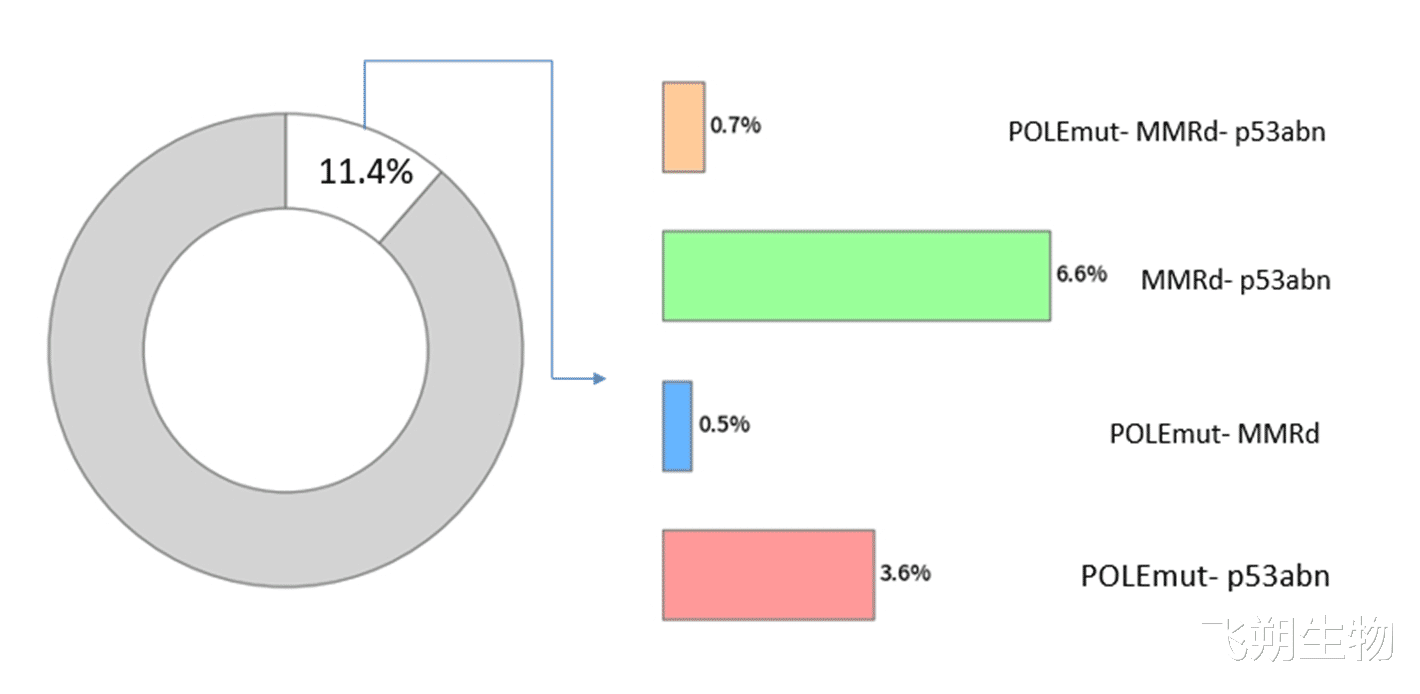
▲图1.多重分子特征子宫内膜癌分布占比
这一类型的发现,得益于全面的分子检测技术——仅通过免疫组化可能漏诊部分病例,而结合下一代测序(NGS)技术后,能更精准地捕捉到这类特殊分型。过去,临床对单一分子特征的预后判断已有明确认知:
单一TP53异常(p53abn):妥妥的"不良预后信号",研究数据显示,这类患者的5年复发风险高达34.3%,3年无病生存率仅38.0%,且多为晚期、非子宫内膜样癌,侵袭性强[1]。
单一dMMR(MSI-H):预后中等偏上,3年无病生存率约91.9%,复发率仅4.0%,且对免疫检查点抑制剂反应良好[1]。
当这两种特征同时出现在一位患者身上时,无论是患者还是医生,都难免担忧:会不会是"雪上加霜"?预后该如何判断?要不要调整治疗方案?这两个看似"矛盾"的分子特征,一个常与免疫治疗获益相关,一个多提示预后不佳,它们的"相遇"曾让临床判断陷入困境。
PART2关键发现:预后呈现"中间态",既不最差也不最优基于三大国际临床研究的大样本数据(累计纳入超过4000例子宫内膜癌患者),我们对MMRd-p53abn患者的预后规律有了明确答案:这类患者的预后呈现独特的"中间特征",既显著优于单一TP53异常患者,也略逊于单一dMMR患者[1-3]。
01.复发风险显著降低,生存获益明确
研究数据显示,MMRd-p53abn患者的复发率仅为7.1%,远低于单一TP53异常患者的23.3%;其3年无病生存率高达87.8%(95% CI:59.6-96.8),是单一TP53异常患者(38.0%)的2倍多,p<0.001[1]。
另一项纳入3518例患者的大型研究也证实,MMRd-p53abn患者的5年无病生存率达83.4%,远高于单一TP53异常患者的70.8%,差异具有统计学意义(p=0.024)[3]。这一数据充分说明,dMMR特征的存在,显著"中和"了TP53变异带来的不良预后影响。
02.临床特征更温和,侵袭性较低
基因检测结合临床病理分析发现,MMRd-p53abn患者多呈现"低侵袭性"临床特征 [1]:
分期偏早:60.7%为I-II期,仅39.3%为晚期(III-IV期),而单一TP53异常患者的晚期比例高达53.4%;
病理类型更优:85.2%为子宫内膜样癌,非子宫内膜样癌比例仅14.8%,远低于单一TP53异常患者的50.0%;
恶性特征少见:弥漫性淋巴血管间隙浸润发生率仅18.5%,淋巴结转移率22.2%,均低于单一TP53异常患者。
这些临床特征为MMRd-p53abn患者的良好预后奠定了基础,而这些特征的精准识别,离不开基因检测与病理分析的结合。
03.TP53变异仍存额外风险
与单一dMMR仍有差距,TP53变异仍存额外风险。值得注意的是,MMRd-p53abn患者的预后仍略逊于单一dMMR患者[1]:
复发率:7.1%
vs 4.0%;
3年无病生存率:87.8% vs 91.9%;
高分级比例:55.6%为G3级,高于单一dMMR患者的22.2%(p=0.001)。
这提示TP53变异虽然不是主导因素,但仍会给肿瘤带来轻微的额外风险,这一细节只有通过精准的分子分型才能捕捉到,也为后续治疗方案的微调提供了依据。
PART3.深层机制:TP53变异在这里可能是"继发突变"为什么TP53变异的"坏影响"会被dMMR"中和"?这背后的分子机制,通过NGS基因检测技术得以揭示 [1,3]:
1.变异发生时序不同,TP53多为"继发事件"
研究发现,在MMRd-p53abn肿瘤中,TP53变异多表现为"亚克隆表达",约18.2%的患者会出现这一特征,而单一TP53异常患者中仅2.9%出现(p=0.005)[1]。
亚克隆表达意味着TP53变异是肿瘤进展过程中"后来出现"的变化,而非驱动肿瘤发生的核心因素。相比之下,dMMR作为更早出现的"驱动事件",已经塑造了肿瘤的主要生物学行为,这也是dMMR能主导预后的关键原因。
2.分子图谱更贴近dMMR,而非TP53异常
通过对TCGA数据库中肿瘤样本的基因聚类分析发现,MMRd-p53abn肿瘤的单核苷酸变异(SNV)特征和拷贝数改变模式,更接近单一dMMR肿瘤(20/23例聚类于dMMR组),而非单一TP53异常肿瘤(仅3/23例聚类于p53abn组)[3]。
这一分子层面的证据进一步证实,dMMR是主导这类肿瘤生物学行为的核心特征,TP53变异更像是"继发突变",并未改变肿瘤的本质属性。
3.免疫浸润优势保留,为免疫治疗提供基础
dMMR肿瘤的典型特征是高肿瘤突变负荷(TMB)和丰富的免疫浸润,而这一特征在MMRd-p53abn肿瘤中得以保留 [2,3]:
肿瘤浸润淋巴细胞(TILs)和淋巴细胞比例较高;
微卫星不稳定性(MSI)阳性率达92.3%;
MMR蛋白表达异常以MSH6丢失为主(55.6%),这类异常更易引发免疫反应。
这也是MMRd-p53abn患者仍能从免疫治疗中获益的关键机制。
PART4临床启示:精准基因检测指导下的治疗决策MMRd-p53abn患者的治疗决策,应基于精准的基因检测结果,避免"一刀切"[1,2]:
1.避免过度治疗,参考dMMR肿瘤治疗原则
由于dMMR是主导特征,MMRd-p53abn患者无需因TP53变异而盲目强化治疗:
早期患者(I-II期):以手术治疗为主,必要时联合辅助放疗(如阴道近距离放疗),无需常规加用高强度化疗;
中高危患者:可根据是否存在LVSI、肌层浸润深度等因素,个体化选择辅助治疗方案,无需因TP53变异而升级为放化疗联合。
2.免疫治疗仍可获益,晚期患者优先考虑基于dMMR的分子特征,MMRd-p53abn患者仍可能从免疫检查点抑制剂治疗中获益[2]:
晚期或复发患者:可优先考虑PD-1/PD-L1抑制剂单药治疗,或联合低剂量化疗;
临床数据支持:KEYNOTE-158研究显示,dMMR/MSI-H子宫内膜癌患者接受帕博利珠单抗治疗的客观缓解率(ORR)达46%,其中部分患者为MMRd-p53abn分型[2]。
3.强调全面分子检测,避免漏诊和误判
研究证实,仅依靠免疫组化(IHC)可能漏诊部分多重分类肿瘤[1]:
TP53测序能额外发现18.9%的MMRd-p53abn患者,这些患者的p53免疫组化表现正常;
部分MMRd-p53abn患者存在多灶性TP53突变(17.9%),仅通过IHC无法识别这类复杂变异。
参考文献
[1] Int J Gynecol Cancer. 2024 Feb 5;34(2):229-238.
[2] Int J Mol Sci. 2024 Jan 15;25(2):1056.
[3] J Pathol. 2020 Mar;250(3):312-322.
声明:本文仅用于分享,如涉及版权等问题,请尽快联系我们,我们第一时间更正,谢谢!