说明:本文华算科技介绍了循环伏安法(CV)的原理、作用及应用。CV是一种通过施加三角波电位并记录电流响应的电化学测量方法,可用于判断反应的可逆性、测定动力学参数、分析电极表面吸附行为以及评估电极材料性能,在能源存储和电催化领域具有广泛应用。
01、什么是循环伏安法(CV)?
是一种常用的电化学测量方法,属于伏安法的一种,是通过在工作电极上施加一个线性变化的电压,并在达到设定的终止电位后立即反向扫描,形成一个对称的三角波电位信号,同时记录通过电极的电流随电位变化的曲线,即CV。
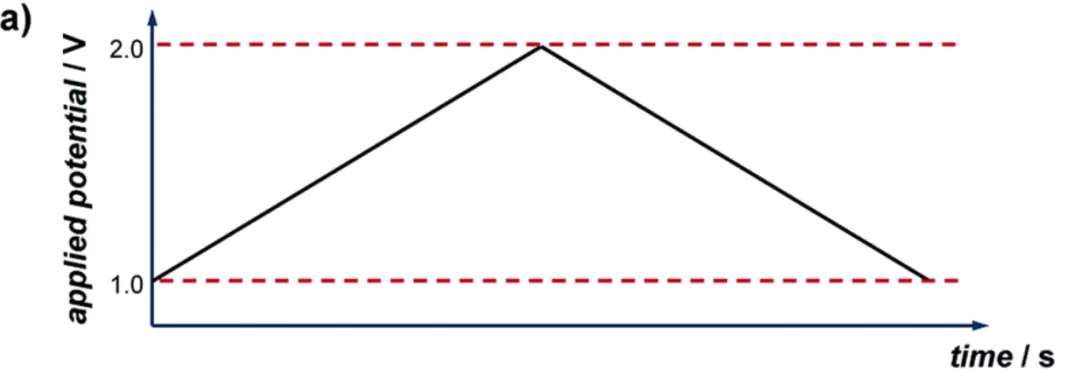
1当电位达到足够的负正电位时,导致化学物质在电极表面氧化或还原,产生电流对于,当电极电位朝正方向扫描时,氧化还原活性物质在电极表面发生氧化,导致观察到氧化电流从氧化还原事件的起始电位开始(此时背景减去电流变为非零)。
2E)继续上升时,氧化在热力学上变得更加有利,电流继续增加,直到氧化过程最终受到物质向电极表面扩散的限制,导致以电流下降为特征的扩散尾巴然后,电极的电位扫描被逆转,并以相反的方向扫描,直到达到初始电位。对于化学可逆的电子转移过程,。通过改变扫描电位的速率(ν,扫描速率)和监测电流响应的差异,可以获得有价值的动力学参数。
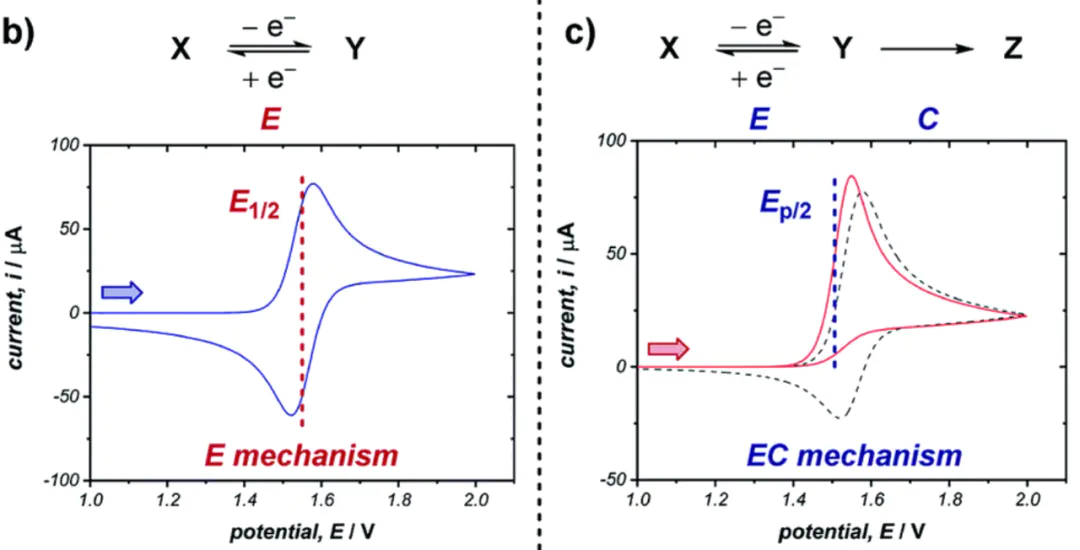
2ECV对于,氧化还原对的浓度与电极电位有关:
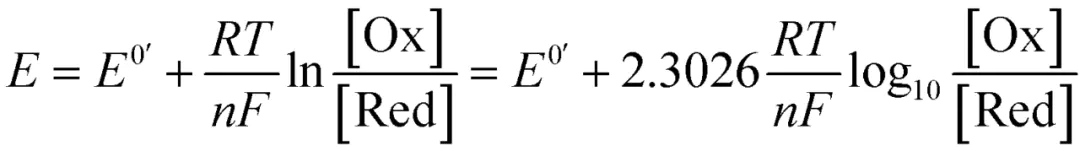
E为形式(热力学)还原势,为气体常数,为温度,为氧化还原过程中转移的电子数,为法拉第常数,和[Red]分别为氧化态和还原态的界面浓度(假设所有态的活度系数为1)。
在电位扫描中,电极界面上的氧化还原活性物质浓度会随时间变化,通过电子转移达到能斯特方程定义的平衡,导致电流响应变化对于电化学可逆过程,1/2,近似等于0′60/n mV若峰分离显著大于此值,则表明电子转移动力学缓慢,适合快速循环伏安法(CV)扫描如图,随后的化学步骤(机制中的C)会导致正向扫描时电生成物的损失,使反向扫描时峰值电流降低。
,因为它可能在期望转化前就分解。通过测量伏安形状随扫描速率变化,还可获得化学步骤动力学的定量数据,高扫描速率下伏安图更具可逆性。
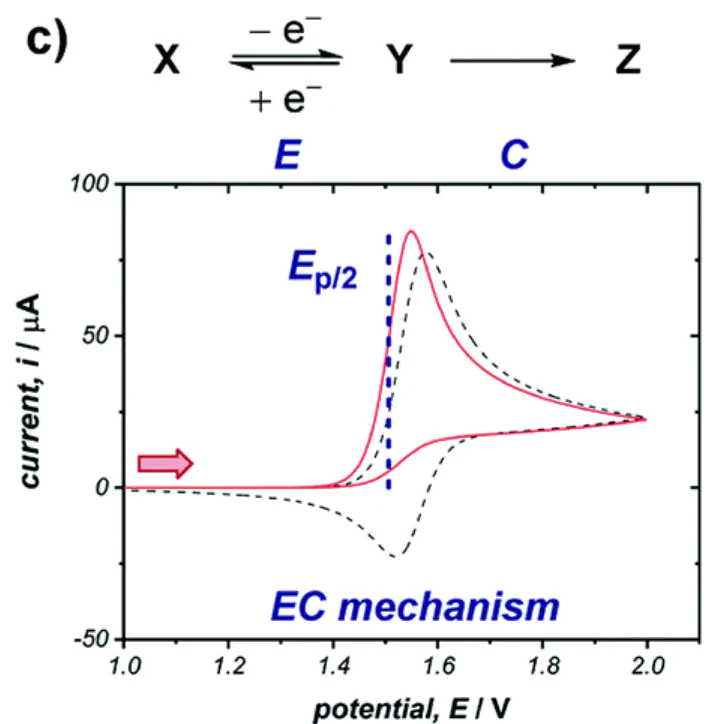
3EC判断电化学反应的可逆性是循环伏安法最基本也是最重要的作用之一。
,其曲线具有明显的特征:pc59/n mVpc1例如,在体系中,Fe³⁺与Fe²⁺之间的电子转移反应是典型的可逆反应,c。
,由于电子转移速率较慢,反应无法及时达到平衡,pc1通过对比不同条件下的CV曲线特征,可以直观地判断电化学反应的可逆性程度,为进一步研究反应机理提供重要依据。
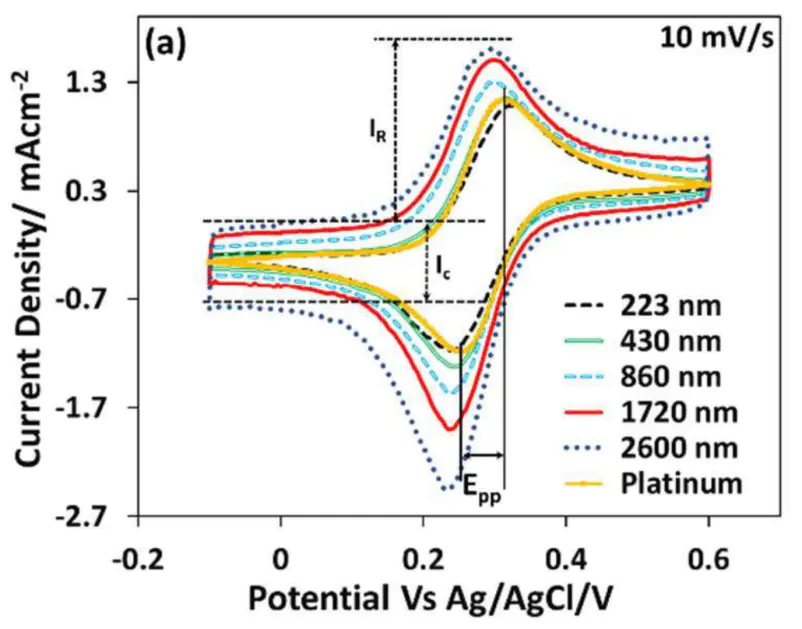
4KFe(CN)/KFe(CN)在溶液中对不同厚度的PEDOT-Tos电极,以及铂
DOI除了判断反应可逆性,循环伏安法还可以用于测定电化学反应的动力学参数,如k⁰等。
5× n^(3/2) × A × D^(1/2) × v^(1/2) × c
对于,峰电流,这是Randles-Sevcik方程的核心内容。通过测量不同扫描速率下的峰电流,并以iₚ对v¹/²作图,得到的直线斜率可以用于计算电活性物质的扩散系数D。
不可逆反应。
分析电极表面的吸附行为
CV对于吸附态的电活性物质,iₚ,这与扩散控制的iₚ ∝ v¹/²形成明显区别。此外,。
等条件,观察CV曲线的变化,可以判断吸附作用的存在与否,并进一步研究吸附等温线、吸附量以及吸附动力学等参数。
CO图:不同单原子催化剂的CO溶出伏安法。:10.1038/s41467-021-23306-6
评估电极材料的电化学性能
。
明显对称的氧化还原峰,且循环稳定性好如图,通过双电层电容法测定10ECSA越高,催化剂的有效活性位点越多,OER性能越好。
该方法通过在非法拉第范围内以不同扫描速率收集样品电流,绘制1.10 V处的电流与扫描速率图,其斜率即为CECSA。
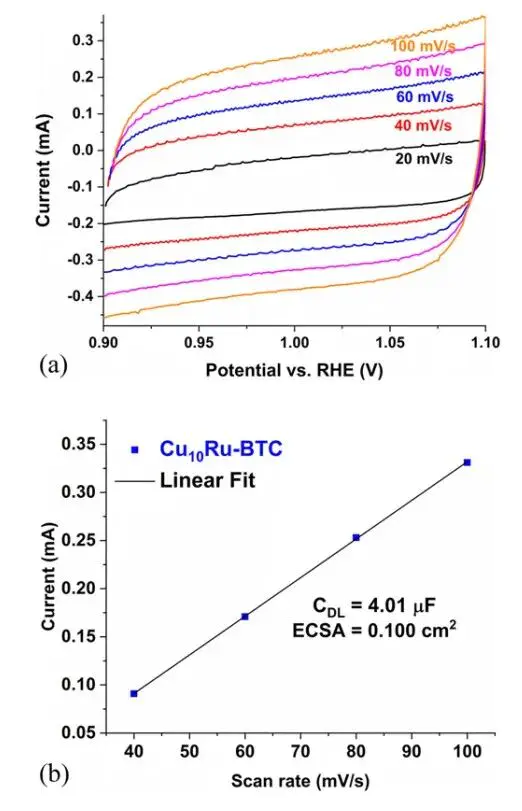
610的CV图和C图。在能源存储领域,循环伏安法()是电池和超级电容器研发的关键表征手段。
CV需通过CV法测定工作电压窗口、比电容、速率性能和循环稳定性如图在低负载下测试。其在不同pH值电解液中的最佳比电容分别为:酸性639 F g、中性-1366 F g。当扫描速率从-1200 mV s时,图:CCDH-800在三电极体系中不同PH条件下的循环伏安曲线。DOI:10.1002/anie.202519704
电催化领域
ORR)、析氢反应(HER)、析氧反应(OER)以及CO₂还原反应如图在条件下测量了Cu CF和Cu Ref的循环伏安曲线(CV)。Cu Ref的阳极电流峰和阴极电流峰是由Cu的氧化还原反应引起的。
91000次循环也没有观察到Cu CF的氧化峰,足以证明。
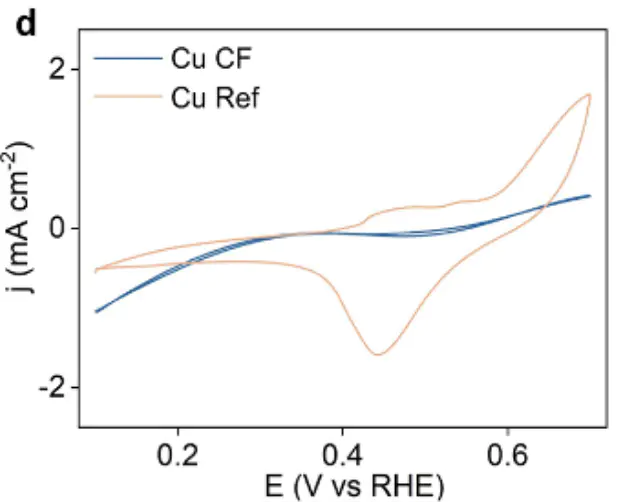
8Cu CFDOI图:在0.1 M KOH条件下1000次循环Cu CF的CV曲线。DOI:10.1021/jacs.3c02399