
当山东枣庄67岁的田新菊女士自然受孕生下女儿,当山东济南一位60岁的母亲平安诞下男孩,当广东佛山56岁的妈妈通过剖宫产迎来一对双胞胎儿子……
这些曾经被视为生命奇迹的新闻,正在频繁地出现在我们的视野中。
这并非偶然,随着社会发展和生育观念变化,高龄生育已从个例演变为一种趋势。
数据显示,我国35岁及以上高龄产妇比例已突破18.7%,在一线城市甚至超过25%。
辅助生殖技术的进步,让许多女性在40岁、50岁甚至更年长时,依然拥有了成为母亲的可能。
然而,在医学庆祝这些奇迹的同时,科学家们却在试验室里观察到了另一幅更为复杂、也更为深远的图景。
顶级学术期刊上的最新研究揭示了一个超越个体健康,关乎家族未来的生物学真相:高龄母亲的影响,可能远不止于怀孕和生产时的风险。

到底是怎么回事呢?今天圈姐就透过这些轰轰烈烈的社会新闻背后,深入那份顶刊研究,看看高龄生育这份礼物的包装之下,究竟藏着怎样一份关乎三代人健康的说明书。
01问题的起点:妈妈的线粒体我们都知道,我们每一个的线粒体全部遗传自我们的母亲,妈妈们的卵子就像一个孩子的启动包。
随着妈妈年龄增长,卵子这个启动包在存放过程中会产生氧化损伤,这种损伤会损害线粒体功能,细胞为了隔离被损伤的脂肪就把它们打包成更多的小油滴储存起来。
所以,很多研究观察到高龄卵母细胞内的脂滴。
研究发现高龄妈妈的卵子和早期胚胎里,都堆积了过多的脂滴,科学家还不完全清楚,为什么这种高脂状态会一直持续到胚胎早期。
在怀孕初期,胚胎着床前,胚胎全靠卵子自带的启动包过日子,只有成功着床、胎盘开始工作后,妈妈才能通过脐带持续供给新鲜的、无氧化的营养。
如果这个供应链转换顺利,胚胎就有充足的资源来清理氧化损伤;
但如果供给不足或不及时,那些最需要启动包的发育中器官,比如大脑,就可能因为过度氧化而受到损伤。
研究者想探讨的是,胚胎期这些氧化迹象和高脂状态,到胎儿中后期,甚至孩子长大成人后还会存在吗?
更可怕的是,如果高龄妈妈生的是女儿,那么女儿卵子里的启动包状态会不会受到影响?孙女会不会受到影响?
研究者认为,鉴于线粒体只能母系遗传,且脂质代谢异常在卵子中很明显,这种通过女性血脉的跨代传递非常有可能。
本文就是要研究以上这些问题。
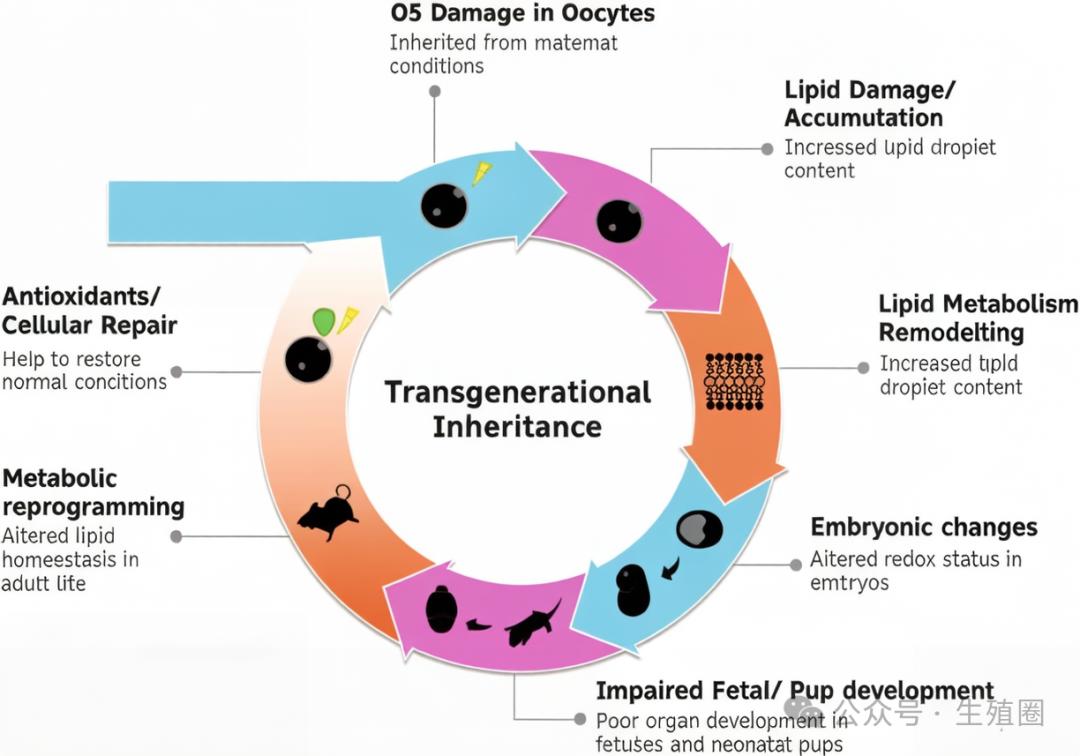 02第一代受到哪些影响
02第一代受到哪些影响不管是人类还是小鼠,高龄母亲的卵子里,都会发现脂滴数量和体积变多,所以本文的研究都是基于小鼠试验。
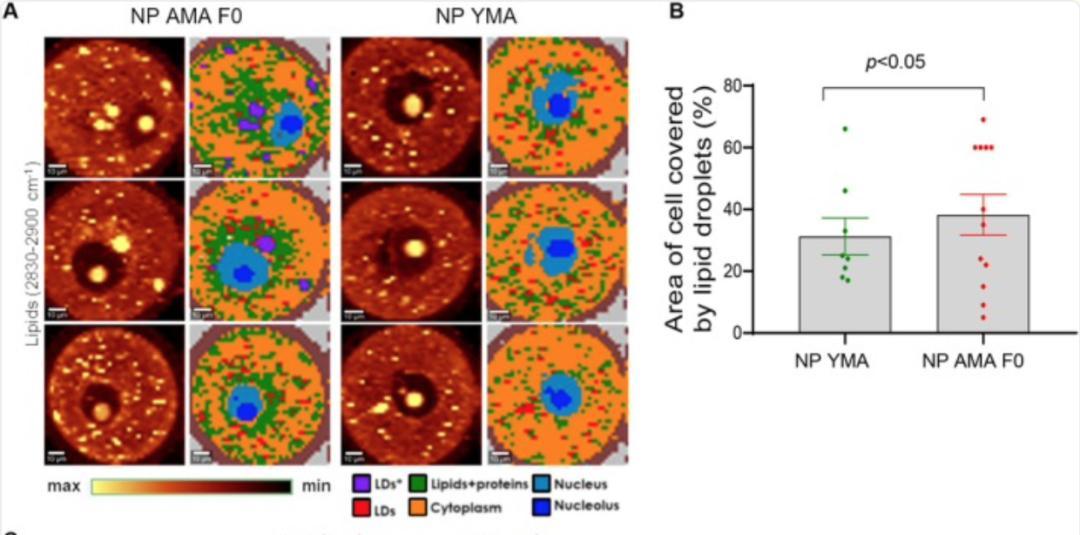
这些小脂滴在卵子里喜欢挤在细胞核和细胞膜附近,这就好比在重要设备边上堆满了易燃易爆物,一旦出事,对胚胎的早期发育很危险。
卵子里油多,由它发育成的早期胚胎里的油也多,这说明高油状态从生命的最初阶段就继承了。
那么这对胎儿有哪些影响呢?
研究者发现,在高龄妈妈所生的胎儿(自然怀孕F1)肝脏里,两种关键的抗氧化剂水平都异常升高,这说明,肝脏在加班加点处理氧化问题。
高龄鼠妈妈的卵子受精后,研究者也移植到了年轻鼠妈妈的子宫里发育(试管婴儿),这样可以区分出问题是来自卵子还是子宫。
即使胚胎在年轻子宫里长大,这个现象依然存在,这说明问题的根源是来自高龄的卵子,而不是子宫。
在年轻子宫里长大的高龄卵子胎儿,大脑重量更轻,这说明,子宫很好,但卵子质量不佳,也会直接影响大脑这个高消耗器官的发育。
自然怀孕高龄鼠妈妈,其胎儿的胎盘变大,但胎儿自己反而更小,胎儿/胎盘重量比下降。
胎盘是营养转运站,胎盘变大,意思是身体努力多给胎儿输送营养,但效率太低(胎儿/胎盘比低),说明这个转运站功能不好,胎儿还是营养不良,生长受限。
但是试管婴儿组把高龄卵子移植进年轻子宫里,胎盘和胎儿大小就正常了。
这说明高龄的子宫是导致胎盘效率低下的主因,而高龄卵子主要影响胎儿自身的代谢和发育程序。
也就是说,高龄生育的影响是卵子和子宫双重作用,卵子老化会给后代设定一个更容易产生氧化应激的代谢程序,并可能直接影响大脑等器官的发育。
子宫老化则可能导致胎盘功能差,让胎儿在宫内就营养不足,生长受限。
这些第一代小鼠成年后新陈代谢系统已被重新编程,变得不那么健康,具体表现为血脂异常、胰岛素水平紊乱、肝脏的脂肪代谢失调。
这就像身体处理能量的软件出现了bug,虽然机器依然能跑,但耗能高、损耗大、容易出故障。
03跨代影响还不完的健康债研究者追踪到了曾孙辈(F3代),发现了更深远的影响。
从体重来看,第一代(F1)幼鼠从出生后养育明显比年轻小鼠子代更胖,但成年后体重正常了。
到了第二代、第三代(F2、F3),体重看起来没什么大问题了。
但是第三代(F3)幼鼠存活率显著降低了,这意味着表面看起来正常的孙辈,可能背负着隐形的健康债务,导致他们的生命力更脆弱。
从代谢方面来看,成年后的后代(F1、F2、F3),无论是雌雄,血液和肝脏中的多种代谢物水平都发生了改变。
这表明他们的新陈代谢系统被重新编程了,处理脂肪和能量的方式变得低效或不正常。
这种代谢异常的模式在雌性和雄性后代中表现不同,这说明影响存在性别差异。
最关键的来了,研究人员检查了第三代(F3)年轻雌鼠的卵子,它们的妈妈(F2)和外婆(F1)都是在正常年龄生育的,只有它们的曾外婆(F0)是高龄生育。
这些年轻F3代雌鼠的卵子内部的油脂成分谱和代谢特征,竟然和它们高龄生育的曾外婆(F0)的卵子高度相似,而与正常年轻鼠的卵子截然不同。
这证明了,高龄生育带来的代谢记忆,可以通过卵子本身,跨越三代进行传递。
即使后代妈妈在最佳年龄生育,这个烙印仍存在于她的卵子中,并可能继续影响下一代。
04为什么高龄生育影响这么大?为什么只是一个简单的高龄生育,影响就足足跨越了三代人呢?研究者深入到了分子层面,试图解释这其中的机制。
高龄来源的卵子,其内部的线粒体处于应激状态,相关的工作部件(如细胞色素C)和智慧生产脂肪的部件(SREBP-1)都变多了.
这说明细胞在努力产生更多能量来对抗压力,并可能因此合成了更多脂肪。
卵子里有一套维甲酸系统(与维生素A相关),它对于能量生产和抗氧化都至关重要。
在年轻卵子中,这套系统的各个成分运作灵活、平衡。
在高龄卵子(F0)及其第三代(F3)卵子中,这个系统变得紧绷和失调,各成分间关联性过强,失去了灵活性。
这就像一套长期处于一级战备状态的消防系统,资源被透支,难以应对新的危机。
这其中,抗氧化形式的维生素A(如视黄醇)被不可逆地消耗,转化为其他形式,这正是严重的氧化应激标志。
所以从机制上来看,我们高龄女性在备孕和孕期服用抗氧化剂的思路是对的,但是这其中到底有多少能派上用场,到底什么形式的补充吸收才更好,还是个大大的问号。
简单来说,这项研究提示,高龄生育的影响,可能不仅仅是一代人的事,它像一道涟漪,通过改变卵子最基础的能量和代谢状态,将健康风险传递给未来的子孙。
05我们如何应对这个挑战面对枣庄奇迹背后日益普遍的高龄生育趋势,我们是否有能力改写或减轻呢?答案是谨慎而分层次的。
首先,临床上已有成熟的优化内膜方案,通过精准的激素与代谢管理,在医学上已经可以尽力为胎儿营造更好的宫内环境。
其次,这警示我们,辅助生殖技术不能只看卵子和胚胎的外形是否好看,更需要开发新技术去检测这些内在的、细问的分子锈迹和代谢异常。
未来的生育力评估和干预,需要深入到细胞代谢层面,才有可能打破这种不良的跨代循环。
前沿研究正探索更根本的方法,比如为卵子补充年轻的线粒体,或使用特定抗氧化剂试图修复细胞损伤,但这些方法大多仍在实验室阶段,距离安全可靠的临床应用尚有距离。
因此,目前最现实、最有效的策略,或许并非逆转,而是预见与守护。
这意味着,当一位女性在较高年龄成为母亲,她与医疗系统可以建立一份超越婴儿期的、长期的健康监护计划。
从孕期密切监测胎盘功能与胎儿生长,到孩子成长过程中关注其代谢指标,如血糖、血脂,并通过科学的营养与运动进行早期预防。
这种基于科学认知的、贯穿生命早期的主动健康管理,是切断不良连锁反应最有力的现实工具。
当然,如果有可能,在最佳生育年龄实现生育,是最稳妥的策略,注意啊,这并非圈姐的催生,而是基于这篇研究产生的感叹。

这篇研究揭示的,并非为了给高龄生育的选择蒙上阴影,而是为了点亮一盏更审慎、更长远的路灯。
它告诉我们,新生命的馈赠,不仅在于诞生那一刻的喜悦,更在于一份可能延续数代人的健康嘱托。
它让我们意识到,现代医学的职责已从保证出生,前移至优化生命起点,并延伸到对孩子长达数十年代谢健康的早期守护。
因此,标题中健康债的隐喻,其意义不在于催生焦虑,而在于催生认知与行动。
它意味着,每一位在较晚年龄迎接新生命的母亲,都值得获得从孕前营养、孕期监测到子代长期健康指导的全周期支持。
在充分了解风险的基础上,用科学与理性的规划,尽可能为孩子的健康未来储备更充足的资本——这或许是我们面对生命规律时,最负责任、也最温暖的回应。
全文完!现在流量为王的年代,围观也是一份力量,转发就是一份担当,希望动动您发财的小手,给我点个赞,如果您能转发到微信群或朋友圈,就会让更多孕育困难的小家庭受益,谢谢您!
郑重声明
本账号发表的内容仅作为科普分享,不对所引用文献的准确性和完整性作出任何承诺和保证,亦不承担因该内容已过时、所引用资料可能的不准确或不完整等情况引起的任何责任,请相关各方在采用或者以此作为决策依据时另行核查。本账号不做任何形式的营销推广,在采取任何预防或治疗措施前,请与你的医疗保健提供者沟通。
不传小道消息和谣言
不做只为转发量而存在的公众号
永远在意真实数据和文献论证
抱娃路上,我愿意陪你一起走过最无助的岁月
——THE END——
参考文献
Intergenerational Transmission of Metabolic Changes in Oocytes From Aged Mice. Aging Cell. 2026 Mar;25(3):e70426. doi: 10.1111/acel.70426.