2026年3月25日发表在 Nature Medicine的一篇I期临床试验论文,标题为“In vivo generation of anti-BCMA CAR-T cells in relapsed or refractory multiple myeloma: a phase 1 study”。通讯作者为华中科技大学同济医院血液科的李春瑞教授。研究团队来自同济医院、深圳普瑞基因生物制药和比利时EsoBiotec公司(后被阿斯利康收购)。这款试验性疗法虽能对部分多发性骨髓瘤患者的病情起到抑制作用,但其安全性或并未优于实验室制备的细胞疗法。

该研究公布了5名接受ESO-T01治疗的多发性骨髓瘤新患者的临床结果,其中4名患者对治疗产生应答,且在治疗两个月后均达到微小残留病阴性,这意味着患者血液中已检测不到癌细胞,是预示长期治疗效果的积极信号。
值得一提的是,此前武汉协和医院研究人员已在《柳叶刀》发表过4名接受该试验性疗法患者的相关数据。ESO-T01是最早进入人体临床试验的体内CAR-T疗法,在该疗法于中国开展的研究者发起试验中公布首例患者早期治疗结果后,阿斯利康随即宣布收购其研发方比利时初创企业EsoBiotec。
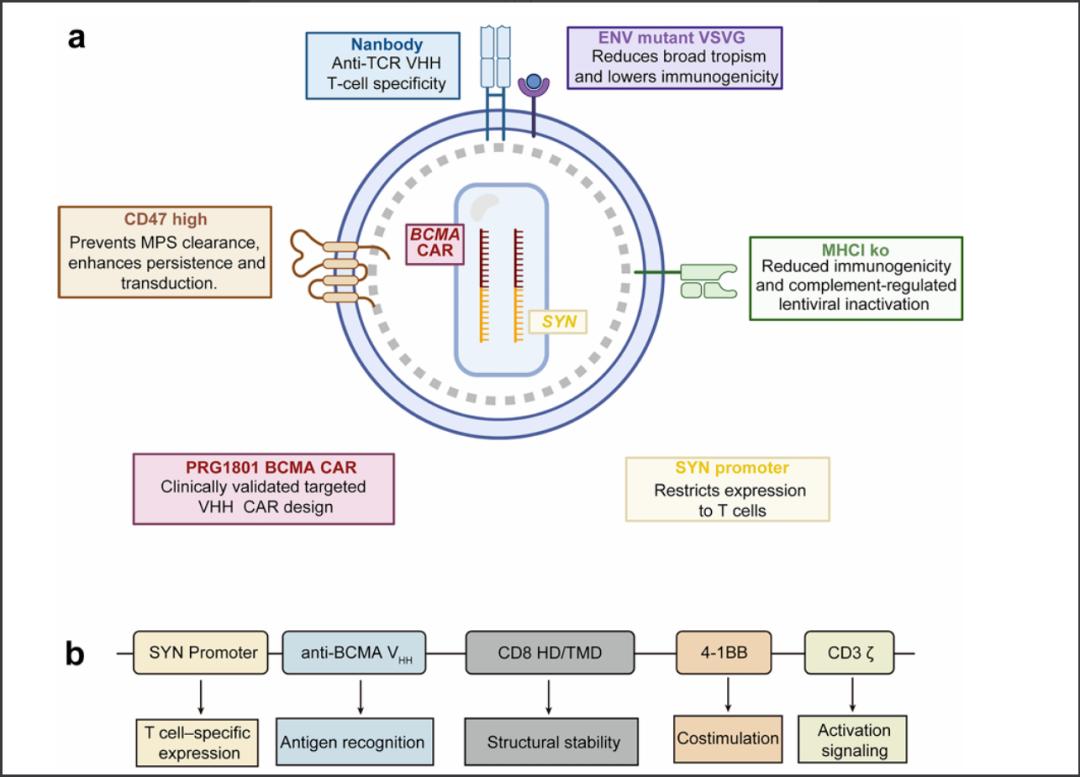
试验纳入了5名经过大量前期治疗的复发或难治性多发性骨髓瘤男性患者,中位年龄52岁,既往接受过中位3线治疗。在极短的中位8小时37分钟入组至输注时间内,所有患者接受了单次0.2×10^9转导单位的低剂量给药。
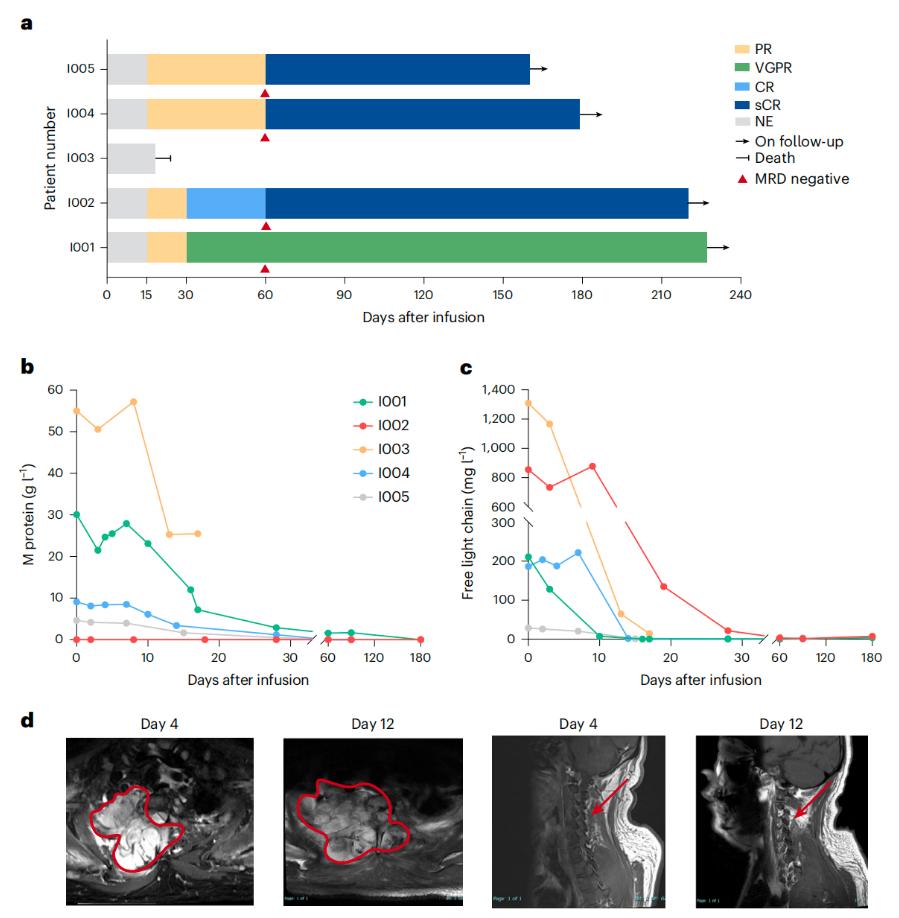
安全性评估显示,虽然所有患者出现了3级或以上不良事件,但未出现剂量限制性毒性反应。80%的患者发生细胞因子释放综合征(3例3级,1例2级),均通过标准治疗得到控制。最常见毒性为短暂性血细胞减少和可逆性肝酶升高。研究期间有1名患者因髓外病变导致脊髓压迫死亡,这与疾病进展密切相关。
疗效方面,5名患者中4名达到客观缓解(ORR 80%),其中3名实现严格完全缓解(sCR 60%)。所有可评估缓解者在治疗第60天时微小残留病灶均为阴性(MRD阴性率100%),显示出强大的肿瘤清除能力。MRD阴性是多发性骨髓瘤治疗中的重要里程碑,与患者的长期无进展生存和总生存期改善密切相关。ESO-T01实现100%的MRD阴性率,即使在低剂量下也展现出强大的疾病清除能力,为后续更高剂量的探索提供了有力支持。
药代动力学分析表明,输注后4-8天即可在外周血中检测到CAR-T细胞,且能浸润至骨髓、肿瘤组织甚至脑脊液等传统疗法难以触及的部位,对伴有髓外病变的难治患者尤为重要。
传统CAR-T面临制造复杂性带来的供应链脆弱性、高昂成本导致的支付压力、等待期间病情恶化风险等多维挑战。ESO-T01所代表的体内CAR-T技术,正尝试从源头解决这些问题:简化治疗流程、降低制造成本、提高治疗可及性。
目前,ESO-T01的后续研发走向尚不明确。阿斯利康发言人向媒体表示,公司正基于现有研究结果,进一步开展体内CAR-T疗法的研发工作,但并未回应ESO-T01是否会继续推进开发。
文献:An N, Wang D, Zhang P, Zhang J, Parone P, Hu J, Bao Y, Xu L, Ruan H, Wan Y, Wen X, Gao Y, Li C. In vivo generation of anti-BCMA CAR-T cells in relapsed or refractory multiple myeloma: a phase 1 study. Nat Med. 2026 Mar 25. doi: 10.1038/s41591-026-04244-6
— END —

新干细胞者说
- 科普 情怀 责任 -