前言
“慢加急性肝衰竭(ACLF)主题月评”是中国慢(加急)性肝衰竭联盟受《国际肝病》编辑部邀请,制作的ACLF相关学术月评专栏。本专栏每月以ACLF某一特定领域为主题展开,旨在普及ACLF的概念及意义、帮助读者快速了解有关领域的进展。希望本专栏对无论是需要了解相关领域热点的肝病专家及研究人员,或是需要实用知识、活跃于临床一线的医务工作者,均能有所裨益。
本期月评介绍了由欧州、拉丁美州、印度及中国四大地区的多中心队列建立的肝硬化基础上的ACLF新诊断标准——ATANGO-OF评分,简化了较复杂的诊断过程采用单个器官衰竭即可诊断ACLF。此外,该诊断标准统一了东西方在肝硬化ACLF诊断上存在的分歧。最后,对本月(2026.1.23-2026.2.22)PubMed上更新的ACLF相关重要文献进行简评。

关于作者:
中国慢(加急)性肝衰竭联盟(Chinese Acute-on-chronic liver failure Consortium,Ch-CLIF-C)是由上海交通大学附属仁济医院消化内科李海教授牵头,由全国17家三甲医院感染科/肝病中心共同参与成立的肝病科研合作团队,致力于探索慢加急性肝衰竭(ACLF)的发病机制、制定基于高循证等级的乙肝高流行区ACLF诊断标准。目前团队开展了全球已报道入组数最多的ACLF前瞻性多中心队列研究“CATCH LIFE”(Chinese AcuTe-on-CHronic LIver FailurE),包含2个大型队列(入组2600例的探索队列与入组1370例的验证队列)。
本期责任编辑

李海教授
上海交通大学医学院附属仁济医院消化内科主任医师,卫生部消化重点实验室副主任,目前担任上海医学会临床流行病学与循证医学分会主任委员。研究方向为慢加急性肝衰竭。牵头组织全国14家三甲医院肝病中心开展慢加急性肝衰竭前瞻性研究(CATCH-LIFE Study),该研究入组23970余例患者,成为全球入组数量最多之一的慢加急肝衰竭领域临床研究。该多中心临床研究目前已发表30余篇原创性论著。
本期责任副编辑

边曰响
上海交通大学医学院博士在读研究生,师从上海交通大学医学院附属仁济医院李海教授,目前研究方向为慢加急肝衰竭的机制和治疗研究。论文摘要曾入选EASL年会壁报展示;以第一/共一作者身份在SCI期刊发表2篇学术论文。
主题述评慢加急性肝衰竭(ACLF)是一类以器官衰竭、短期预后不佳为特征的危重症肝病。2026年2月17日在Journal of Hepatology线上发表的根据全球4个大型肝硬化队列制定的A-TANGO诊断标准,为统一全球肝硬化ACLF诊断迈出重要一步。A-TANGO诊断属于CANONIC 2.0版本,主要解决仅根据以酒肝、丙肝为主要病因的欧洲肝硬化ACLF CANONIC 1.0版本(即CLIF-C OF评分),适合于西方型(酒精性)肝硬化ACLF,而不完全适用于东方型(HBV)诊断的局限。为了克服单一地区的不足,A-TANGO整合了欧洲CANONIC和PREDICT、拉丁美洲ACLARA、印度Ambi-spective和中国CATCH-LIFE四大队列研究(欧洲及拉丁美洲建模,中国及印度队列验证),获得了一个适合于东、西方不同病因的通用型针对肝硬化ACLF的诊断标准,朝ACLF统一标准迈进了关键一步(DOI:https://doi.org/10.1016/j.jhep.2026.02.017)。本项目由英国Rajiv Jalan教授牵头完成,印度队列Ajay Duseja教授以及中国CATCH-LIFE队列李海和陈金军教授为本文共同senior author。
该诊断标准具备重要的中国患者权重(CATCH-LIFE队列病例贡献达到30%),因此中国CATCH-LIFE小组根据中国患者疾病特征将该诊断标准略做修改,形成更容易在临床应用的A-TANGO单器官衰竭标准(见下)。
01
四大队列的病因构成和两个标准诊断的ACLF权重占比
欧洲CANONIC、PREDICT队列2622例患者(酒精性肝病66%,丙型病毒性肝炎21%),A-TANGO诊断ACLF的占比为32%(CLIF-C OF 19%)。
拉丁美洲ACLARA队列1274例患者(酒精性肝病 71%,代谢相关脂肪性肝病14%),A-TANGO诊断ACLF的占为42%(CLIF-C OF 31%)。
印度Ambi-spective队列2055例患者(酒精性肝病 70%,病毒性肝炎12%),A-TANGO诊断ACLF的占比83%(CLIF-C OF 77%)。
中国CATCH-LIFE队列2568例患者(乙型病毒性肝炎66%,酒精性肝病21%),A-TANGO诊断ACLF的占比为31%(CLIF-C OF 16%)。
02
根据中国人群疾病特征修订的A-TANGO标准
以器官衰竭28天死亡率≥15%作为诊断ACLF的最低标准(与CANONIC 1.0版本一致)。在A-TANGO研究中参与的中国CATCH-LIFE人群中,单个神经和循环的衰竭即可使28天死亡率达到15%。因此,在修订的A-TANGO标准中,神经和循环系统采用“单器官衰竭”替代原标准中“单器官加另一器官损害”的诊断。
表. A-TANGO 单器官衰竭诊断标准(经CATCH-LIFE修订)

03
A-TANGO诊断标准在中国CATCH-LIFE队列中的实际表现和应用情况(与CANONIC诊断标准进行比较)
A-TANGO诊断的肝硬化ACLF(31%,n=807)较CANONIC 1.0版(CLIF-C OF诊断)(16%,n=409)多398个患者(图1)。与后者相比,在识别1级ACLF中明显增加了307个患者,从而纠正了CANONIC 1.0版本(CLIF-C OF)对1级ACLF存在明显漏诊的缺陷。这显示CANONIC 2.0版本(A-TANGO)在诊断东、西方肝硬化ACLF方面取得了更好的平衡(图2)。
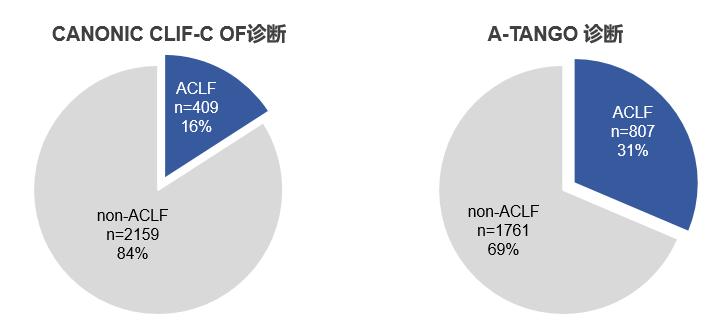
图1. CATCH-LIFE队列在CLIF-C OF与和A-TANGO OF两种评分下诊断为ACLF的人数及占比
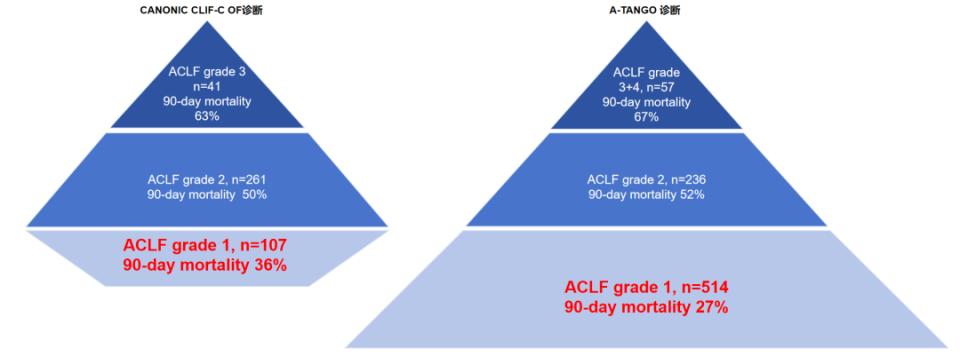
图2. CATCH-LIFE队列中,采用CLIF-C OF与A-TANGO OF评分诊断的ACLF,不同级别的患者人数及占比
04
小结
因中国队列参与了上述诊断标准的制定,因此可以根据中国患者的实际情况对上述标准做适当修订,以符合中国人群疾病特征。修改后的A-TANGO标准通过单一器官衰竭即可诊断肝硬化ACLF,方便临床使用,同时也修正了欧洲原有的CLIF-C OF漏诊1级ACLF的缺点。
综上,CANONIC 2.0版的A-TANGO研究综合了全球四大区域的肝硬化患者,所制定的诊断标准适合于全球各地区的肝硬化ACLF患者,为制定全球统一的ACLF标准迈出了重要一步。后续需解决的是肝硬化与非肝硬化ACLF共用上述多器官衰竭诊断标准还是需采用肝脏单器官衰竭诊断标准,是该领域为制定全球统一诊断标准需解决的下一重要问题。
近一月ACLF研究优秀论文简评2026.1.23-2026.2.22在PubMed上在线发表ACLF相关文献共26篇,涉及疾病预测预后、治疗、诊断与发病机制,具体分布见下图。

01
Garg P, Verma N, et al. Proteomics-guided Biomarker Discovery, Validation, and Pathway Perturbation in Infection-related Acute Decompensation of Cirrhosis. Clin Gastroenterol Hepatol. 2026 Feb;24(2):407-420.e39. doi: 10.1016/j.cgh.2025.01.005. Epub 2025 Feb 7. PMID: 39924007. IF=12.2
简述:本研究旨在通过蛋白组学筛选肝硬化急性失代偿(AD)患者的感染早期诊断及感染类型分型的生物标记物。研究共纳入391例急性失代偿患者,分为建模队列与验证队列:建模队列采用液相色谱-串联质谱(LC-MS/MS)进行生物标记物初筛,验证队列采用ELISA对候选标记物进行验证。结果显示,建模队列共84例患者(54例感染、30例非感染)经血浆蛋白质组差异分析筛选出65种差异表达蛋白。通过机器学习、多因素校正、验证队列1(106例感染、41例非感染)验证,确定4种核心蛋白生物标志物:半乳糖凝集素3结合蛋白(LGALS3BP)、补体蛋白P(CFP)、磷脂转移蛋白(PLTP)、谷胱甘肽过氧化物酶3(GPX3),最终由CLIF-C OF、核心蛋白生物标志物及临床生化指标构建PACIFY模型,在验证队列1中诊断感染的AUC:0.965(95% CI,0.933-0.997),并在验证队列2(108例感染、52例非感染)、外部验证队列3(98例感染、62例非感染)中得到验证,AUC达0.906(95% CI,0.860-0.952)、0.949(95% CI,0.916-0.982)。性激素结合球蛋白(SHBG)、丝氨酸蛋白酶抑制剂4(SERPINA4)可区分真菌与细菌感染;皮肤抗菌肽(DCD)、甘露聚糖结合凝集素相关丝氨酸蛋白酶1(MASP1)下调可提示多重耐药菌感染。最后揭示了感染引起通路的异常,包括补体激活受阻、吞噬作用缺陷、中性粒细胞胞外诱捕网形成障碍,糖酵解及磷酸戊糖途径增强,碳水化合物代谢紊乱以及凝血与纤溶失衡。
简评:本研究通过蛋白组学筛选并验证LGALS3BP、PLTP、CFP、GPX3为AD患者感染的特异性蛋白质标志物,构建PACIFY模型诊断可优化抗菌药物使用决策降低耐药。揭示了免疫功能缺陷、代谢紊乱等通路机制,为开发感染防治新策略提供了理论基础。本研究局限性在于尚未在多中心进行验证,需进一步开展多中心验证。此外,生物标志物的检测方法仍需进一步简化,以提升其临床适用性。
02
Shabbir R, Garrido-Trevino L, O'Leary JG, et al. MELD-Lactate and lactate clearance in critically ill cirrhosis patients with sepsis. Am J Gastroenterol. Published online January 27, 2026. doi:10.14309/ajg.0000000000003934.IF=8.1
简述:本研究旨在评估MELD-Lactate(MELD-LA)评分结合24小时乳酸清除率(LA clearance)对肝硬化合并脓毒症患者30天死亡率的预测效能 。研究纳入了北美大型医疗系统中 3437 名患有脓毒血症且临床数据完整的肝硬化ICU患者,并在包含1,259名患者的亚洲 APASL-ACLF 队列中进行了外部验证 。结果显示,MELD-LA评分是肝硬化合并脓毒症患者30天死亡率的独立预测因素。入院后30天内存活者的24小时乳酸清除率中位数为35.2%,显著高于非存活者的12.0% 。在入院24小时内,乳酸清除率 ≥35% 的患者表现出显著的生存优势,其死亡风险较清除率较低者降低了约 60% 。这一关联在北美队列(OR 0.41, 95% CI 0.31-0.53)与亚洲验证队列(OR 0.42, 95% CI 0.28-0.62)中均保持高度一致。此外,早期的治疗干预(尤其是4小时内使用抗生素)与更高的乳酸清除率和更好的生存率直接相关。
简评:该研究将静态的肝病评分(MELD)与动态的代谢指标(乳酸清除率)相结合,提供了一个简单且可量化的工具来评估重症肝硬化患者对早期复苏治疗的反应 。这填补了传统评分系统在“动态监测治疗效果”方面的短板。
该研究精准地界定了“35%乳酸清除率”这一临床预警线,对于ICU医生判断肝硬化败血症患者是否需要调整治疗方案(如考虑早期肝移植或加强复苏)具有重要的指导意义 。对于24小时内清除率未能达标的患者,该指标可作为预后不良的早期预警信号,提示临床医生需重新评估当前治疗方案的有效性,或考虑采取更高阶的干预措施 。通过跨区域、多中心的外部验证,研究证明了该动态评估模型在不同医疗体系及ACLF人群中的普适性,为完善肝硬化脓毒症的临床管理路径提供了高质量的循证医学证据。
03
Lin T, Tong C, Liebe R, et al. Massive hepatic necrosis-associated acute liver failure. eGastroenterology. 2026;4(1):e100217. doi:10.1136/egastro-2025-100217
简述:本综述系统讲解了大块肝坏死相关的急性肝衰竭(MHN-associated ALF)的病理生理机制及肝祖细胞(LPCs)生物学研究进展。文章首先明确MHN是ALF中最严重的病理损伤,其特征为肝细胞广泛丢失(>60-70%),死亡率显著高于其他病因ALF。且与其他ALF不同,MHN后的肝再生依赖于位于Hering管和的LPCs,这些细胞能否快速增殖并完成功能替代决定了患者临床结局。研究重点探讨了MHN的发病机制,包括HBV相关ALF中体液免疫(抗HBc抗体介导的补体沉积)和AIH中的浆细胞浸润作用;肝细胞死亡方式的多样性(坏死、凋亡等)及其与临床预后的争议关系。总结了LPCs功能启动的关键机制:FOXA2作为先导因子打开染色质结构;HNF4α与C/EBPα共同调控肝细胞转录程序;超增强子(super-enhancer)的重新形成。提示MHN发生后的再生不是简单增殖,而是一场高度程序化的细胞重塑。此外,文章还总结了LPCs增殖的微环境信号网络及 zebrafish模型中胆管细胞转分化为肝细胞的再生途径,指出当前研究瓶颈在于缺乏理想动物模型和动态临床观察,并提出未来需阐明LPCs激活、功能替代及分化的分子机制。
简评:该综述系统阐述了大块肝坏死(MHN)相关急性肝衰竭(ALF)的病理机制,尤其聚焦肝祖细胞(LPCs)在肝再生中的核心作用。首次明确LPCs是MHN后肝再生的关键执行者,提出其实现肝功能代偿的新机制。同时,揭示了B细胞介导的体液免疫在HBV相关MHN中的致病作用,为靶向治疗提供新视角。并指出未来的研究重点:1. 探索LPCs激活的启动机制,特别是炎症微环境中巨噬细胞与LPCs的交互信号;2 建立MHN动物模型以模拟人类疾病进程;3. 研究LPCs向成熟肝细胞分化的谱系追踪及关键转录因子的时空调控网络。
各研究中心PI