
阿尔茨海默病(AD)以认知功能下降、记忆力丧失以及日常生活能力逐渐衰退为特征。尽管在这一领域已经开展了大量研究,阿尔茨海默病的有效治疗手段仍然有限。目前的治疗策略(如乙酰胆碱酯酶抑制剂、谷氨酸受体调节剂)仅能缓解症状,无法抑制疾病进展。
在各类疗法中,基于干细胞的治疗凭借其再生潜能及调控病理过程的能力,展现出良好的临床应用前景。自体血源性干细胞(ABSCs)是从患者自身血液中分离得到的干细胞,已在阿尔茨海默病的临床前研究中显示出治疗效果。
2025年12月,来自韩国延世大学的研究人员及其合作者在《Molecular Neurobiology》期刊上发表了题为《Therapeutic Efficacy of Autologous Blood-Derived Stem Cells with Growth Factors in Moderate to Severe Alzheimer’s Disease: A Clinical Trial》的临床试验结果,评估了ABSCs联合生长因子治疗阿尔茨海默病的安全性与有效性,并探究了经ABSCs治疗后生长因子水平的变化。
研究设计
这项临床研究为一项前瞻性、单中心、随机对照试验(RCT),旨在评估ABSCs联合生长因子治疗中重度阿尔茨海默病患者的疗效、安全性及作用机制。研究采用了简易智能精神状态检查量表(Mini-Mental State Examination, MMSE)、临床痴呆评定量表(Clinical Dementia Rating, CDR)以及阿尔茨海默病评定量表-认知部分(AD Assessment Scale-Cognitive Subscale)评估治疗对认知功能的影响。神经影像学与分子机制为次要结局指标。
所开展的神经影像学检查包括:
淀粉样蛋白PET-CT:用于评估基线及治疗后3个月、6个月时脑内淀粉样斑块沉积情况;
氟代脱氧葡萄糖PET(FDG-PET):用于检测脑葡萄糖代谢水平,进而反映神经元活性与整体脑功能;
磁共振成像(MRI):于基线及随访时完成,用于评估脑结构改变。
患者分组如下图所示,试验组患者静脉输注ABSCs,剂量根据患者体重(通常为1×10⁶~5×10⁶个细胞/kg)及临床耐受性进行调整。生长因子在干细胞输注结束后立即输注。
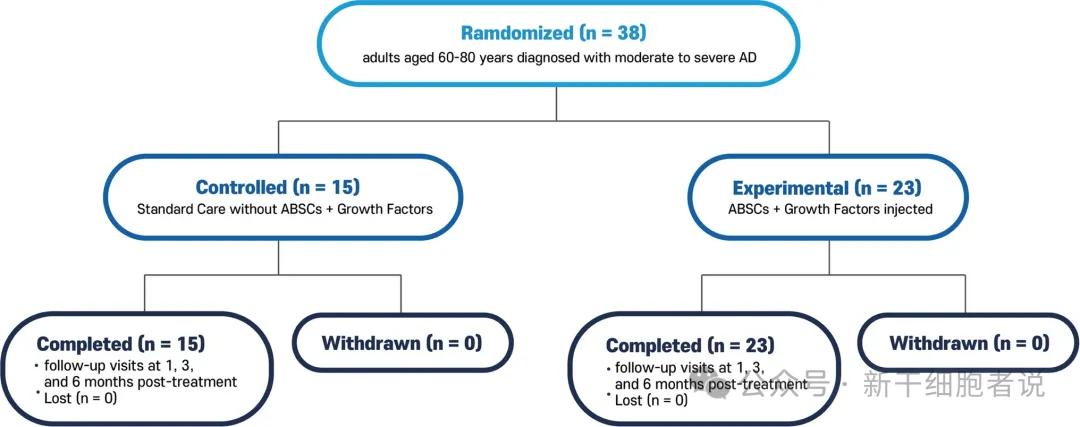
研究设计
结果分析
研究共纳入了38名患者。ABSCs治疗可显著改善认知功能、降低淀粉样斑块负荷,并优化神经影像学结果。这意味着该新型疗法不仅能够缓解症状,还可改善疾病本身的进程。
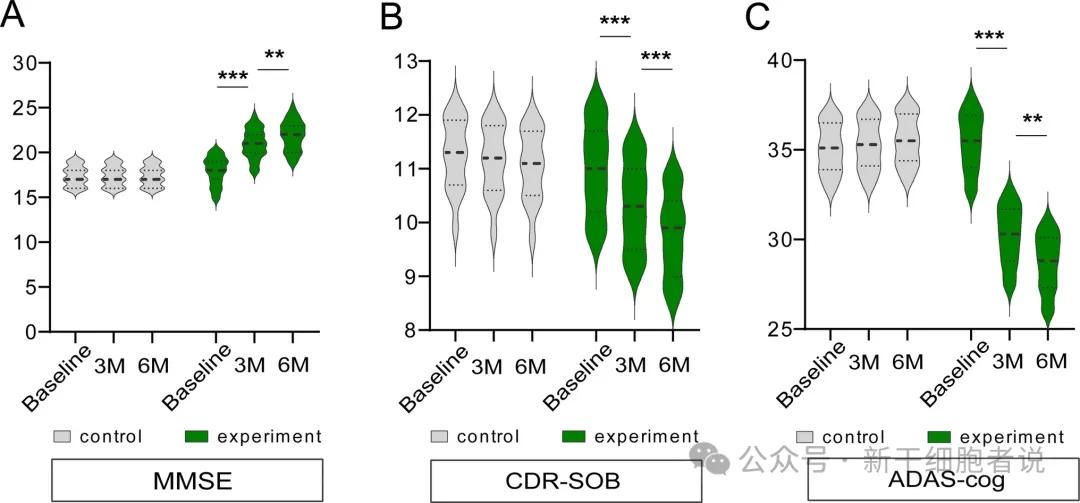
ABSCs治疗后的认知功能特征
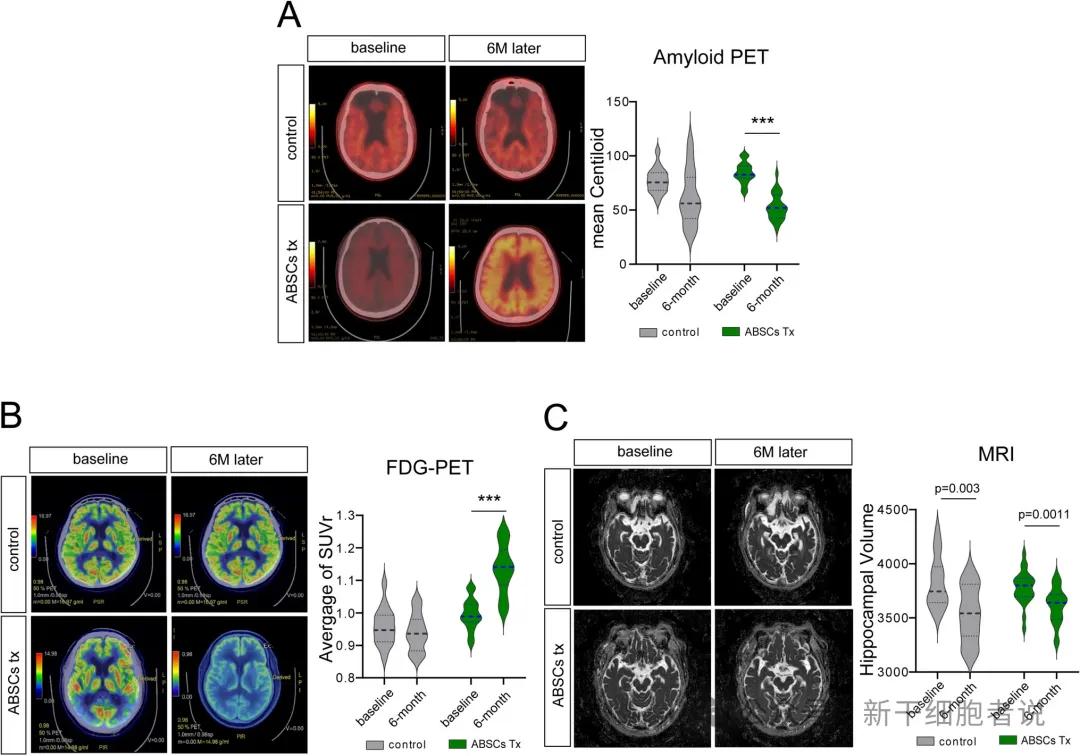
神经影像结果
试验中未出现严重不良事件,治疗安全性良好。自体干细胞治疗还可降低免疫排斥风险,相较于异基因干细胞治疗具有明显的安全性优势。此外,联合应用生长因子以提升干细胞疗效的思路,与现有改善干细胞局限性的相关研究结论一致。
机制研究发现,PI3K/Akt和MAPK/ERK等关键分子通路被正向调控,进而促进神经元存活、发挥神经保护作用并增强神经可塑性。这些结果提示,该疗法可针对神经退行性病变的多重机制发挥作用,以实现全面的治疗获益。
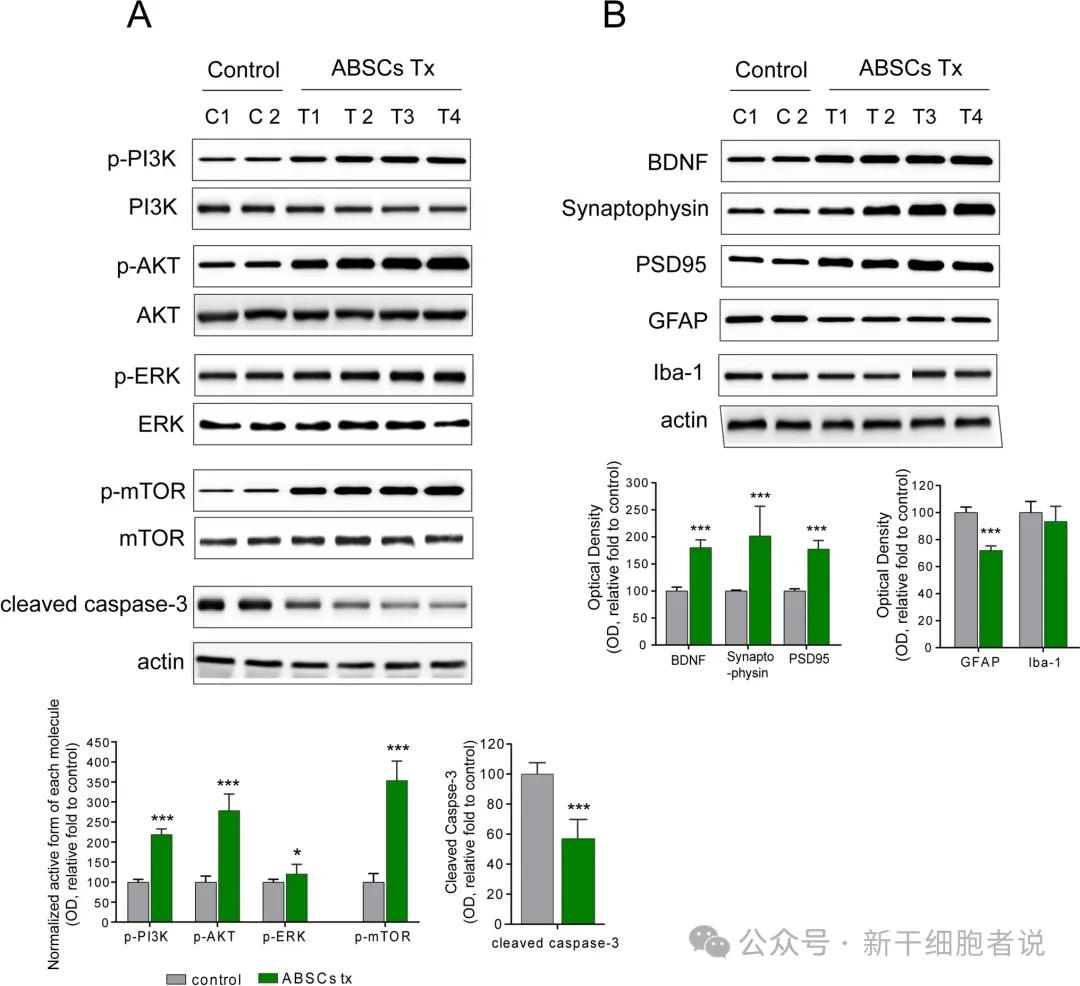
分子通路相关的测量

讨论
这项研究有力地证明了ABSCs联合生长因子对中重度阿尔茨海默病患者具有显著的治疗潜力。虽然该疗法对认知功能改善的具体机制仍不明确,但神经炎症反应很可能发挥关键作用。阿尔茨海默病以小胶质细胞和星形胶质细胞激活为特征,其会触发促炎细胞因子的释放。
这些促炎细胞因子会加剧突触丢失与神经元损伤,进而促进神经退行性变。研究中观察到炎症因子水平显著降低,提示ABSCs可发挥抗炎作用,保护神经元免受进一步损伤。干细胞(尤其是自体血来源的干细胞)的免疫调节特性已有充分文献证实,这或许可以解释神经炎症的减轻以及后续认知功能的改善。
总之,为应对神经退行性疾病复杂的发病机制,ABSCs联合生长因子治疗方案可提供多靶点干预途径,有望成为阿尔茨海默病可持续的治疗策略。
— END —

新干细胞者说
- 科普 情怀 责任 -