编者按
中晚期肝细胞癌(HCC)患者远期预后不佳,即便符合肝切除指征,术后高复发率仍严重影响患者预后,新辅助治疗成为优化中晚期HCC诊疗路径的关键探索方向。GUIDANCE002 作为中国多中心回顾性研究,聚焦经肝动脉化疗栓塞(TACE)联合酪氨酸激酶抑制剂(TKIs)、免疫检查点抑制剂(ICIs)的新辅助三联疗法,为可切除中晚期HCC的治疗提供了重要真实世界证据。广西医科大学附属肿瘤医院钟鉴宏教授深度解读该研究,为临床医生制定个体化治疗方案提供参考,也为HCC新辅助治疗的后续研究与临床应用指明路径,助力中晚期HCC诊疗的精准化与规范化发展。相关研究结果发表于Communications Medicine。

文章发表封图
约70%的HCC患者在确诊时已处于中晚期。根据中国HCC指南,肝切除术适用于部分经过选择的中晚期患者。尽管被指南列为“可切除”的此类患者已显示出生存获益,但术后复发率很高。AASLD指南(2023版本)也扩大这类患者肝切除的适用范围。为了降低复发风险,许多医疗中心在肝切除术前采用新辅助治疗(局部和/或全身治疗),以缩小肿瘤并根除微转移病灶。
EASL指南推荐TACE作为中晚期HCC患者的标准治疗。然而,既往研究发现,新辅助TACE并未降低可切除HCC的术后复发风险。虽然有临床试验证明了新辅助免疫治疗对可切除HCC患者的生存获益,但新辅助治疗本身存在不良事件、肿瘤进展或增加后续肝切除难度的风险。
在LEAP-012和EMERALD-1研究中,TACE联合ICIs和TKIs(或抗VEGF单抗)治疗不可切除HCC,相较于单独TACE,显著提高了OS和无进展生存期。本研究团队近期的大型回顾性研究也支持TACE联合ICIs和TKIs治疗不可切除HCC的疗效。然而,对于可切除的中晚期HCC患者,新辅助TACE联合ICIs和TKIs(即新辅助三联疗法)在改善患者预后和降低术后复发风险方面的疗效仍不明确。
本研究回顾性比较了2019年至2023年间在中国20家医疗中心接受治疗、符合可切除标准并被分配接受新辅助三联疗法(n=205)或直接肝切除术(n=378)的583例患者的总生存期(OS)、无事件生存期(EFS)、不良事件和术后并发症。亚组分析包括106例接受新辅助三联疗法后行肝切除术的患者和99例接受该疗法但未后续手术的患者。
主要研究结果1
基线特征与治疗暴露情况
在筛选的2486例患者中,583例被纳入最终分析,其中378例(64.8%)接受直接肝切除术,205例(35.2%)接受新辅助三联疗法(图1)。在新辅助三联疗法组中,106例(51.7%)后续接受了肝切除术,99例(48.3%)未接受肝切除术,原因包括患者拒绝手术(83例,83.8%)或肿瘤进展至不可切除状态(16例,16.2%)。接受直接肝切除术的患者中位随访时间为30.2个月,接受新辅助三联疗法的患者中位随访时间为26.1个月。

图1. 患者选择与研究流程
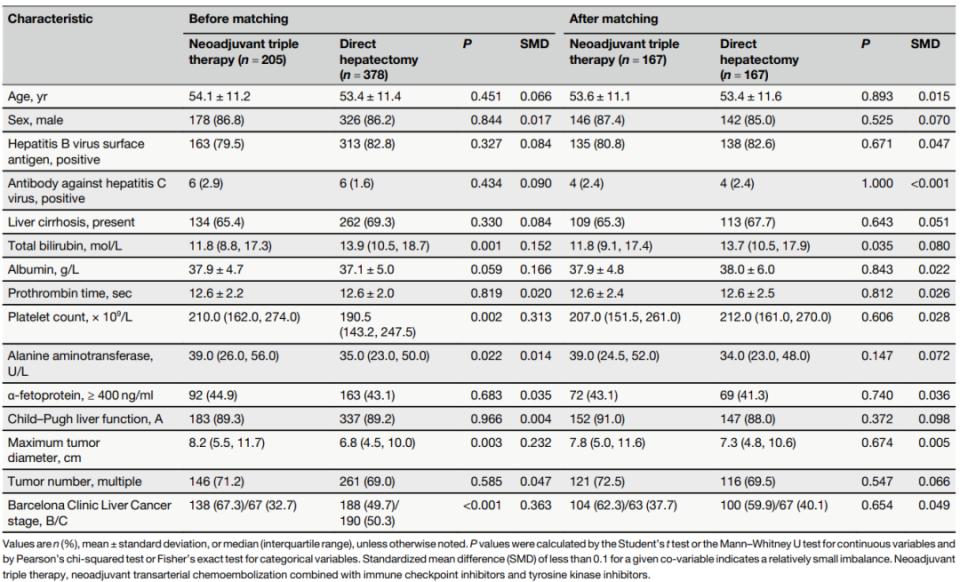
基线特征显示,直接肝切除组患者肿瘤直径更小、BCLC C期占比更高,且总胆红素水平更高、白蛋白和血小板计数更低(表1),存在一定的基线偏倚;经PSM匹配后,两组所有基线特征的SMD均<0.1。
表1. 按初始治疗方式(肝切除 vs. 新辅助三联疗法)分层的患者基线特征(PSM前、后)
2
三联疗法显著提升OS与EFS
整体人群:与直接肝切除组相比,新辅助三联疗法组患者的1年、2年、3年OS率更高(88.7% vs. 78.7%, 65.9% vs. 59.5%, 52.9% vs. 49.3%),OS显著延长(HR=0.70)(图2)。中位EFS也显著延长(19.7个月 vs. 10.9个月)。PSM后结果一致。
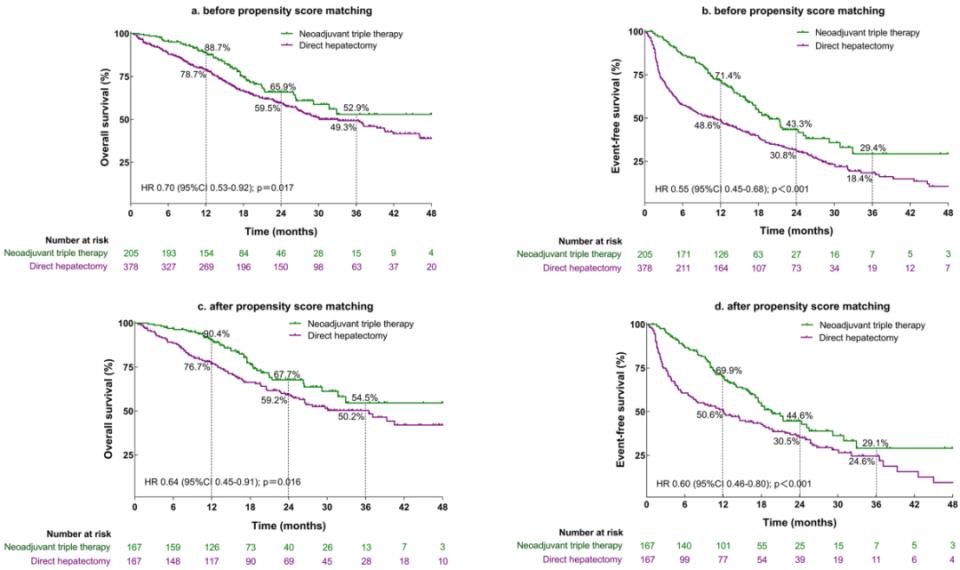
图2. 接受直接肝切除或新辅助三联疗法患者的Kaplan-Meier生存曲线
肝切除亚组:在接受肝切除的患者中,预先进行新辅助三联疗法者的OS(HR=0.45)和EFS(HR=0.49)均显著优于直接肝切除术者(图3)。PSM后结果一致。在BCLC C期患者中,新辅助三联疗法后手术同样显示出显著的OS和EFS获益。
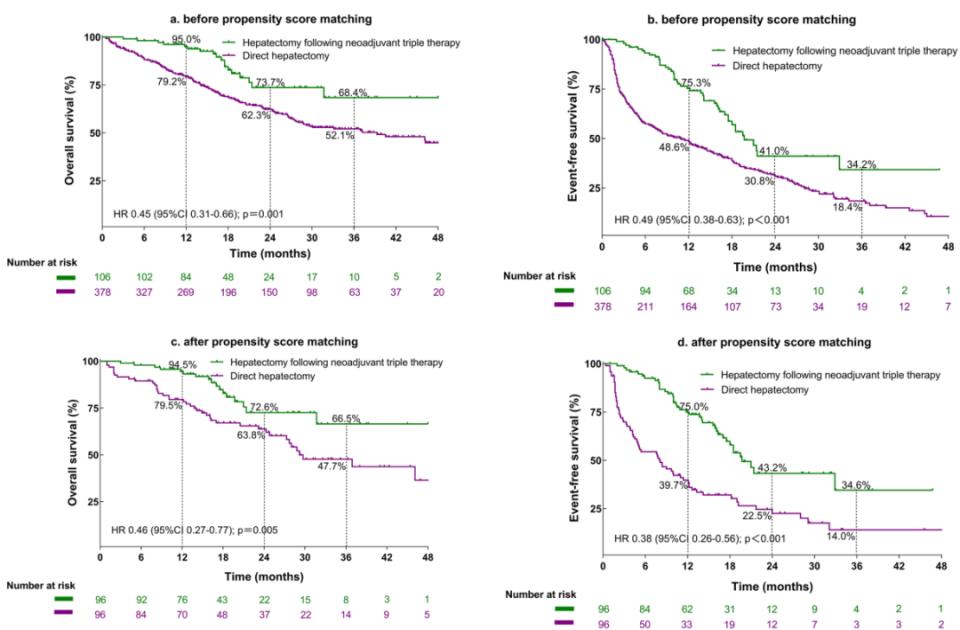
图3. 接受直接肝切除或新辅助三联疗法后行肝切除患者的Kaplan-Meier生存曲线
新辅助治疗亚组:在接受新辅助三联疗法的患者中,后续接受肝切除术者的OS显著优于未手术者(HR=0.40),但两组EFS相似。若排除因肿瘤进展而失去手术机会的16例患者,手术组的OS仍显著更优,但EFS相似(图4)。
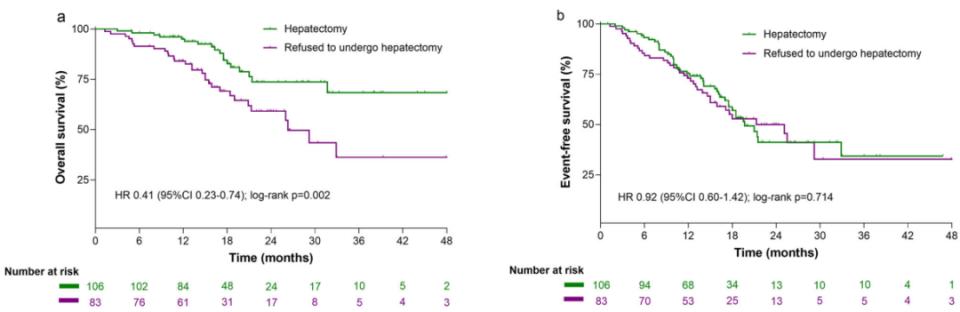
图4. 新辅助三联疗法后接受肝切除与拒绝肝切除患者的Kaplan-Meier生存曲线(排除16例因肿瘤进展失去手术机会的患者)
病理反应:新辅助三联疗法的客观缓解率为67.3%,疾病控制率为84.9%。病理完全缓解率为34.0%,主要病理缓解率为43.4%。基线时为单发肿瘤与更好的治疗反应相关。
不良预后预测因素:多因素分析确定,在总体人群中,直接肝切除术(而非新辅助三联疗法)、无肝硬化、甲胎蛋白≥400 ng/mL和大血管侵犯是OS和EFS不良的独立预测因素。在接受肝切除的患者中,未接受新辅助三联疗法、存在肝硬化、最大肿瘤直径≥10 cm和大血管侵犯是不良生存的独立预测因素。
手术机会丧失的预测因素:16例患者在新辅助三联疗法后因肿瘤进展失去手术机会。多因素逻辑回归确定,甲胎蛋白≥400 ng/mL和大血管侵犯是肿瘤进展和随后丧失切除机会的独立预测因素。
3
安全性
在接受新辅助三联疗法的205例患者中,三分之一发生了3或4级不良事件,83.9%发生了任何级别的不良事件。常见不良事件包括呕吐、高血压、腹痛、低蛋白血症、皮疹、腹水、食欲下降等。
术后并发症方面,与直接肝切除术相比,新辅助三联疗法后接受肝切除术的患者发生肝功能不全(III/IV级)、胆汁漏(I/II级)和腹水(I/II级)的比例显著更高。但手术组无微血管侵犯的比例更高,术中出血量也更大。
结 论这项多中心回顾性研究首次提供证据表明,对于可切除的中晚期HCC,新辅助三联疗法相比直接肝切除术能获得更好的OS和EFS。然而,其生存获益必须与相关风险仔细权衡。未来需要通过随机对照试验加以验证。
原文链接:Yang DL, Qin C, Peng N, et al. Neoadjuvant transarterial chemoembolization with tyrosine kinase and immune checkpoint inhibitors improves survival from resectable hepatocellular carcinoma in a multicenter, retrospective study (GUIDANCE002). Commun Med (Lond). 2026;6(1):139. Published 2026 Mar 12. doi:10.1038/s43856-025-01303-w

钟鉴宏 教授
广西医科大学附属肿瘤医院
教授、博士、博士生导师、博士后合作导师
中国抗癌协会腔镜与机器人分会委员
广西抗癌协会理事
Infect Agent Cancer副主编、J Transl Gastroenterol副主编
iLIVER青年副主编、Hepatoma Research青年副主编
J Clin Transl Hepatol、WJH、中国癌症防治杂志等期刊编委
第一/最后通信作者在Hepatology、Ann Surg、BJS、Liver Cancer、JHEP Reports 等期刊发表SCI论著、综述和述评百余篇;28项成果被列入30多个国内外肝癌和乙肝诊疗指南;Google学术引用近万次
入选“全球前2%顶尖科学家榜单(2025)”和“终身科学家影响力”排行榜
广西八桂青年学者、广西青年科技奖获得者