文章发表封图
FRBM丨戊型肝炎病毒诱导线粒体融合:整合自噬与免疫逃逸双重机制促进病毒复制戊型肝炎病毒(HEV)是一种单链RNA病毒,主要通过粪-口途径传播,全球每年约有2 000万人感染。尽管多数感染者表现为自限性急性肝炎,但孕妇、器官移植受者及慢性肝病患者可能面临重症肝炎、肝衰竭或慢性化风险。目前临床上尚无HEV特异性抗病毒药物,主要依赖利巴韦林和干扰素治疗,但其副作用及耐药性限制了临床应用。因此,深入探索HEV与宿主细胞的相互作用,寻找新的抗病毒治疗靶点具有重要的临床意义。
线粒体是动态的细胞器,通过不断的融合与分裂维持功能稳态。线粒体不仅是细胞的“动力工厂”,也是抗病毒天然免疫信号转导的核心平台。许多病毒通过调控线粒体动力学来逃避宿主免疫清除或利用宿主资源进行复制。然而,线粒体融合在HEV感染中的演变过程及其对病毒生命周期的具体贡献,此前尚未得到系统阐明。
近日,相关研究在Free Radical Biology and Medicine上发表,题为“Mitochondrial fusion orchestrated by hepatitis E virus couples pro-viral autophagy and innate immune evasion for efficient replication”。该研究利用多种HEV感染模型,详细阐明了HEV诱导线粒体融合的分子机制及其在病毒生命周期中的生物学意义。
研究团队首先分析HEV感染者肝活检样本,发现在抗-HEV IgM阳性患者的肝组织中,线粒体呈现显著伸长的形态,且这种线粒体形态异常与患者血清AST水平升高显著相关,提示线粒体重构与肝损伤程度密切相关。
在体外模型中,无论是通过HEV基因组RNA电转还是感染性病毒颗粒接种,HEV感染均能诱发Huh7.5等多种细胞系的线粒体融合。透射电镜进一步证实,感染细胞中线粒体长度显著增加,但伴有嵴结构破坏,提示存在线粒体损伤。机制研究发现,HEV通过两阶段调控策略驱动融合:急性感染期优先上调内膜融合蛋白OPA1,而慢性感染期则转为依赖外膜融合蛋白MFN1。
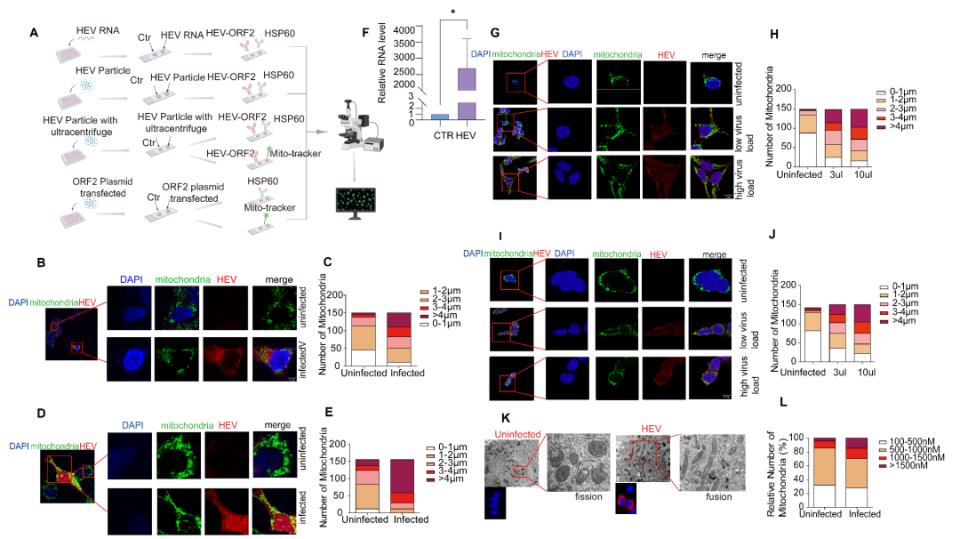
HEV在多种体外模型中诱导线粒体融合
功能实验显示,使用shRNA沉默OPA1或MFN1不仅逆转HEV诱导的线粒体融合,还显著抑制病毒复制。在HEV复制子模型中,OPA1敲低使病毒复制活性下降,而MFN1敲低在此体系中无明显影响,这一差异提示OPA1和MFN1虽共同维持线粒体融合结构,但在不同感染阶段可能存在功能偏向性。
转录组学分析进一步揭示,OPA1或MFN1缺失均显著影响自噬、细胞周期及多条免疫通路(如TNF、NF-κB信号)。机制验证表明,HEV通过OPA1/MFN1介导的线粒体融合激活自噬流(LC3-II升高、p62下降),且自噬抑制剂3-MA或CQ处理可显著抑制HEV复制,证实自噬是HEV复制所必需的。
在免疫调控方面,OPA1或MFN1敲低可显著上调干扰素(IFN-β、IFN-λ)及多种干扰素刺激基因(ISGs)的表达,且这种上调依赖于JAK-STAT通路,提示HEV通过诱导线粒体融合抑制宿主固有免疫应答,实现免疫逃逸。
此外,研究发现HEV感染诱导宿主细胞发生G0/G1期阻滞,这与CDKN1A(p21)上调及CDK4下调密切相关。通过药物(HU、洛伐他汀)将细胞同步至G0/G1期可显著增强HEV复制,而CDK4过表达则逆转了线粒体融合并抑制病毒复制,证明细胞周期阻滞是HEV维持线粒体融合的上游调控事件。
该研究首次系统阐明了HEV通过诱导宿主细胞G0/G1期阻滞,进而驱动线粒体融合,并协同促进自噬、抑制固有免疫,从而构建有利于病毒复制的细胞内环境。这一发现不仅揭示了HEV独特的致病机制,还提示线粒体融合相关蛋白(OPA1、MFN1)有望成为抗HEV治疗的新靶点。
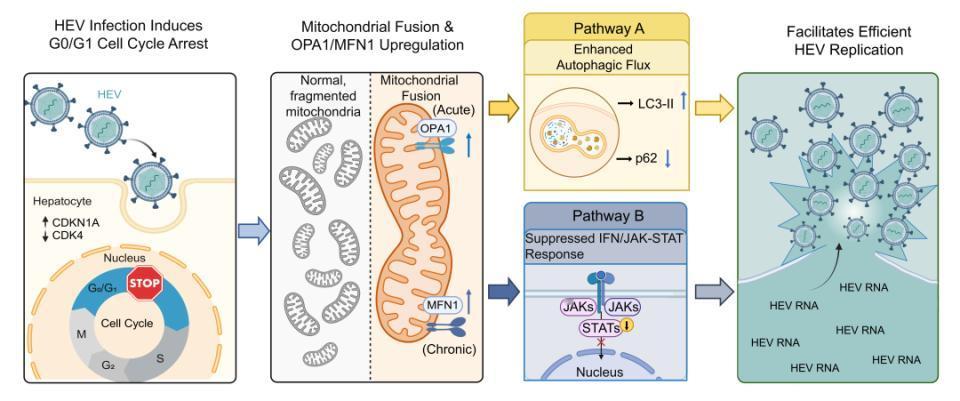
研究机制图
南方科技大学王艺瑾教授和深圳市第三人民医院(南方科技大学第二附属医院)袁静教授为本文共同通讯作者。刘小曼、蒋义韵、王晨、李家磊为该论著的共同第一作者。

通讯作者
王艺瑾
南方科技大学副教授,研究员,博士生导师。长期从事感染及代谢性肝脏疾病免疫调节机制研究,以第一/通讯作者在Science Advances、Lancet Respiratory Medicine、Gastroenterology、Journal of Hepatology、Hepatology、EBioMedicine、Metabolism等权威期刊发表论文30余篇;入选2022全球前2%科学家榜单;相关成果多次获得欧洲、亚太肝病年会青年科学家奖。主持国家自然科学基金3项,省部级课题5项。获北京市科技新星、广东省珠江人才、深圳市海外高层次人才。牵头成立了中国戊型肝炎研究协作组(CCSHE),并牵头发布《中国戊型病毒性肝炎院内筛查管理流程专家共识(2023年版)》。

第一作者
刘小曼
南方科技大学在读博士。主要研究方向为应用单细胞多组学技术,解析线粒体动力学在戊型肝炎病毒复制及致病机制中的作用,并开展病毒性肝炎的基础与转化研究。